Unzureichendes Wachstum der R-Zacke in v1 v3. Merkmale der elektrokardiographischen Diagnostik bei Menschen älterer Altersgruppen. So erstellen Sie ein EKG
Umkehrung negativer T-Wellen bei Patienten mit akutem Myokardinfarkt als Manifestation einer falsch-negativen EKG-Dynamik.
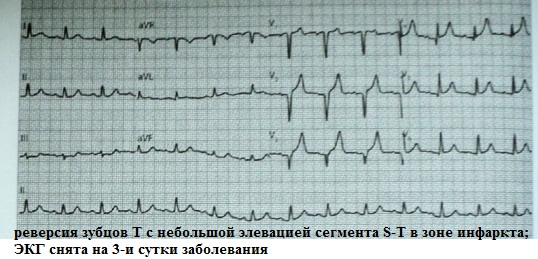
Das Koechker-Syndrom tritt am 2.–5. Tag des Myokardinfarkts auf; ist nicht mit einer Rethrombose und dem Auftreten (Verstärkung) klinischer Anzeichen einer linksventrikulären Insuffizienz verbunden. Mit anderen Worten, das ist kein rückfall Herzinfarkt. Die Dauer des Koechker-Syndroms beträgt in der Regel nicht mehr als 3 Tage. Anschließend kehrt das EKG-Bild zu seinem ursprünglichen Zustand zurück: Die T-Welle wird negativ oder isoelektrisch. Die Gründe für dieses EKG-Muster sind unbekannt. Ich bin beeindruckt von der Ansicht, dass es sich um eine Manifestation einer Episthenocarditis-Perikarditis handelt; Allerdings werden bei diesem Syndrom keine charakteristischen Herzbeutelschmerzen beobachtet. Durch die richtige Interpretation des Koechker-Syndroms können Sie unnötige medizinische Eingriffe vermeiden: Thrombolyse oder PCI. Prävalenz: ~1 von 50 Fällen von Myokardinfarkt.
(Synonym: Gedächtnisphänomen) – unspezifische Veränderungen im Endteil des Ventrikelkomplexes (hauptsächlich der T-Welle) bei spontanen Kontraktionen, die bei längerer künstlicher (künstlicher) rechtsventrikulärer Stimulation auftreten.

Die künstliche Stimulation der Ventrikel geht mit einer Verletzung der Geometrie ihrer Kontraktion einher. Bei mehr oder weniger langfristiger Stimulation (von 2-3 Monaten) können in vielen EKG-Ableitungen Veränderungen im QRS-Komplex in spontanen Kontraktionen in Form negativer T-Wellen auftreten. Eine solche Dynamik simuliert ischämische Veränderungen. Andererseits macht dieses Phänomen bei echten Angina pectoris-ähnlichen Schmerzen die Diagnose eines kleinherdigen Myokardinfarkts nahezu unmöglich. Durch die richtige Interpretation des Shaterrier-Phänomens können unnötige Krankenhausaufenthalte und ungerechtfertigte medizinische Eingriffe vermieden werden.
Es ist wichtig zu verstehen, dass das Shaterier-Phänomen nicht nur vor dem Hintergrund einer längeren künstlichen Stimulation des Herzens auftreten kann – dies ist der Hauptgrund, aber nicht der einzige. Bei chronischer Blockade des Schenkelbündels, bei häufiger ventrikulärer Extrasystole oder beim WPW-Phänomen kann sich auch der Endteil des Ventrikelkomplexes bei normalen Kontraktionen verändern – es bilden sich negative oder T-Wellen mit niedriger Amplitude.
Daher können alle langfristigen Störungen in der Geometrie der ventrikulären Kontraktion aufgrund einer abnormalen Leitung des intraventrikulären Impulses mit dem Shaterrier-Phänomen einhergehen.
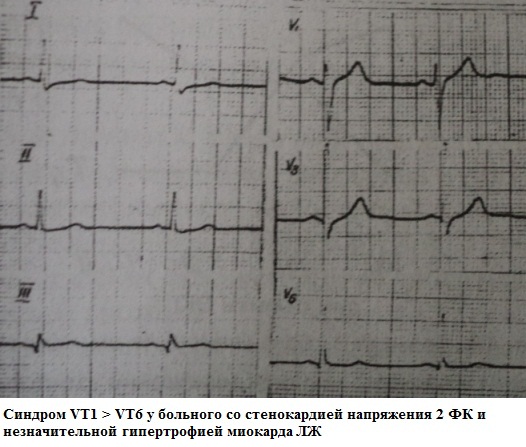
Es wurde festgestellt, dass im EKG gesunder Menschen die Amplitude der T-Welle in V6 immer etwa 1,5-2 mal größer ist als die Amplitude der T-Welle in V1. Darüber hinaus spielt die Polarität der T-Welle in V1 keine Rolle. Verletzung dieser Beziehung, wenn sich die Amplituden der T-Wellen in V1 und V6 „ausgleichen“ oder Zinn V1 überschreitet T in V6 ist eine Abweichung von der Norm. Dieses Syndrom wird am häufigsten bei Bluthochdruck (manchmal ist dies das früheste Anzeichen einer LV-Myokardhypertrophie) und bei verschiedenen klinischen Formen der koronaren Herzkrankheit beobachtet. Es kann auch ein frühes Anzeichen einer Digitalis-Intoxikation sein.
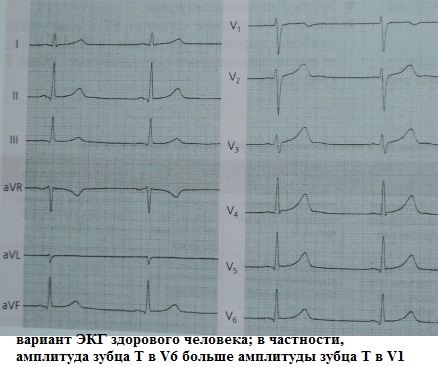


Die klinische Bedeutung dieses Syndroms ermöglicht es Ihnen, „nicht normal“ zu vermuten und bei Bedarf die diagnostische Suche „von einfach bis komplex“ fortzusetzen.
In den meisten Fällen nimmt die Amplitude der R-Welle in den „rechten“ Brustableitungen zu und erreicht bei Ableitung V3 mindestens 3 mm. In Situationen, in denen die Amplitude der R-Welle in V3 weniger als 3 mm beträgt, ist es sinnvoll, vom Syndrom des unzureichenden Wachstums der R-Welle von V1 nach V3 zu sprechen. Dieses Syndrom kann in 2 Kategorien unterteilt werden:
1. Es gibt keine weiteren Auffälligkeiten im EKG.
Variante der Norm (häufiger bei hypersthenischer Konstitution),
Anzeichen einer LV-Myokardhypertrophie,
Falsche Platzierung der Brustelektroden (V1-V3) im Interkostalraum darüber.
2. Es gibt andere Auffälligkeiten im EKG.
Typisch für die folgenden klinischen Situationen:
- aktueller Myokardinfarkt (in diesem Fall kommt es zu einer EKG-Dynamik in den Ableitungen V1-V3, die für einen Herzinfarkt charakteristisch ist),
Kardiosklerose nach Infarkt,
Schwere LV-Myokardhypertrophie mit anderen EKG-Kriterien für Hypertrophie,
Blockade des LBP (vollständig oder unvollständig), Blockade des vorderen Astes des LBP,
- Rechtsventrikuläre Hypertrophie vom S-Typ (selten).




Schwierigkeiten bei der Interpretation des Syndroms des unzureichenden Wachstums der R-Zacke von V1 nach V3 ergeben sich in der Regel, wenn es als eigenständiges, asymptomatisches EKG-Muster diagnostiziert wird und keine anderen EKG-Auffälligkeiten vorliegen. Bei korrekt angelegten Brustelektroden und fehlender kardialer Vorgeschichte liegt die Hauptursache in einer mäßigen Hypertrophie des LV-Myokards.
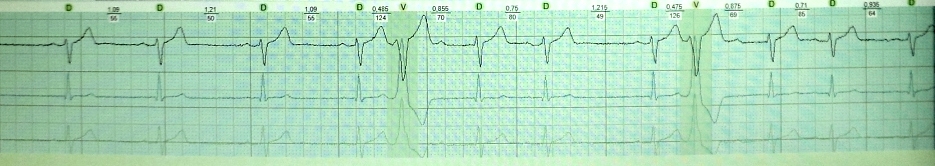
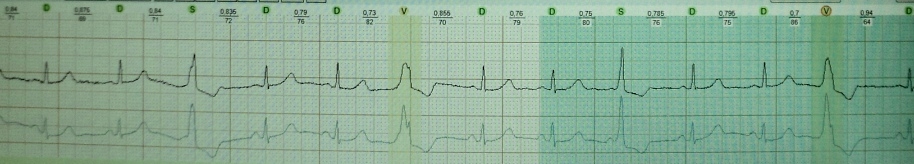
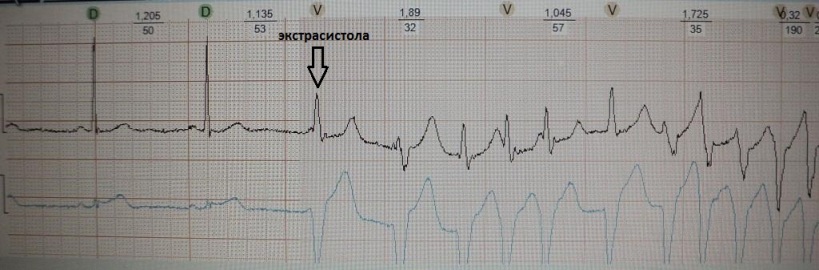
Wie Sie wissen, wird eine vorzeitige Kontraktion des Herzens Extrasystole genannt. Das zusätzliche Anregungskopplungsintervall ist kürzer ( kurz) Intervall zwischen den Hauptkontraktionen. Es folgt eine Ausgleichspause ( lang), was mit einer Verlängerung der Herzfeuerfestigkeit und einer Zunahme ihrer Streuung (Feuerfestigkeitsstreuung) einhergeht. In diesem Zusammenhang besteht unmittelbar nach einer postextrasystolischen Sinuskontraktion die Möglichkeit einer erneuten Extrasystole ( kurz) - das „Produkt“ der Feuerfestigkeitsdispersion. Mechanismus der „wiederholten“ Extrasystole: Wiedereintritt oder frühe Postdepolarisation. Beispiele:
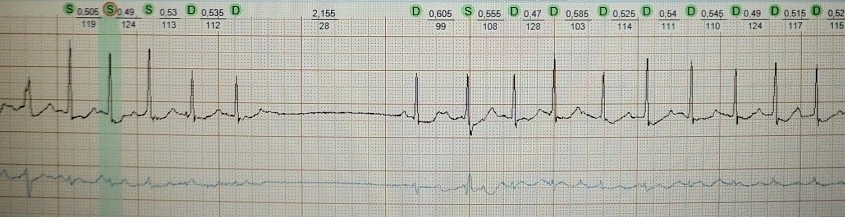
kurz-lang-kurz bei einem Patienten mit funktioneller Brady-abhängiger Extrasystole, die in diesem Fall keine besondere klinische Bedeutung hat:
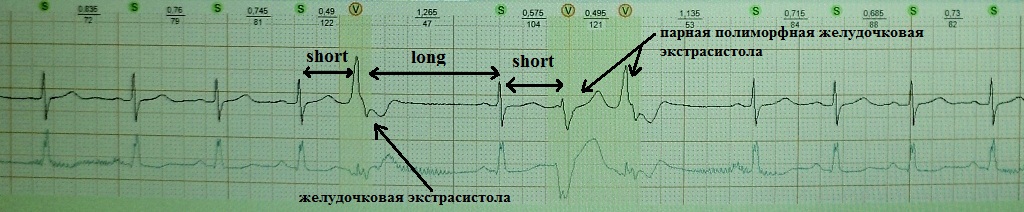
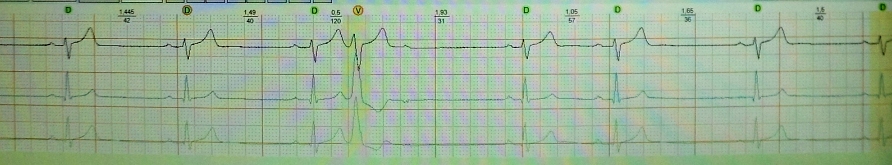
Kurz-lang-kurz bei einem Patienten mit schwerem Schlafapnoe-Syndrom, Fettleibigkeit und Bluthochdruck im Stadium 3. Wie wir sehen können, trat nach einer kompensatorischen Pause eine paarweise polymorphe ventrikuläre Extrasystole auf. Bei diesem Patienten kann das Kurz-Lang-Kurz-Phänomen eine polymorphe ventrikuläre Tachykardie auslösen und zum plötzlichen Tod führen:
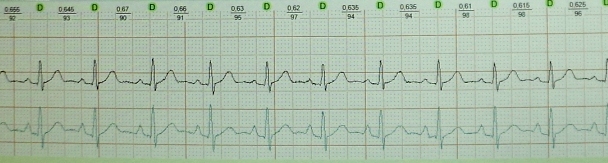
Kurz-lang-kurz bei einem Patienten mit langem QT-Syndrom: Auslösung einer VT vom Typ „Pirouette“. Manchmal ist bei diesem Syndrom das Kurz-Lang-Kurz-Phänomen Voraussetzung für die Auslösung einer ventrikulären Tachyarrhythmie:
Bei Patienten mit funktioneller Extrasystole hat das Kurz-Lang-Kurz-Phänomen keine klinische Bedeutung; es „erleichtert“ nur das Auftreten einer Brady-abhängigen Extrasystole. Bei Patienten mit schweren organischen Herzerkrankungen und Kanalopathien kann dieses Phänomen lebensbedrohliche ventrikuläre Arrhythmien auslösen.
Dieser Begriff bezieht sich auf einen Zeitraum im Herzzyklus, in dem die Weiterleitung eines vorzeitigen Impulses unmöglich (oder verlangsamt) wird, obwohl Impulse mit weniger vorzeitigen Impulsen weitergeleitet werden. Unterschiede in der Feuerfestigkeit auf verschiedenen Ebenen des Reizleitungssystems des Herzens liefern die elektrophysiologische Grundlage für dieses Phänomen.
Im ersten EKG sehen wir eine frühe Vorhofextrasystole in die Ventrikel ohne Aberration. Im zweiten EKG ist das Kopplungsintervall der Vorhofextrasystole länger, die Extrasystole wird jedoch verzögert in die Herzkammern weitergeleitet (Aberration).
Das „Lücken“-Phänomen tritt vor allem bei Spezialisten auf, die kardiale Elektrophysiologie durchführen.
- Kurzzyklus-Aberration (3. Phasenblock), die auftritt, wenn die Refraktärzeit der AV-Verbindung aufgrund einer plötzlichen Verlängerung des Intervalls zwischen zwei vorherigen Kontraktionen zunimmt. Je länger das Intervall zwischen den Kontraktionen ist, desto höher ist die Wahrscheinlichkeit einer fehlerhaften Leitung (oder Blockierung) des nächsten supraventrikulären Impulses.
Ein klassisches Beispiel für das Ashman-Phänomen bei Vorhofflimmern:
Ashman-Phänomen, das nach einer postextrasystolischen Kompensationspause auftrat:
Blockierung der Vorhofextrasystole, die nach einer spontanen Verlängerung des Intervalls zwischen den Sinuskontraktionen auftritt:
Klinische Bedeutung des Ashman-Phänomens: Durch seine korrekte Interpretation kann eine Überdiagnose von a) ventrikulärer Extrasystole und b) organischen Erregungsleitungsstörungen im AV-Übergang vermieden werden.
Kontinuierlich rezidivierender Verlauf des paroxysmalen Vorhofflimmerns, wenn nach dem Ende eines Anfalls, nach 1-2 Sinuskontraktionen, ein neuer Anfall beginnt.
Charakteristisch für vagusabhängiges Vorhofflimmern. Das Phänomen spiegelt einerseits die hohe ektopische Aktivität der Muskelkupplungen der Lungenvenen wider, andererseits die hohe profibrillatorische Bereitschaft des Vorhofmyokards.
Neben der retrograden Erregung der Vorhöfe besteht die Möglichkeit, dass der ventrikuläre Impuls mit seiner Entladung unterschiedlich tief in den AV-Übergang eindringt (Refraktärverlängerung, Blockade). Dadurch werden nachfolgende supraventrikuläre Impulse (normalerweise 1 bis 3) verzögert (aberriert) oder blockiert.
Verdeckte VA-Überleitung aufgrund von PVCs, die zu einem funktionellen AV-Block der Stufe 1 führt:
Versteckte VA-Überleitung aufgrund von PVCs, die zu einem funktionellen AV-Block der Stufe 2 führt:
Verdeckte VA-Überleitung aufgrund von PVCs, begleitet von einer nachpositionierten (verschobenen) kompensatorischen Pause:

Klinische Bedeutung der versteckten AV-Überleitung: Die richtige Interpretation dieses Phänomens ermöglicht die Unterscheidung zwischen funktionellen und organischen AV-Blockaden.
Bei den meisten Menschen ist der AV-Knoten homogen. In einigen Fällen ist der AV-Knoten elektrophysiologisch in eine schnelle und eine langsame Leitungszone unterteilt (dissoziiert). Wenn ein Mensch subjektiv gesund ist, hat dieses Phänomen keine klinische Bedeutung. Bei einigen Patienten geht die Dissoziation des AV-Knotens jedoch mit der Entwicklung von Anfällen einer nodalen reziproken AV-Tachykardie einher. Auslöser der Tachykardie ist die supraventrikuläre Extrasystole, die auf dem schnellen Weg abläuft und auf dem langsamen Weg nur retrograd verläuft – die Re-entry-Schleife ist geschlossen. Das Phänomen der AV-Knoten-Dissoziation wird durch die Elektrophysiologie des Herzens zuverlässig nachgewiesen. Allerdings kann ein normales EKG manchmal Anzeichen einer dissoziativen Erkrankung erkennen.
Betrachten wir den folgenden klinischen Fall. Eine 30-jährige Patientin klagt über Anfälle von unmotiviertem Herzklopfen. Es wurde eine tägliche EKG-Überwachung durchgeführt.
Fragment eines EKG - normale Variante:
EKG-Fragment – AV-Block im 1. Stadium. vor dem Hintergrund einer Sinustachykardie – absolut untypisch für die Norm:
EKG-Fragment – AV-Block im 2. Stadium, Typ 1. Beachten Sie die „schnelle“ Verlängerung des P-R-Intervalls, gefolgt vom Verlust der ventrikulären Welle:
Ein plötzlicher Anstieg des P-R-Intervalls um mehr als 80 ms lässt an die Dissoziation des AV-Knotens in Zonen mit unterschiedlichen Impulsleitungsgeschwindigkeiten denken. Das sehen wir in diesem Beispiel. Anschließend wurde der Patient einer kardialen Elektrophysiologie unterzogen: Es wurde eine reziproke Tachykardie im AV-Knoten festgestellt. Die Ablation des langsamen AV-Knotenwegs wurde mit guter klinischer Wirkung durchgeführt.
So ermöglichen Anzeichen einer AV-Knoten-Dissoziation im Oberflächen-EKG (Wechsel von normalen und verlängerten P-R-Intervallen; eine einmalige Erhöhung des P-R-Intervalls in der Wenckebach-Periode um mehr als 80 ms) in Kombination mit einer arrhythmischen Vorgeschichte die Feststellung eine Diagnose mit hoher Wahrscheinlichkeit noch vor der kardialen Elektrophysiologie.
Trotz der scheinbar unglaublichen Natur dieses Phänomens ist es nicht so selten. Das Kent-Bündel dient nicht nur als zusätzlicher Weg zur Impulsleitung von den Vorhöfen zu den Ventrikeln, sondern ist auch zur Automatik (spontane diastolische Depolarisation) fähig. Eine Extrasystole aus dem Kent-Bündel kann vermutet werden, wenn im EKG Anzeichen des WPW-Phänomens mit einer spätdiastolischen Ektopie kombiniert werden, was eine ventrikuläre Extrasystole simuliert. In diesem Fall stellt der erweiterte Ventrikelkomplex eine kontinuierliche Deltawelle dar.
Betrachten Sie das folgende klinische Beispiel. Eine 42-jährige Frau klagte über Anfälle von unmotiviertem Herzklopfen. Es wurde eine zweitägige EKG-Überwachung durchgeführt. Am ersten Tag der Studie wurden etwa 500 „erweiterte“ ventrikuläre Komplexe registriert, die in der Spätdiastole auftraten und mit erhöhter Herzfrequenz verschwanden. Auf den ersten Blick eine harmlose funktionelle ventrikuläre Extrasystole. Die kalziumabhängige spätdiastolische ventrikuläre Extrasystole tritt jedoch hauptsächlich vor dem Hintergrund der Tachysystole oder unmittelbar nach deren Ende auf. In diesem Fall werden späte ventrikuläre Komplexe bei normaler Herzfrequenz und Bradykardie aufgezeichnet, was an sich schon seltsam ist.
Die Situation wurde am zweiten Tag der Überwachung völlig klar, als Anzeichen einer intermittierenden ventrikulären Präexitation auftraten. Es wurde deutlich, dass spätdiastolische Ventrikelkomplexe nichts anderes als eine Extrasystole aus dem Kent-Bündel sind.
Klinische Bedeutung der Extrasystole aus dem Kent-Bündel: Die korrekte Interpretation dieses Phänomens ermöglicht es uns, die Diagnose einer ventrikulären Extrasystole auszuschließen und den Diagnose- und Behandlungsprozess in die notwendige Richtung zu lenken.
Es wird bei supraventrikulären Tachyarrhythmien, insbesondere bei Vorhofflimmern, beobachtet. Der Kern des Phänomens besteht darin, dass supraventrikuläre Impulse, die häufig und unregelmäßig am AV-Übergang ankommen, diesen unterschiedlich tief durchdringen; Entladen Sie es, ohne die Ventrikel zu erreichen. Infolgedessen verlangsamt sich 1) die Weiterleitung nachfolgender supraventrikulärer Impulse, 2) der ektopische Ersatzimpuls verlangsamt sich (fällt aus).
Im Oberflächen-EKG kann das Phänomen der verdeckten AV-Überleitung anhand folgender Anzeichen angezeigt werden:
Wechsel von kurzen und langen R-R-Intervallen bei Vorhofflimmern:
Keine Fluchtkomplexe in zu großen Abständen R-R bei Vorhofflimmern:
Fehlen von Fluchtkomplexen während einer Pause von mehreren Sekunden, wenn der Sinusrhythmus wiederhergestellt ist:
Wenn regelmäßiges Vorhofflattern in unregelmäßiges oder Vorhofflimmern übergeht:
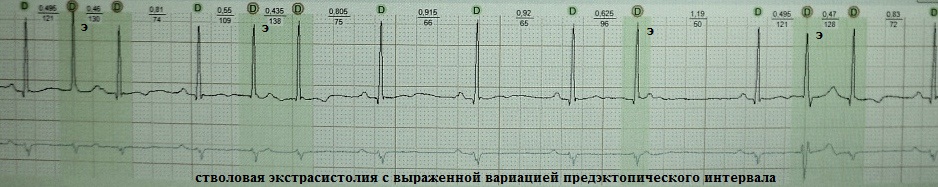
Die Extrasystole aus den distalen Teilen des AV-Knotens (Stamm des His-Bündels) ist eine Art ventrikuläre Extrasystole und wird „Stamm“ genannt. Ich bezeichne diese Art von Extrasystole als arrhythmisches Phänomen, erstens wegen ihrer relativen Seltenheit, zweitens wegen ihrer äußerlichen Ähnlichkeit mit einer typischen parietalen ventrikulären Extrasystole und drittens wegen ihrer Resistenz gegenüber herkömmlichen Antiarrhythmika.
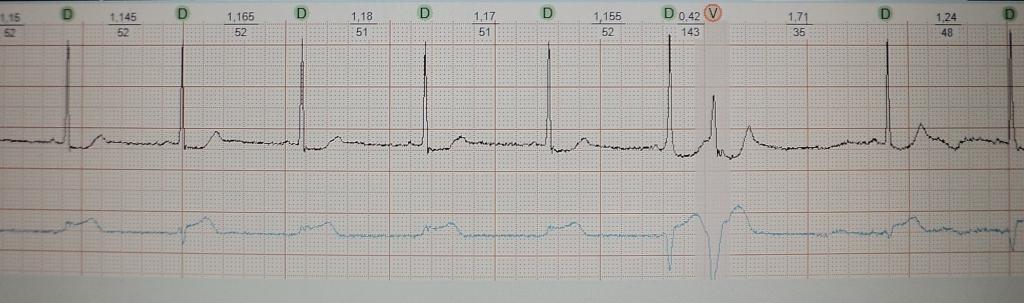
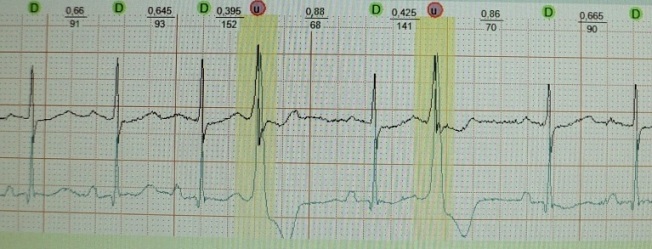
Klinische und elektrokardiographische Anzeichen einer Stammextrasystole: 1) Der QRS-Komplex hat oft ein supraventrikuläres Aussehen oder ist aufgrund sporadischer Aberrationen oder aufgrund der Nähe zum proximalen Teil eines der Schenkeläste leicht verbreitert; 2) eine retrograde Aktivierung der Vorhöfe ist nicht typisch; 3) das Kopplungsintervall ist variabel, da die Hirnstammlokalisation des extrasystolischen Fokus auf eine kalziumabhängige Depolarisation hindeutet – also einen abnormalen Automatismus; 4) absolut refraktär gegenüber Antiarrhythmika der Klassen I und III.
Beispiele:
Bei der Stammextrasystole kann eine gute klinische Wirkung nur bei langfristiger Anwendung von Antiarrhythmika der Klasse II oder IV erzielt werden.
- Durchführen eines Impulses anstelle der erwarteten Blockade (Aberration).
Beispiel 1:
Wahrscheinlicher Mechanismus: Der Vorhofimpuls hat die LAP in ihrer übernormalen Phase erfasst.
Beispiel #2:
Wahrscheinlicher Mechanismus: Die Größe des spontanen diastolischen Potenzials im His-Purkinje-System ist unmittelbar nach dem Ende der Repolarisation der „Sinus“-Kontraktionen maximal (in unserem Fall werden sie aufgrund der LBP-Blockade erweitert), daher haben frühe Vorhofimpulse die größte Chance der „normalen“ Leitung.
Beispiel Nr. 3 (umgekehrtes Ashman-Phänomen):

Wahrscheinlicher Mechanismus: das Phänomen einer „Lücke“ (Ausfall) in der Leitung; Verkürzung der Feuerfestigkeit, wenn sich die Länge des vorherigen Zyklus ändert.
Plötzliche Sinuspausen im EKG können nicht immer eindeutig interpretiert werden. Manchmal ist für die richtige Interpretation des Phänomens neben einer gründlichen Analyse des Kardiogramms selbst eine umfassende klinische und anamnestische Beurteilung erforderlich. Beispiele:
Pausen während einer Sinusarrhythmie können so ausgeprägt sein, dass ein Missverständnis über das Vorliegen einer SA-Blockade entsteht. Es muss daran erinnert werden, dass Sinusarrhythmien asymptomatisch sind; typisch hauptsächlich für junge und mittlere Menschen, einschließlich subjektiv gesunder Menschen; erscheint (verstärkt) mit Bradykardie (normalerweise nachts); die Pausen selbst sind nie zu lang, ohne dadurch den Anschein von Abrutschkomplexen zu erwecken; Kardioeurotische Symptome sind ein häufiger klinischer Begleiter.
Sinusblock 2. Grades:

Es ist notwendig herauszufinden, um welche Art von Blockade es sich handelt: 1. oder 2. Blockade. Dies ist eine grundsätzliche Frage, da die Prognose unterschiedlich ist. Eine SA-Blockade, Stadium 2, Typ 1, tritt bei jungen, gesunden Personen häufig im Ruhezustand (insbesondere nachts) auf; in klassischen Fällen gehen ihr klinisch und elektrokardiographisch Wenkibachs Zeitschriften voraus; in der Regel überschreitet die Pausenlänge nicht das Doppelte des R-R-Intervalls der vorangegangenen Kontraktionen; das Vorhandensein von Gleitkomplexen ist nicht typisch; Es gibt keine Vorgeschichte von Synkopen.

SA-Blockade, Stadium 2, Typ 2, tritt plötzlich ohne Wenkibach-Periodizität auf; häufig liegt gleichzeitig eine organische Myokardschädigung vor, die instrumentell festgestellt wird; Bei älteren Menschen ohne offensichtliche Veränderungen am Herzen während ECHO ist die Hauptursache Kardiosklerose; die Pause kann länger als das Doppelte des R-R-Intervalls der vorherigen Wehen sein; Es treten häufig Gleitkomplexe auf. Charakteristisch ist eine Synkopenanamnese oder Ähnliches.


Blockierte Vorhofextrasystole:
In der Regel führt es nur dann zu Schwierigkeiten bei der Diagnose, wenn die Anzahl der blockierten Extrasystolen gering ist und die Anzahl der gewöhnlichen (nicht blockierten) Extrasystolen die statistische Norm nicht überschreitet – dies schwächt die Wachsamkeit des Arztes. Durch die grundlegende Sorgfalt bei der EKG-Analyse können Sie eine blockierte Vorhofextrasystole zuverlässig überprüfen. Meiner Erfahrung nach verformt eine extrem frühe blockierte ektopische P-Welle die T-Welle immer in dem einen oder anderen Grad, was es ermöglicht, dieses Phänomen ohne EPI zu diagnostizieren.
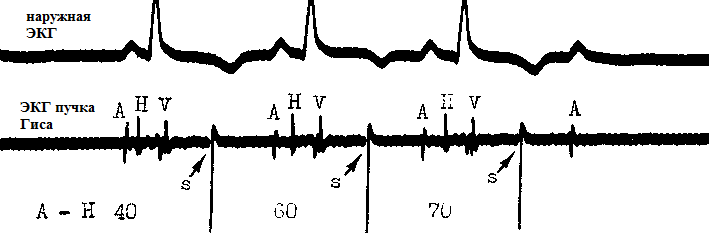
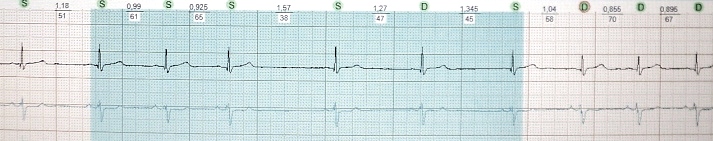
Indem ich in diesem Abschnitt die versteckte Extrasystole erwähne, möchte ich die extreme Ungewöhnlichkeit dieses Phänomens würdigen. Es handelt sich um eine Stammextrasystole, deren Erregungsleitung antero- und retrograd blockiert ist. Daher ist es im Oberflächen-EKG nicht sichtbar. Die Diagnose ist nur mit der His-Bündel-Elektrokardiographie möglich. In der obigen Abbildung wird die Stammextrasystole künstlich provoziert: Reiz S. Wie wir sehen können, reichen S-Reize nicht über den AV-Übergang hinaus und sind daher im EKG nicht sichtbar. Der dritte auferlegte Reiz verursacht einen vorübergehenden AV-Block 2. Grades ("). Bei einem externen EKG kann eine versteckte Hirnstammextrasystole vermutet werden, wenn eine Kombination aus herkömmlichen (kabelgebundenen) AV-Extrasystolen und plötzlichen Herzpausen ähnlich einem AV-Block 2. Grades vorliegt.
Aberration mit zunehmender Frühgeburt überrascht niemanden – da sie mit einem schnellen Anstieg der Herzfrequenz verbunden ist, wenn die Refraktärität im Reizleitungssystem noch keine Zeit hatte, sich zu verkürzen. Die Aberration sieht viel ungewöhnlicher aus, wenn sich die Herzfrequenz verlangsamt, wenn es den Anschein hat, dass die Refraktärzeit offensichtlich vorbei ist.

Die Grundlage für die Aberration eines langen Zyklus ist die Fähigkeit der Zellen des His-Purkinje-Systems zur spontanen diastolischen Depolarisation. Bei einer Unterbrechung der Herzarbeit kann daher das Membranpotential in einigen Teilen des Reizleitungssystems des Herzens den Wert des Ruhepotentials erreichen („kritische Hypopolarisation“), wodurch es langsamer wird oder unmöglich wird den nächsten Impuls durchführen. Man muss verstehen, dass eine solche Situation fast immer eine organische Pathologie des Reizleitungssystems widerspiegelt, wenn sich die Zellen des AV-Übergangs zunächst in einem Zustand der Hypopolarisation befinden (niedriger Wert des maximalen diastolischen Potenzials). Das Phänomen der Brady-abhängigen Blockade ist für ein gesundes Herz nicht typisch und geht häufig schwereren Erregungsleitungsstörungen voraus.
Bedeutet wörtlich: Unterdrückung von Herzschrittmachern durch häufigere Impulse. Dieses Phänomen beruht auf der Hyperpolarisierung automatischer Zellen aufgrund der Tatsache, dass sie häufiger aktiviert werden als ihre eigene Erregungsfrequenz. Dieses physiologische Phänomen können wir im EKG eines jeden gesunden Menschen beobachten, wenn der Sinusknoten alle untergeordneten Schrittmacher unterwirft. Je höher die Sinusrhythmusfrequenz, desto geringer ist die Wahrscheinlichkeit heterotoper Impulse, einschließlich Extrasystole. Wenn andererseits die Impulsfrequenz des ektopischen Fokus die Automatizität des Sinusknotens überschreitet, wird der Sinusknoten selbst einer Überfrequenzunterdrückung unterzogen. Letztere Tatsache erregt häufig ärztliche Aufmerksamkeit, da die Pause nach der Wiederherstellung des Sinusrhythmus übermäßig lang sein kann. Zum Beispiel:
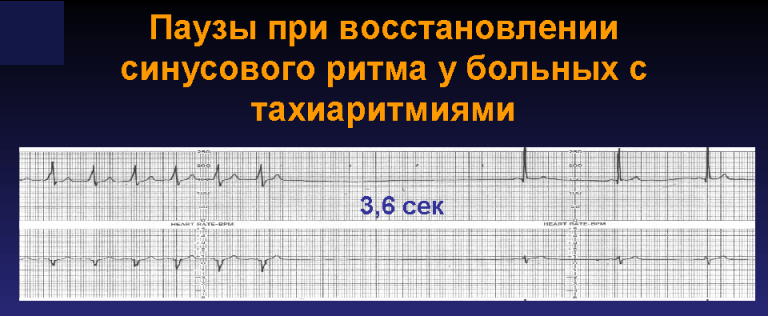

Mit EPI wird eine Funktionsstörung des Sinusknotens durch das Phänomen der „Overdrive-Unterdrückung“ erkannt.
Im Frühstadium spricht man von ventrikulärer Extrasystole Typ R auf T und atrialer Extrasystole Typ P auf T.
Bei aller Wahrscheinlichkeit des Auftretens solcher Extrasystolen bei einem gesunden Menschen (insbesondere atrialen) muss beachtet werden, dass sie für ein normales Myokard umso weniger typisch sind, je kürzer die Vorzeitigkeit der Extraerregung ist. Daher ist es beim erstmaligen Auftreten einer frühen Extrasystole notwendig, klinisch und instrumentell das Vorhandensein einer Varianz in der Refraktärität des Myokards zu beurteilen – d. h. die Wahrscheinlichkeit, durch eine Extrasystole eine Tachyarrhythmie auszulösen. Eine frühe Vorhofextrasystole, die von den Muskelverbindungen der Lungenvenenmündungen herrührt, wird häufig bei Menschen mittleren Alters festgestellt. Am häufigsten äußert es sich durch einen Reflexmechanismus im Rahmen einer extrakardialen Erkrankung aufgrund von falscher Lebensstil. Und wenn die Ursache der Arrhythmie nicht beseitigt wird, beginnt früher oder später eine frühe Vorhofextrasystole, Vorhofflimmern auszulösen. Die Kombination aus frühen atrialen Extrasystolen, Dilatation des linken Vorhofs und Bluthochdruck (oder latenter arterieller Hypertonie) ist der zuverlässigste klinische Prädiktor für eine zukünftige atriale Tachyarrhythmie. Bei älteren Menschen wird in den meisten Fällen eine frühe Vorhofextrasystole festgestellt.
Eine viel größere Verantwortung liegt bei der klinischen Analyse der frühen ventrikulären Extrasystole auf den Schultern des Arztes – denn lebensbedrohliche ventrikuläre Rhythmusstörungen werden fast immer durch das R-auf-T-Phänomen ausgelöst. Bei einem gesunden Menschen kann eine frühe ventrikuläre Extrasystole nur dagegen erfasst werden der Hintergrund eines schnellen Rhythmus; wenn es langsamer wird, wird es mitteldiastolisch:
Ein isoliertes R-auf-T-Phänomen vor dem Hintergrund einer Normo- oder Bradykardie ist immer verdächtig hinsichtlich seines besonderen elektrophysiologischen Ursprungs: der frühen Nachdepolarisation. Bekanntlich gibt es im gesunden Myokard keine Bedingungen für frühe Nachdepolarisationen (insbesondere im ventrikulären Myokard). Wenn daher die offensichtlichen Ursachen einer frühen ventrikulären Extrasystole in Form einer akuten oder chronischen organischen Schädigung des Myokards abgelehnt werden, müssen andere – angeborene – ausgeschlossen werden. Ich möchte Sie daran erinnern, dass bei der sogenannten elektrischen Herzkrankheit die frühe ventrikuläre Extrasystole für lange Zeit die einzige Manifestation einer versteckten Pathologie sein kann.
Es besteht noch kein Konsens über den Ursprung der U-Welle. Die Frage nach der klinischen Bedeutung bleibt umstritten. Es gibt mehrere Theorien zu seiner Entstehung:
1) Die U-Welle wird durch Spätpotentiale verursacht, die ihren eigenen Aktionspotentialen folgen.
2) Die U-Welle wird durch Potentiale verursacht, die aus der Dehnung der Ventrikelmuskulatur während der Phase der schnellen Füllung der Ventrikel in der frühen Phase der Diastole resultieren.
3) Die U-Welle wird durch Potentiale verursacht, die durch eine verzögerte späte Repolarisation induziert werden, wenn die Wände des linken Ventrikels während der Diastole gedehnt werden.
4) Die U-Welle wird durch Repolarisation der Papillarmuskeln oder Purkinje-Fasern verursacht.
5) Die U-Welle wird durch elektrische Schwingungen verursacht, die durch eine mechanische Welle ausreichender Intensität an den Venenmündungen nach dem Durchgang eines normalen arteriellen Impulses entlang eines geschlossenen „Arterie-Vene“-Kreislaufs verursacht werden.
Daher basieren alle Theorien auf der Existenz bestimmter später Oszillationen, die das Transmembranpotential des Myokards zum Zeitpunkt der frühen Diastole kurzzeitig in Richtung Hypopolarisation verschieben. Ich bin näher an Theorie Nr. 2. Ein mäßig hypopolarisiertes Myokard weist eine erhöhte Erregbarkeit auf – bekanntlich fällt die U-Welle im EKG chronologisch mit der sogenannten übernormalen Phase des Herzzyklus zusammen, in der beispielsweise leicht eine Extrasystole auftritt.
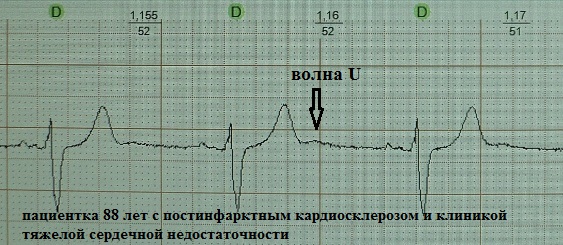
Die klinische Bedeutung der U-Welle ist ungewiss (und meiner Meinung nach unbedeutend). Normalerweise ist die U-Welle eine kleine (ca. 1,5–2,5 mm im EKG), positive, leicht abfallende Welle, die der T-Welle 0,02–0,04 Sekunden folgt. Sie lässt sich am besten in den Ableitungen V3 und V4 darstellen. Oftmals wird die U-Welle überhaupt nicht erkannt oder liegt auf der T-Welle „aufgeschichtet“. Und beispielsweise bei einer Herzfrequenz von mehr als 95-100 Schlägen pro Minute ist ihre Erkennung aufgrund der Überlappung mit dem Vorhof nahezu unmöglich P-Welle. Es wird angenommen, dass sie normalerweise bei gesunden jungen Menschen die größte Amplitude hat. Theoretisch kann es jedoch in jeder klinischen Situation auftreten und während der Tachysystole an Amplitude zunehmen:

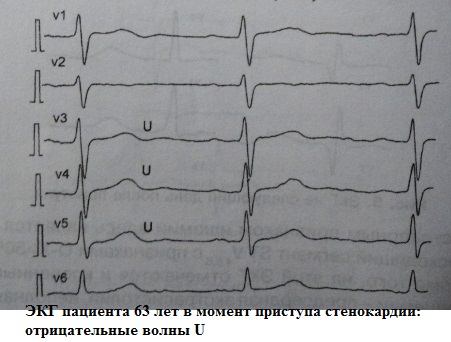
Es wird angenommen, dass eine negative U-Welle absolut nicht typisch für die Norm ist. Eine negative U-Oszillation ist fast immer mit irgendeiner Pathologie verbunden. Eine andere Sache ist, dass der diagnostische Wert einer solchen Umkehrung völlig unterschiedlich sein kann:
Es ist richtig, von der ersetzenden („rettenden“) Rolle des ventrikulären Rhythmus nur dann zu sprechen, wenn er vor dem Hintergrund eines Herzstillstands während einer „paroxysmalen“ SA oder AV-Blockade oder während einer passiven AV-Dissoziation auftritt. In anderen Situationen haben wir es mit einem beschleunigten idioventrikulären Rhythmus (AVR) zu tun, der scheinbar unmotiviert („aktiv“) ist. Seine Frequenz überschreitet nicht 110-120 pro Minute, andernfalls wird eine ventrikuläre Tachykardie diagnostiziert. Es gibt mehrere Gründe für das Auftreten von UIR:
Reperfusionssyndrom bei akutem Myokardinfarkt,
Bekannte organische Herzerkrankung mit verminderter linksventrikulärer systolischer Funktion (als Teil einer potenziell bösartigen größeren Ektopie),
Digitalis-Intoxikation,
Idiopathische Fälle bei gesunden Personen.
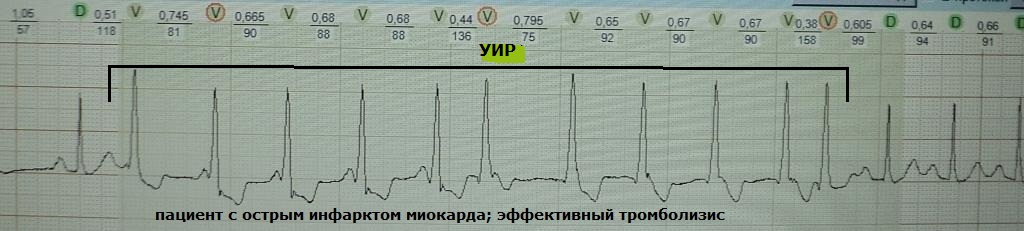
Am häufigsten treten URIs während eines akuten Myokardinfarkts zum Zeitpunkt der vollständigen oder teilweisen Rekanalisation der Koronararterie auf. In einer solchen Situation gelangt eine große Menge Kalzium in die betäubten Kardiomyozyten, was das Transmembranpotential auf den Schwellenwert verschiebt (Zellhypopolarisation); Dadurch erwerben Kardiomyozyten die Eigenschaft der Automatizität. Es ist wichtig zu wissen, dass der URI kein verlässliches Kriterium für eine erfolgreiche Reperfusion ist: Die Rekanalisation kann teilweise oder intermittierend erfolgen. In Kombination mit anderen klinischen Symptomen ist der prognostische Wert der UIR als Marker für die Wiederherstellung des koronaren Blutflusses jedoch recht hoch. Fälle von „Reperfusion“-Kammerflimmern sind sehr selten. Beispiele:
Das Reperfusionssyndrom tritt vor allem bei Krankenhausärzten auf, die auf kardiologischen Intensivstationen arbeiten; Klinikkardiologen oder Funktionsdiagnostiker befassen sich häufiger mit anderen Ursachen von URI.
Eine Digitalisvergiftung als Ursache der UID ist in den letzten Jahren immer seltener geworden. Man muss es sich einfach merken.
Die Identifizierung von UIR bei Patienten mit organischen Herzerkrankungen vor dem Hintergrund einer linksventrikulären systolischen Dysfunktion ist von großer klinischer Bedeutung. Jede ventrikuläre Ektopie in einer solchen Situation sollte als potenziell bösartig behandelt werden – sie erhöht sicherlich das Risiko eines plötzlichen Herztodes durch die Einleitung von Kammerflimmern, insbesondere wenn sie während der Erholungsphase nach dem Training auftritt. Beispiel:
Noch vor 10 bis 15 Jahren kamen Kardiologen bei der Registrierung von UID bei Menschen ohne organische Herzerkrankung zu dem Schluss, dass die klinische Prognose „unsicher“ sei – solche Probanden standen unter ärztlicher Schirmherrschaft. Langzeitbeobachtungen haben jedoch gezeigt, dass URIs das Risiko eines plötzlichen Herztodes nicht erhöhen und in solchen Fällen eine „kosmetische“ Herzrhythmusstörung darstellen. URI bei gesunden Personen ist häufig mit anderen kardialen und nichtkardialen Anomalien verbunden: WPW-Phänomen, akzessorische Chordae, frühes ventrikuläres Repolarisationssyndrom, Manifestationen Bindegewebsdysplasie-Syndrom. Die klinische Bedeutung von URI wird durch die subjektive Verträglichkeit der Arrhythmie und ihre Auswirkung auf die intrakardiale Hämodynamik (die Wahrscheinlichkeit der Entwicklung einer arrhythmogenen Dilatation des Herzens) bestimmt. Beispiele:

Der Arzt sollte sich nicht durch URI-Parameter wie Frequenzvariabilität und Polymorphismus ventrikulärer Komplexe verwirren lassen. Die Unregelmäßigkeit des Rhythmus wird durch den inneren Automatismus des ektopischen Zentrums oder die Blockade des Ausgangs mit Wenckebach-Periodizität bestimmt. Die scheinbare Polytopie ektopischer Komplexe ist in Wirklichkeit nichts anderes als eine fehlerhafte Erregungsleitung. Der allgemeine Konsens besteht darin, dass der Mechanismus der URI bei gesunden Personen eine abnormale Automatik ist.
Bei der Differentialdiagnose beschleunigter ventrikulärer Rhythmen sollten das Ashman-Phänomen, das WPW-Phänomen und ein tachy- oder bradyabhängiger Schenkelblock ausgeschlossen werden.
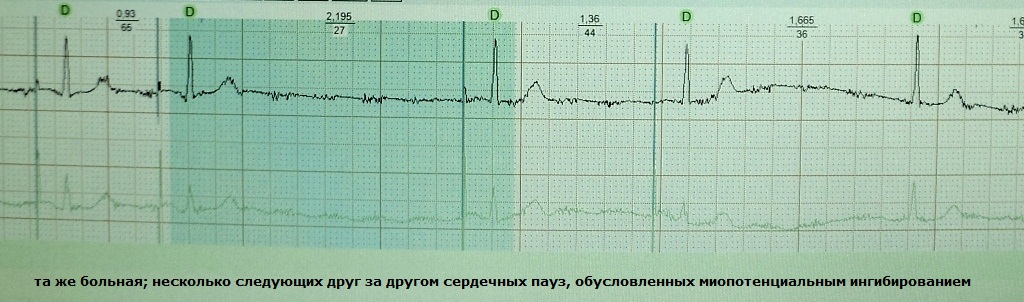
Dabei handelt es sich um eine Variante der Hypersensierung eines Herzschrittmachers auf die Potentiale der Skelettmuskulatur von Brust, Schultergürtel, Bauchmuskulatur oder Zwerchfell. Infolgedessen gibt die Erkennungselektrode, die extrakardiale Signale wahrnimmt, den Befehl, den nächsten künstlichen Impuls zu unterdrücken – es kommt zu einer Herzpause, die für den Patienten zur Ohnmacht führen kann. In der Regel wird die Hemmung des Myopotentials durch eine Aktion hervorgerufen, beispielsweise durch aktive Arbeit mit den Händen. Dieses Phänomen ist typisch für Herzschrittmacher mit monopolarer Elektrodenkonfiguration; Sie wurden in den letzten Jahren immer seltener implantiert. Beispiele:
Optionen zur Korrektur der Myopotentialhemmung: 1) Reduzierung der Empfindlichkeitsschwelle der Elektrode, 2) Neuprogrammierung des Systems auf eine bipolare Version der Wahrnehmung, 3) Austausch der Elektrode durch eine neue mit bipolarem Kern.
Bekanntlich ist die Delta-Welle ein spezifisches Zeichen einer ventrikulären Vorerregung, da ein zusätzlicher antegrader Leitungsweg ohne die für den AV-Knoten charakteristische Impulsverzögerung vorhanden ist. Das bekannte EKG-Bild in Form einer Deltawelle, die den QRS-Komplex erweitert und das P-Q-Intervall aufgrund der Präexitation verkürzt, wird als WPW-Phänomen bezeichnet. Manchmal besteht jedoch die „Versuchung“, eine Deltawelle dort zu erkennen, wo sie tatsächlich nicht existiert, sondern wo eine ventrikuläre Extrasystole vorliegt, deren Beginn der Vorerregung sehr ähnlich ist. Dies ist die sogenannte Pseudo-Delta-Welle. Ein solcher ventrikulärer Komplex imitiert eine kontinuierliche Deltawelle (Synonyme: kontinuierliche antidrome Überleitung, Extrasystole aus dem Kent-Bündel). Eine diagnostische Schwierigkeit entsteht, wenn in einem Standard-EKG eine ventrikuläre Extrasystole mit einer Pseudo-Delta-Welle aufgezeichnet wird. Bei der Analyse der Langzeit-EKG-Überwachung passt alles zusammen: das WPW-Phänomen mit Extrasystole aus dem Kent-Bündel (solide Delta-Welle) Stets wird mit dem Vorhandensein ventrikulärer Komplexe mit einer echten Deltawelle kombiniert. Im Gegensatz dazu werden bei der Registrierung einer ventrikulären Extrasystole mit einer Pseudo-Delta-Welle klassische Anzeichen des WPW-Phänomens (einschließlich intermittierender Präexitation) nicht erkannt. Beispiele:
Anhand der „Breite“ der Pseudo-Delta-Welle kann man die Lokalisierung des extrasystolischen Fokus beurteilen: endokardial oder epikardial. Der Algorithmus lautet wie folgt: 1) Wenn die Pseudo-Delta-Welle länger als 50 ms dauert, können wir über den epikardialen Ursprung der PVC sprechen. 2) Wenn die Pseudo-Delta-Welle weniger als 50 ms dauert, dann achten Sie darauf zum kürzesten RS-Intervall in der Extrasystole im 12-Kanal-EKG: Seine Dauer von weniger als 115 ms weist auf eine endokardiale Lokalisierung des Fokus hin, während bei einer Dauer von 115 ms oder mehr mit dem dritten Schritt fortgefahren wird: dem Vorhandensein von a q-Welle in Ableitungs-aVL, 3) Das Vorhandensein einer q-Welle in Ableitungs-aVL weist auf den epikardialen Ursprung der PVC hin, ihr Fehlen - etwa endokardial. Im folgenden EKG beispielsweise übersteigt die Breite der Pseudo-Delta-Welle selbst nach den gröbsten Berechnungen 50 ms:
Die Lokalisation des extrasystolischen Herdes ist nicht nur für invasive Arrhythmologen von Interesse: Bei häufigen epikardialen Extrasystolen ist das Risiko einer arrhythmogenen Dilatation des Herzens deutlich höher.
. Bei einer hohen Herzfrequenz werden myokardiale Energieressourcen mobilisiert. Wenn eine Tachysystole-Episode zu lange anhält oder die Herzfrequenz extrem hoch ist, ist der intrazelluläre Stoffwechsel gestört (kann die Belastung nicht bewältigen) – es entsteht eine vorübergehende Myokarddystrophie. In einem solchen Fall können nach Ende der Tachykardie im EKG unspezifische Veränderungen der Repolarisation, ein sogenanntes Posttachykardie-Syndrom, festgestellt werden. Theoretisch können nach jeder Tachykardie (Sinus, supraventrikulär oder ventrikulär) in der Erholungsphase Manifestationen eines Posttachykardie-Syndroms auftreten. In seiner klassischen Form stellt es eine vorübergehende Umkehr der TV-Welle in den präkordialen Ableitungen dar. Die praktische Erfahrung zeigt jedoch, dass EKG-Veränderungen nach einer Tachykardie auch das S-T-Segment betreffen können. Daher sind in der klinischen Praxis folgende Erscheinungsformen des Posttachykardie-Syndroms anzutreffen:
Schräg aufsteigende Senkung des S-T-Segments mit Aufwärtskonvexität (wie „systolische Überlastung“),
- „langsame“ schräg aufsteigende Senkung des S-T-Segments,
Negative T-Welle.
Die Dauer des Posttachykardie-Syndroms ist unvorhersehbar variabel: von mehreren Minuten bis zu mehreren Tagen. Bei anhaltender Sympathikotonie können Manifestationen eines Posttachykardie-Syndroms über Monate und Jahre bestehen. Ein klassisches Beispiel ist der juvenile EKG-Typ (negative T-Wellen in den Ableitungen V1-V3), der für Jugendliche und junge Menschen mit labiler Psyche charakteristisch ist.
Betrachten wir kurz die Möglichkeiten des Posttachykardie-Syndroms.
Eine schräge Depression des S-T-Segments mit einer Konvexität nach oben nach einer Tachykardie bildet sich in der Regel bei Personen mit anfänglichen Manifestationen einer linksventrikulären Myokardhypertrophie; Bei solchen Patienten weist das Standard-Ruhe-EKG völlig normale Parameter auf. Die stärkste Depression wird in den Ableitungen V5, V6 beobachtet. Sein Aussehen ist jedem bekannt:

In der Regel normalisiert sich das EKG innerhalb von spätestens einer Stunde nach einer Tachykardie-Episode. Wenn die Myokardhypertrophie fortschreitet, verzögert sich die Normalisierung des S-T-Segments um Stunden oder sogar Tage, und anschließend werden die Manifestationen einer systolischen Überlastung in Ruhe „behoben“.
Eine „langsame“ schräg aufsteigende Senkung des S-T-Segments ist selten. Am häufigsten tritt es nach einer Tachykardie vor dem Hintergrund funktioneller Myokardstörungen vom Typ NCD auf.

Eine negative T-Welle ist die häufigste Variante des Posttachykardie-Syndroms. Es ist äußerst unspezifisch. Ich werde drei Beispiele nennen.
Negative T-Wellen in den präkordialen Ableitungen bei einem 21-jährigen Jungen (kann als juveniler EKG-Typ angesehen werden) vor dem Hintergrund einer anhaltenden Sympathikotonie:

Negative T-Wellen in den präkordialen Ableitungen entstehen nach ventrikulärer Tachykardie:
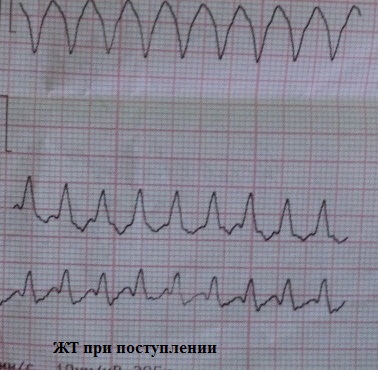
Negative T-Wellen in den präkordialen Ableitungen entstehen nach supraventrikulärer Tachykardie:
Klinische Bedeutung Posttachykardie Das Syndrom ist großartig! Es ist eine häufige Ursache für unnötige Krankenhausaufenthalte und medizinische Untersuchungen. Durch Simulation ischämischer Veränderungen, insbesondere in Kombination mit kardiales Syndrom, Posttachykardie-Syndrom kann eine Koronarpathologie „nachahmen“. Erinnere ihn! Viel Glück bei Ihrer Diagnose!
Bei etwa 2/3 der Menschen verzweigt sich der linke Schenkel nicht in zwei, sondern in drei: vordere, hintere und hintere Median. Entlang des Medianasts erstreckt sich die elektrische Erregung bis zum vorderen Teil des IVS und einem Teil der Vorderwand des linken Ventrikels.
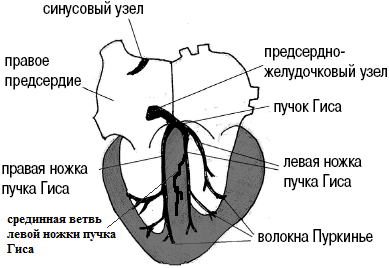
Seine isolierte Blockade kommt äußerst selten vor. Wenn dies jedoch geschieht, werden ein Teil des IVS und die vordere Wand des linken Ventrikels abnormal erregt – von der hinteren und seitlichen Wand des linken Ventrikels. Dadurch wird in der horizontalen Ebene der gesamte elektrische Vektor nach vorne gerichtet und in den Ableitungen V1-V3 wird die Bildung hoher R-Wellen (Komplexe wie qR, R oder Rs) beobachtet. Dieser Zustand muss unterschieden werden von:
WPW-Syndrom
Rechtsventrikuläre Hypertrophie
Posterobasaler Myokardinfarkt,
Normales EKG von Kindern in den ersten Lebensjahren, wenn aus natürlichen Gründen die Potenziale des rechten Ventrikels überwiegen.
Eine Blockade des mittleren Astes des linken Schenkels kann sowohl im Rahmen einer funktionellen Erregungsleitungsstörung auftreten als auch indirekt beispielsweise atherosklerotische Läsionen der vorderen absteigenden Arterie widerspiegeln, die ein subklinischer EKG-Marker einer koronaren Herzkrankheit sind.
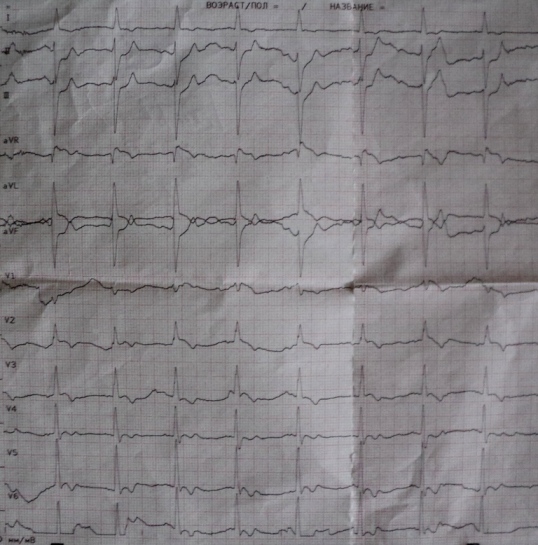

Der Autor dieser Zeilen ist im Laufe seiner beruflichen Laufbahn im wahrsten Sinne des Wortes mehrmals mit dieser Erregungsleitungsstörung in Berührung gekommen. Ich werde eine solche Beobachtung machen. Bei einem Patienten mit starken Brustschmerzen wurde das folgende EKG-Muster verifiziert (Abb. A): schräge Anhebung des S-T-Segments in den Ableitungen aVL, V2 und V3; vorderer oberer Halbblock und Blockade des mittleren Zweigs des linken Schenkels (R-Wellen mit hoher Amplitude in den Ableitungen V2, V3). Außerhalb des Anfalls normalisierte sich das EKG wieder (Abb. B).
Die Koronarangiographie ergab einen Spasmus der vorderen absteigenden Arterie im mittleren Drittel des Patienten, der sich durch intrakoronare Gabe von Nitraten auflöste; Eine konzentrische koronare Atherosklerose fehlte. Es wurde eine vasospastische Angina pectoris diagnostiziert. Somit trat die Blockade des Medianasts nur zum Zeitpunkt eines Angina pectoris-Anfalls auf, was auf eine „tiefe“ Myokardischämie zurückzuführen ist.
Wie bekannt, Herzschrittmacher-Syndrom kann durch eine chronisch bestehende Verletzung des normalen Kontraktionsablaufs der Vorhöfe und Ventrikel ausgelöst werden, beispielsweise aufgrund einer ventrikuloatrialen Überleitung oder einer zu langen AV-Verzögerung; oder seine Manifestation ist damit verbunden hämodynamische Nichtäquivalenz von natürlichen (eigenen) und erzwungenen Herzkontraktionen.
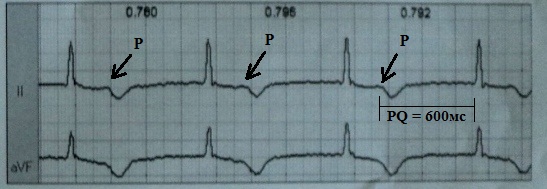
Das Pseudo-Schrittmachersyndrom ist eine hämodynamische Störung, die durch das Vorliegen einer ventrikuloatrialen Überleitung oder eines schweren AV-Blocks 1. Grades mit ähnlichen klinischen Manifestationen wie beim Schrittmachersyndrom, jedoch ohne Herzstimulation, verursacht wird. Die Entwicklung dieses „Pseudo-Syndroms“ wird am häufigsten bei einem langfristigen AV-Block 1. Grades von mehr als 350–400 ms beobachtet, wenn elektrokardiographisch die P-Welle beginnt, das S-T-Intervall des vorhergehenden ventrikulären Komplexes zu überlappen; In diesem Fall erfolgt die Vorhofsystole vor dem Hintergrund einer geschlossenen Mitralklappe.
Ich werde eine literarische Beobachtung machen. Der Patient wurde 4 Jahre nach der Herzschrittmacherimplantation im DDDR-Modus mit einer Basisstimulationsfrequenz von 50 pro Minute mit Symptomen einer dekompensierten CHF in die Klinik eingeliefert. Das EKG zeigte einen Sinusrhythmus mit AV-Block 1. Grades. Dauer ca. 600 ms:
Der Gesamtprozentsatz der atrialen Stimulation überstieg nicht 5 %, der ventrikuläre 7 %. In der Dynamik wurde festgestellt, dass seltene Episoden des aufgezwungenen Rhythmus oder der P-synchronen Stimulation der Ventrikel durch eine ventrikuläre Extrasystole unterbrochen wurden, auf die wiederum ein Sinusrhythmus mit ausgeprägtem AV-Block 1. Grades folgte:
Der Betriebsalgorithmus dieses Herzschrittmachers war so, dass nach jeder ventrikulären Kontraktion eine atriale Refraktärzeit von 450 ms ausgelöst wurde und die P-Welle etwa 200 ms nach dem ventrikulären Komplex auftrat – also sehr früh und daher nicht erkannt wurde. Dies führte zu einer nahezu vollständigen Hemmung der ventrikulären Stimulation. In diesem Fall war es notwendig, entweder die atriale Refraktärzeit zu verkürzen oder die Entwicklung eines vollständigen AV-Blocks zu provozieren. Diesem Patienten wurden zusätzlich zur Grundbehandlung der Herzinsuffizienz hohe Dosen Verapamil verschrieben, was durch die Blockierung der AV-Überleitung dazu führte, dass die ventrikulären Kontraktionen zu 100 % forciert wurden (P-synchrone Stimulation). Als entscheidender Faktor erwies sich die medikamentöse AV-Blockade – sie ermöglichte die Beseitigung der Desynchronisation bei der Kontraktion der Vorhöfe und Ventrikel, wodurch die Symptome einer Herzinsuffizienz gestoppt wurden.
In diesem Beispiel sehen wir, wie langfristig ein schwerer AV-Block 1. Grades verläuft. kann zur Entwicklung einer Herzinsuffizienz führen.
Manchmal kann man beim Pseudo-Schrittmacher-Syndrom das Phänomen einer „springenden“ P-Welle beobachten ( P-übersprungen), wenn sich die P-Welle vor dem Hintergrund einer deutlichen Verlangsamung der AV-Überleitung nicht einfach im QRS-Komplex „auflöst“, sondern diesem vorausgeht.
- Änderung der Länge des P-P-Intervalls unter dem Einfluss der ventrikulären Kontraktion bei fehlender ventrikuloatrialer Überleitung. Traditionell wird angenommen, dass diese Arrhythmie auftritt, wenn die Anzahl der Sinuswellen P die Anzahl der ventrikulären QRS-Komplexe übersteigt – also bei einem AV-Block 2. oder 3. Grades. In diesem Fall wird das P-P-Intervall, das den QRS-Komplex enthält, kürzer als das P-P-Intervall ohne ventrikuläre Kontraktion:

Gleichzeitig, Bei ventrikulärer Extrasystole und künstlicher ventrikulärer Stimulation kann eine ventrikulophasische Sinusarrhythmie beobachtet werden. Zum Beispiel:
Der wahrscheinlichste Mechanismus für dieses Phänomen: Dehnung der Vorhöfe während der ventrikulären Systole, wodurch mechanische Stimulation des Sinusknotens.
In den letzten Jahren hat sich die klinische und elektrokardiographische Herangehensweise an das frühe ventrikuläre Repolarisationssyndrom erheblich verändert. Nach Meinung der Experten kann dieses Syndrom ohne klinische Manifestationen (Anfälle einer polymorphen ventrikulären Tachykardie oder Kammerflimmern) korrekt bezeichnet werden Muster der frühen ventrikulären Repolarisation, Dies unterstreicht seine derzeitige Gutartigkeit im Rahmen einer harmlosen EKG-Anomalie. Begriff Syndrom Es wird empfohlen, RRG zu verwenden nur bei symptomatischen Patienten, die an einer Synkope oder einem plötzlichen Herztod aufgrund eines ventrikulären Tachyarrhythmiemechanismus leiden. Angesichts der außergewöhnlichen Seltenheit dieses Verlaufs des RGC-Phänomens (~ 1 pro 10.000 Menschen) ist die Verwendung des Begriffs sinnvoll Muster sollte nicht nur als Priorität betrachtet werden, sondern als die einzig richtige.
Die Kriterien zur Diagnose des RGC-Musters sind strenger geworden. Es ist ein Fehler zu glauben, dass die konkave Erhebung des S-T-Segments einer der Marker für RGC ist.Zu analysieren nur Verformung des absteigenden Teils der R-Zacke: Das RJ-Muster bezieht sich auf das Vorhandensein einer Kerbe (Welle j) darauf oder auf seine Glätte. Der Abstand von der Isolinie (der Meldepunkt ist die Position des P-Q-Intervalls) bis zur Spitze der Kerbe oder dem Beginn der Glätte muss in zwei oder mehr aufeinanderfolgenden Ableitungen eines Standard-EKGs (ausgenommen Ableitungen aVR, V1) mindestens 1 mm betragen -V3); Die Breite des QRS-Komplexes sollte weniger als 120 ms betragen und die QRS-Dauer wird nur in Ableitungen berechnet, in denen kein RR-Muster vorhanden ist.


Nach den oben beschriebenen Kriterien weist nur EKG Nr. 1 ein RGC-Muster auf:
Leider gibt es noch keine verlässlichen Kriterien für die potenzielle Bösartigkeit des RGC-Musters und die Möglichkeit seines Übergangs in ein Syndrom. Wenn jedoch die folgenden klinischen Anzeichen vorliegen, sollte sich eine Person mit dem RGC-Muster in ärztliche Behandlung begeben:
Dynamische Änderung der J-Punkt-Höhe ohne Änderung der Herzfrequenz,
Das Vorhandensein ventrikulärer Extrasystolen vom Typ „R nach T“,
Das Vorliegen einer Synkope, die sich im klinischen Verlauf vermutlich von der vasovagalen Synkope unterscheidet (d. h. „plötzlich lag ich auf dem Boden“-Synkope),
Unerklärlicher Tod eines Verwandten ersten Grades unter 45 Jahren mit einem dokumentierten RGC-Muster,
Das Vorhandensein eines RGC-Musters in den meisten Ableitungen (aVR, V1-V3 – nicht berücksichtigt),
Übergang der Welle j in ein horizontales oder abwärts gerichtetes S-T-Segment.
Um die Art des S-T-Segments (aufsteigend, horizontal oder absteigend) zu bestimmen, wird die Position des Punktes Jt und eines Punktes auf dem S-T-Segment, der 100 ms davon entfernt ist, verglichen:
Der Nachweis eines AV-Blocks 2. Grades vom Typ Mobitz II ist fast immer ein ungünstiges prognostisches Zeichen, da sein Vorliegen zum einen eine Erregungsleitungsstörung distal des AV-Knotens widerspiegelt und zum anderen oft als Vorbote für die Entwicklung schwerwiegenderer Erkrankungen dient dromotrope Insuffizienz, zum Beispiel vollständiger AV-Block. Blockaden
Gleichzeitig kommt es in der praktischen Kardiologie zu einer deutlichen Überdiagnose des AV-Blocks 2. Grades. Typ Mobitz II. Betrachten wir Situationen, die einen solchen Block vortäuschen können – den sogenannten Pseudo-Mobitz II (falscher AV-Block zweiten Grades, Typ II):
Lange AV-Knoten-Periodizitäten mit AV-Block 2. Grades Typ I;

Plötzlicher vorübergehender Anstieg des Vagustonus;
Versteckt ;

Nach ventrikulärer Extrasystole;

Syndrom W.P.W.;

Potentialunterschied zwischen benachbarten Bereichen des Myokardsynzytiums während der Repolarisationsphase des Herzzyklus. Im gesunden Myokard ist die Streuung der Refraktärität minimal und ihre klinische Bedeutung geht gegen Null. Wenn wir über das Vorhandensein einer Streuung der myokardialen Refraktärität bei einem Patienten sprechen, sagen wir: a priori wir gehen von einem hohen Risiko für die Entwicklung einer profibrillatorischen Arrhythmie aus.
Die Entwicklung einer klinisch signifikanten Varianz der Refraktärität ist in zwei Fällen möglich: 1) beim Vorliegen einer organischen Herzerkrankung mit schwerer systolischer Dysfunktion; 2) Störungen des Ionentransports (Kanalopathien, Elektrolytungleichgewicht). In beiden Fällen ist die Verteilung der elektrischen Erregung in allen Phasen des Herzzyklus nicht homogen, was bedeutet, dass im Moment der Repolarisation (relative Refraktärität) Bedingungen für das Auftreten eines vorzeitigen Aktionspotentials entstehen – was elektrokardiographisch äquivalent ist eine extrasystolische Kontraktion. Die extrasystolische Erregungsfront wird gleich asynchron sein, daher besteht während der Repolarisation eine hohe Wahrscheinlichkeit des Auftretens einer weiteren Extrasystole usw., bis die nächste elektrische Welle in mehrere Wellen zerfällt und sich eine fibrillierende Aktivität in den Vorhöfen entwickelt oder Ventrikel.
Beispiel 1. Während eines akuten Myokardinfarkts löste eine andere PVC eine polymorphe VT aus, die sich in eine VF verwandelte:
Beispiel 2. Ein Patient mit schwerer Hypokaliämie (1,7 mmol/l). „Riesiges“ Q-T-Intervall (~750 ms). Vor diesem Hintergrund treten häufig polytope ektopische Kontraktionen auf. Hohes Risiko, Kammerflimmern zu entwickeln:

Obwohl die Streuung der Refraktärität ein elektrophysiologisches Konzept ist, wird sie von Ärzten häufiger in einem beschreibenden Sinne als Marker für ein erhöhtes Risiko lebensbedrohlicher ventrikulärer Tachyarrhythmien verwendet, das anhand des Vorhandenseins instrumenteller Anzeichen einer linksventrikulären systolischen Dysfunktion verifiziert wird. Mit Ausnahme einiger Störungen des Ionentransports hat die Streuung der Refraktärität keine direkten EKG-Manifestationen.
1. Kurzes Intervall „PQ“ (< 0,12 с):
CLC-Syndrom:
2. Langes Intervall „PQ“ (>0,2 s):
· AV-Block 1. Grades;

· AV-Block 2. Grades, Typ 2 mit ständig erhöhtem PQ-Intervall (siehe Abschnitt „Bradykardie“).

3. „P“ ist unmittelbar nach dem QRS-Komplex negativ:
· Rhythmus der AV-Verbindung mit vorheriger Erregung der Ventrikel (siehe Abschnitt „Bradykardie“).

Es besteht kein Zusammenhang zwischen der P-Welle und dem QRS
· AV-Block 3. Grades oder vollständiger AV-Block (mit PP-Intervallen). · AV-Dissoziation (mit Intervallen PP>RR) – siehe Abschnitt „Bradykardie“. IV. „R“-Welle Eine Änderung der Dynamik der Amplitude der „R“-Welle in der Brust führt zu: A) „R“-Wellen mit hoher Amplitude in V5–6 und tiefe „S“-Wellen in V1–2 + Abweichung der elektrischen Achse des Herzens nach links (RI>RII>RIII und SIII>SI); R in V5(V6) > 25 mm; S in V1 + R in V5(V6) > 35 mm; R in avL > 11 mm: · B) Hohe oder gespaltene R-Welle in V1, V2 und tiefe, aber nicht breite (weniger als 0,04 Sek.) S-Welle in V5–6 + Abweichung der elektrischen Achse des Herzens nach rechts (RIII>RII>RI und SI>). SIII) R in V1 > 7 mm; S in V5(V6) > 7 mm: · Hypertrophie des rechtsventrikulären Myokards. V. Q-Welle A) Die Breite der Welle beträgt weniger als 0,03 s und/oder die Amplitude beträgt weniger als ¼ der R-Welle dieser Ableitung – normal„Q“-Welle; B) Die Breite der Welle beträgt mehr als 0,03 s und/oder die Amplitude beträgt mehr als ¼ der R-Welle dieser Ableitung – pathologisch Q-Welle: Akuter makrofokaler Myokardinfarkt; narbige Veränderungen im Myokard. Die Diagnose wird auf der Grundlage einer Beurteilung der Dynamik der Veränderungen im QRS-Komplex, im ST-Segment und in der T-Welle gestellt: VI. QRS-Komplex Breite des QRS-Komplexes A. Schmaler Komplex (QRS<0,12 с):
Supraventrikulärer (supraventrikulärer) Rhythmus (ohne Störung der Impulsübertragung entlang der Äste des His-Bündels – intraventrikuläre Blockaden): – Sinusrhythmus (Sinus-„P“-Wellen werden vor den „QRS“-Komplexen aufgezeichnet); – Vorhofrhythmus (vor den QRS-Komplexen werden „P“-Wellen nicht sinusförmigen Ursprungs aufgezeichnet); – AV-Verbindungsrhythmus: · mit vorheriger Erregung der Ventrikel: Der „QRS“-Komplex wird aufgezeichnet, unmittelbar danach oder auf dem die negative „P“-Welle aufgezeichnet wird; · bei gleichzeitiger Erregung der Ventrikel und Vorhöfe: Der „QRS“-Komplex wird aufgezeichnet, die „P“-Welle wird nicht aufgezeichnet. B. Breiter Komplex (QRS >0,12 s): 1. Supraventrikulärer (supraventrikulärer) Rhythmus mit Blockade der His-Schenkeläste.
Eine „P“-Welle beliebigen Ursprungs (jeder Polarität, Konfiguration) wird vor dem ventrikulären Komplex oder negativ auf oder unmittelbar nach einem breiten „QRS“-Komplex aufgezeichnet, der gemäß einem der folgenden Typen deformiert ist: A) In den Ableitungen V5, V6 (I, aVL) ist die R-Welle breit mit abgerundeter Spitze, in V1, V2 (III, aVF) ist die S-Welle tief + Abweichung der elektrischen Achse nach links (RI>RII>RIII und SIII>SI): · voll – mit einer Breite des „QRS“-Komplexes > 0,12 s; · unvollständig – mit der Breite des „QRS“-Komplexes< 0,12 с. B)„M“-förmige Aufspaltung des QRS-Komplexes in den Ableitungen V1, V2 (III, aVF); breit (mehr als 0,04 Sek.), aber flach (< 7 мм) зубец S в отведениях V5, V6 (I, аVL) + отклонение электрической оси вправо (RIII>RII>RI und SI>SIII): * voll – mit QRS-Komplexbreite > 0,12 s; * unvollständig – mit der Breite des QRS-Komplexes< 0,12 с. 2.Idioventrikulärer (ventrikulärer) Rhythmus.
Es gibt keine „P“-Wellen, es werden breite und deformierte „QRS“-Komplexe aufgezeichnet, ähnlich einem vollständigen Block des Schenkelzweigs, gefolgt von einer bradykarden Frequenz von 30 Schlägen/Minute oder weniger. Linksventrikulärer Rhythmus(EKG-Anzeichen von BE P NPG) :
Rechtsventrikulärer Rhythmus(EKG-Anzeichen von BE L NPG) :
3. Wolff-Parkinson-White-Syndrom oder -Phänomen (WPW- oder VPU-Syndrom oder -Phänomen).
· · Deltawelle („Ballerina-Bein“, „Schritt“); · Breit deformierter QRS-Komplex mit diskordanter Verschiebung von ST-Strecke und T-Welle. Die Erregung entlang des zusätzlichen Kent-Bündels wird schneller zu den Ventrikeln geleitet als über den AV-Knoten, wodurch eine zusätzliche Depolarisationswelle der basalen Teile der Ventrikel entsteht – eine Deltawelle. Dadurch wird das P-Q(R)-Intervall verkürzt und die Dauer des QRS-Komplexes verlängert, er wird deformiert Wenn nur EKG-Zeichen erfasst werden, spricht man vom WPW-Phänomen; gehen EKG-Veränderungen mit paroxysmalen Herzrhythmusstörungen einher, spricht man vom WPW-Syndrom. VI. ST-Segment 1. Verschiebung der ST-Strecke über die Isolinie
– akutes Stadium eines Myokardinfarkts
: in mehreren Ableitungen - Anhebung des ST-Segments mit einer Konvexität nach oben mit Übergang zur T-Welle. In reziproken Ableitungen - Senkung des ST-Segments. Die Q-Welle wird häufig aufgezeichnet. Die Veränderungen sind dynamisch; Die T-Welle wird negativ, bevor die ST-Strecke zur Grundlinie zurückkehrt. – akute Perikarditis, Myokarditis
: ST-Segment-Hebung in vielen Ableitungen (I–III, aVF, V 3–V 6), Fehlen einer ST-Senkung in reziproken Ableitungen (außer aVR), Fehlen einer Q-Welle, PQ-Segment-Senkung. Veränderungen sind dynamisch; Die T-Welle wird negativ, nachdem die ST-Strecke zur Grundlinie zurückgekehrt ist. – PVR (vorzeitiges ventrikuläres Repolarisationssyndrom):
Anhebung des ST-Segments mit konvexem Übergang nach unten zu einer konkordanten T-Welle. Kerbe am absteigenden Knie der R-Welle. Breite symmetrische T-Welle. Veränderungen im ST-Segment und in der T-Welle sind dauerhaft. Ist eine Variante der Norm. – Vagotonie
. 2. Verschiebung der ST-Strecke unterhalb der Isolinie:
– IHD
: · subendokardialer Myokardinfarkt oder als Reziprozität (Abwärtsverschiebung des ST-Segments in Ableitungen, die der Wand gegenüber der Wand entspricht, in der der Bereich des großfokalen oder transmuralen Myokardinfarkts lokalisiert ist); · während eines Angina pectoris-Anfalls; – systolische Überlastung bei ventrikulärer Hypertrophie
: Schräge Senkung des ST-Segments mit konvexem Übergang nach oben zu einer negativen T-Welle. – Sättigung mit Herzglykosiden
oder Glykosidvergiftung :
muldenförmige Vertiefung der ST-Strecke. Biphasische oder negative T-Welle. Veränderungen sind in den linken präkordialen Ableitungen stärker ausgeprägt. – Hypokaliämie
: Verlängerung des PQ-Intervalls, Verbreiterung des QRS-Komplexes (selten), ausgeprägte U-Welle, abgeflachte invertierte T-Welle, ST-Strecken-Senkung, leichte Verlängerung des QT-Intervalls. Varianten der ST-Strecken-Depression VI. „T“-Welle 1. Positive, spitze „T“-Welle mit hoher Amplitude in V1–V3: – – Vagotonie; – Hyperkaliämie; – adrenerge Einflüsse; – alkoholische Myokarddystrophie; – diastolische Überlastung mit ventrikulärer Hypertrophie. 2. Negative „T“-Welle in V1–V3 (V4): A) Bei gesunden Personen: – Kinder- und „Jugend“-EKG; – mit Hyperventilation; – nach dem Verzehr von kohlenhydrathaltigen Lebensmitteln. B) Hauptursachen: – Manifestation einer ischämischen Herzkrankheit: – Peri- und Myokarditis; – mit Mitralklappenprolaps; – mit arrhythmogener Dysplasie des rechten Ventrikels und HCM, alkoholischer Herzkrankheit; – bei akutem und chronischem Cor pulmonale; – mit dyshormoneller Myokarddystrophie. B) Sekundäre Ursachen: – systolische Überlastung bei ventrikulärer Hypertrophie; – eine Komponente des WPW-Syndroms oder Schenkelblocks; – zerebrovaskuläre Unfälle; – Posttachykardie-Syndrom und Chaterrier-Syndrom (Post-Kardiostimulationssyndrom); – Magen-Darm-Erkrankungen (Pankreatitis); – Vergiftung (CO, Organophosphorverbindungen); – Pneumothorax; – Sättigung mit Herzglykosiden. VII. QT-Intervall Verlängerung des QT-Intervalls. QTc > 0,46 für Männer und > 0,47 für Frauen; (QTc = QT/ÖRR). a.Angeborene Verlängerung des QT-Intervalls: Romano-Ward-Syndrom (ohne Hörbehinderung), Ervel-Lange-Nielsen-Syndrom (mit Taubheit). B. Erworbene QT-Verlängerung: Einnahme bestimmter Medikamente (Chinidin, Procainamid, Disopyramid, Amiodaron, Sotalol, Phenothiazine, trizyklische Antidepressiva, Lithium), Hypokaliämie, Hypomagnesiämie, schwere Bradyarrhythmie, Myokarditis, Mitralklappenprolaps, Myokardischämie, Hypothyreose, Unterkühlung, kalorienarme Flüssigproteindiäten. Verkürzung des QT-Intervalls. QT< 0,35 с при ЧСС 60-100 мин –1 . Наблюдается при гиперкальциемии, гликозидной интоксикации. Richtiges QT-Intervall und seine Abweichungen (%) abhängig von der Herzfrequenz NEUE NACHRICHT ERSTELLEN. Wenn Sie sich bereits registriert haben, „melden Sie sich an“ (Anmeldeformular oben rechts auf der Website). Wenn Sie zum ersten Mal hier sind, registrieren Sie sich bitte. Wenn Sie sich registrieren, können Sie die Reaktionen auf Ihre Nachrichten weiter verfolgen und den Dialog zu interessanten Themen mit anderen Benutzern und Beratern fortsetzen. Darüber hinaus können Sie durch die Registrierung private Korrespondenz mit Beratern und anderen Benutzern der Website führen. Registrieren Erstellen Sie eine Nachricht ohne Registrierung Schreiben Sie Ihre Meinung zu der Frage, den Antworten und anderen Meinungen: Dies ist der zweite Teil der Serie über EKG (im Volksmund - EKG des Herzens). Um das heutige Thema zu verstehen, müssen Sie Folgendes lesen: Reizleitungssystem des Herzens (erforderlich), Teil 1: Theoretische Grundlagen der Elektrokardiographie Das Elektrokardiogramm spiegelt wider nur elektrische Prozesse im Myokard: Depolarisation (Erregung) und Repolarisation (Wiederherstellung) von Myokardzellen. Verhältnis EKG-Intervalle Mit Phasen des Herzzyklus(ventrikuläre Systole und Diastole). Normalerweise führt die Depolarisation zur Kontraktion der Muskelzelle und die Repolarisation zur Entspannung. Zur weiteren Vereinfachung verwende ich anstelle von „Depolarisation-Repolarisation“ manchmal „Kontraktion-Relaxation“, obwohl dies nicht ganz korrekt ist: Es gibt ein Konzept „ Elektromechanische Dissoziation„, bei dem Depolarisation und Repolarisation des Myokards nicht zu seiner sichtbaren Kontraktion und Entspannung führen. Ich habe zuvor etwas mehr über dieses Phänomen geschrieben. Bevor Sie mit der Entschlüsselung des EKG fortfahren, müssen Sie verstehen, aus welchen Elementen es besteht. Wellen und Intervalle im EKG. Jedes EKG besteht aus Zähne, Segmente Und Intervalle. ZÄHNE- Dies sind Konvexitäten und Konkavitäten im Elektrokardiogramm. (Kontraktion der Vorhöfe), (alle 3 Wellen charakterisieren die Kontraktion der Ventrikel), (Entspannung der Ventrikel), (nicht konstante Welle, selten aufgezeichnet). SEGMENTE INTERVALLE Wellen, Segmente und Intervalle im EKG. Da das ventrikuläre Myokard massiver ist als das Vorhofmyokard und nicht nur Wände, sondern auch ein massives interventrikuläres Septum aufweist, ist die Erregungsausbreitung darin durch das Auftreten eines komplexen Komplexes gekennzeichnet QRS auf dem EKG. Wie richtig Markieren Sie die Zähne darin? Zunächst bewerten sie Amplitude (Größen) einzelner Zähne QRS-Komplex. Wenn die Amplitude überschreitet 5 mm, zeigt der Zahn an Großbuchstabe Q, R oder S; wenn die Amplitude weniger als 5 mm beträgt, dann Kleinbuchstaben (klein): q, r oder s. Die R-Zacke (r) heißt irgendetwas Positives(Aufwärts-)Welle, die Teil des QRS-Komplexes ist. Wenn mehrere Zähne vorhanden sind, weisen die Folgezähne darauf hin Schlaganfälle: R, R‘, R“ usw. Negative (Abwärts-)Welle des QRS-Komplexes, lokalisiert vor der R-Welle, wird als Q(q) bezeichnet und danach - wie S(S). Wenn im QRS-Komplex überhaupt keine positiven Wellen vorhanden sind, wird der ventrikuläre Komplex als bezeichnet QS. Varianten des QRS-Komplexes. Normalerweise spiegelt der Zahn die Depolarisation des interventrikulären Septums wider, der Zahn spiegelt den Großteil des ventrikulären Myokards wider und der Zahn spiegelt die basalen (d. h. in der Nähe der Vorhöfe) Abschnitte des interventrikulären Septums wider. Die Welle RV1, V2 spiegelt die Erregung des interventrikulären Septums wider und RV4, V5, V6 – die Erregung der Muskeln des linken und rechten Ventrikels. Die Nekrose von Bereichen des Myokards (z. B. bei einem Myokardinfarkt) führt zu einer Verbreiterung und Vertiefung der Q-Welle, weshalb dieser Welle immer große Aufmerksamkeit geschenkt wird. Allgemein EKG-Dekodierungsdiagramm Überprüfung der Richtigkeit der EKG-Registrierung. Herzfrequenz- und Leitfähigkeitsanalyse: Beurteilung der Regelmäßigkeit der Herzkontraktionen, Zählen der Herzfrequenz (HF), Bestimmung der Erregungsquelle, Beurteilung der Leitfähigkeit. Bestimmung der elektrischen Achse des Herzens. Analyse der atrialen P-Welle und des P-Q-Intervalls. Analyse des ventrikulären QRST-Komplexes: QRS-Komplexanalyse, RS-T-Segmentanalyse, T-Wellen-Analyse, Q-T-Intervallanalyse. Elektrokardiographischer Bericht. Normales Elektrokardiogramm. 1) Überprüfung der korrekten EKG-Registrierung Am Anfang jedes EKG-Bandes muss es stehen Kalibrierungssignal- sogenannt Referenz-Millivolt. Dazu wird zu Beginn der Aufnahme eine Standardspannung von 1 Millivolt angelegt, die eine Abweichung von aufweisen sollte 10 mm. Ohne Kalibriersignal gilt die EKG-Aufzeichnung als fehlerhaft. Normalerweise sollte die Amplitude in mindestens einer der Standard- oder erweiterten Extremitätenableitungen größer sein 5 mm, und in der Brust führt - 8 mm. Ist die Amplitude geringer, spricht man von einem Aufruf reduzierte EKG-Spannung, was bei einigen pathologischen Zuständen auftritt. Referenz-Millivolt im EKG (zu Beginn der Aufzeichnung). 2) Herzfrequenz- und Reizleitungsanalyse: Beurteilung der Regelmäßigkeit der Herzfrequenz Die Regelmäßigkeit des Rhythmus wird beurteilt durch R-R-Intervalle. Wenn die Zähne den gleichen Abstand voneinander haben, spricht man von einem regelmäßigen oder korrekten Rhythmus. Die Variation der Dauer einzelner R-R-Intervalle ist nicht mehr als zulässig ± 10 % von ihrer durchschnittlichen Dauer. Wenn der Rhythmus sinusförmig ist, ist er normalerweise regelmäßig. Herzfrequenzmessung(Pulsschlag) Auf dem EKG-Film sind große Quadrate aufgedruckt, von denen jedes 25 kleine Quadrate (5 vertikal x 5 horizontal) enthält. Um die Herzfrequenz schnell im richtigen Rhythmus zu berechnen, zählen Sie die Anzahl der großen Quadrate zwischen zwei benachbarten Zähnen R - R. Bei einer Bandgeschwindigkeit von 50 mm/s: HR = 600 (Anzahl der großen Quadrate). Im darüber liegenden EKG beträgt das R-R-Intervall etwa 4,8 große Zellen, was bei einer Geschwindigkeit von 25 mm/s ergibt 300 / 4,8 = 62,5 Schläge/Minute. Mit einer Geschwindigkeit von jeweils 25 mm/s kleine Zelle gleich 0,04 s und bei einer Geschwindigkeit von 50 mm/s - 0,02 s. Daraus werden die Dauer der Zähne und die Intervalle ermittelt. Wenn der Rhythmus nicht stimmt, wird dies normalerweise berücksichtigt maximale und minimale Herzfrequenz entsprechend der Dauer des kleinsten bzw. größten R-R-Intervalls. Bestimmung der Anregungsquelle Mit anderen Worten: Sie suchen nach dem Wo Schrittmacher, was zu Kontraktionen der Vorhöfe und Ventrikel führt. Manchmal ist dies eines der schwierigsten Stadien, da verschiedene Erregungs- und Erregungsleitungsstörungen sehr verwirrend kombiniert werden können, was zu einer falschen Diagnose und falschen Behandlung führen kann. Um die Erregungsquelle im EKG richtig bestimmen zu können, sind gute Kenntnisse des Erregungsleitungssystems des Herzens erforderlich. Sinusrhythmus(Dies ist ein normaler Rhythmus und alle anderen Rhythmen sind pathologisch). In der Standardableitung II sind die P-Wellen immer positiv und liegen vor jedem QRS-Komplex, die P-Wellen in derselben Ableitung haben eine konstant identische Form. P-Welle im Sinusrhythmus. ATRIALER Rhythmus. Befindet sich die Erregungsquelle in den unteren Teilen der Vorhöfe, dann breitet sich die Erregungswelle von unten nach oben (retrograd) in die Vorhöfe aus, also: In den Ableitungen II und III sind die P-Wellen negativ, es gibt P-Wellen vor jedem QRS-Komplex. P-Welle während des Vorhofrhythmus. Rhythmen aus dem AV-Anschluss. Befindet sich der Herzschrittmacher im atrioventrikulären Bereich ( atrioventrikulärer Knoten) Knoten, dann werden die Ventrikel wie gewohnt erregt (von oben nach unten) und die Vorhöfe - retrograd (d. h. von unten nach oben). Gleichzeitig im EKG: P-Wellen können fehlen, weil sie normale QRS-Komplexe überlagern; P-Wellen können negativ sein und sich hinter dem QRS-Komplex befinden. Rhythmus vom AV-Übergang, Überlagerung der P-Welle mit dem QRS-Komplex. Rhythmus vom AV-Übergang, die P-Welle liegt hinter dem QRS-Komplex. Die Herzfrequenz mit einem Rhythmus vom AV-Knoten ist geringer als der Sinusrhythmus und beträgt etwa 40–60 Schläge pro Minute. Ventrikulärer oder idioventrikulärer Rhythmus(vom lateinischen ventriculus – Ventrikel). In diesem Fall ist die Rhythmusquelle das ventrikuläre Reizleitungssystem. Die Erregung breitet sich in den Ventrikeln falsch aus und ist daher langsamer. Merkmale des idioventrikulären Rhythmus: QRS-Komplexe sind verbreitert und deformiert (sie sehen „unheimlich“ aus). Normalerweise beträgt die Dauer des QRS-Komplexes 0,06–0,10 s, daher überschreitet der QRS bei diesem Rhythmus 0,12 s. Es gibt kein Muster zwischen QRS-Komplexen und P-Wellen, da der AV-Übergang keine Impulse von den Ventrikeln abgibt und die Vorhöfe wie gewohnt vom Sinusknoten aus erregt werden können. Herzfrequenz weniger als 40 Schläge pro Minute. Idioventrikulärer Rhythmus. Die P-Welle ist nicht mit dem QRS-Komplex verbunden. Leitfähigkeitsbewertung. Um die Leitfähigkeit zu beurteilen, messen Sie: Dauer P-Welle(spiegelt die Geschwindigkeit der Impulsübertragung durch die Vorhöfe wider), normalerweise bis zu 0,1 s. Dauer Intervall P - Q(spiegelt die Geschwindigkeit der Impulsleitung von den Vorhöfen zum ventrikulären Myokard wider); Intervall P - Q = (Welle P) + (Segment P - Q). Bußgeld 0,12–0,2 s. Dauer QRS-Komplex(spiegelt die Ausbreitung der Erregung durch die Ventrikel wider). Bußgeld 0,06–0,1 s. internes Abweichungsintervall in den Ableitungen V1 und V6. Dies ist die Zeit zwischen dem Beginn des QRS-Komplexes und der R-Zacke. Normal in V1 bis zu 0,03 s und in V6 bis 0,05 s. Es dient vor allem zur Erkennung von Schenkelblockaden und zur Bestimmung der Erregungsquelle in den Herzkammern bei ventrikulärer Extrasystole (außergewöhnliche Kontraktion des Herzens). Messung des internen Abweichungsintervalls. 3) Bestimmung der elektrischen Achse des Herzens. 4) Vorhof-P-Wellen-Analyse. Normalerweise wird die Dauer der P-Welle nicht überschritten 0,1 s und seine Amplitude beträgt 1,5 - 2,5 mm. Pathologische Abweichungen der P-Welle: Charakteristisch sind spitze hohe P-Wellen normaler Dauer in den Ableitungen II, III, aVF Hypertrophie des rechten Vorhofs, zum Beispiel mit „Lungenherz“. Charakteristisch für die Spaltung mit 2 Scheitelpunkten ist die verbreiterte P-Welle in den Ableitungen I, aVL, V5, V6 Hypertrophie des linken Vorhofs, zum Beispiel bei Mitralklappendefekten. Entstehung der P-Welle (P-pulmonale) mit Hypertrophie des rechten Vorhofs. Entstehung der P-Welle (P-Mitral) mit Hypertrophie des linken Vorhofs. P-Q-Intervall: Bußgeld 0,12–0,20 s. AV-Block Es gibt 3 Grade: I-Grad – das P-Q-Intervall ist vergrößert, aber jede P-Welle hat ihren eigenen QRS-Komplex ( kein Komplexverlust). II. Grad - QRS-Komplexe teilweise herausfallen, d.h. Nicht alle P-Wellen haben einen eigenen QRS-Komplex. III. Grad - vollständige Blockade der Erregungsleitung im AV-Knoten. Die Vorhöfe und Ventrikel ziehen sich unabhängig voneinander in ihrem eigenen Rhythmus zusammen. Diese. Es kommt zum idioventrikulären Rhythmus. 5) Ventrikuläre QRST-Analyse: QRS-Komplexanalyse. Die maximale Dauer des ventrikulären Komplexes beträgt 0,07–0,09 s(bis zu 0,10 s). Die Dauer erhöht sich mit jedem Schenkelblock. Normalerweise kann die Q-Welle in allen Standard- und erweiterten Extremitätenableitungen sowie in V4–V6 aufgezeichnet werden. Die Amplitude der Q-Welle überschreitet normalerweise nicht 1/4 R-Wellenhöhe, und die Dauer ist 0,03 s. Bei Lead-AVR gibt es normalerweise eine tiefe und breite Q-Welle und sogar einen QS-Komplex. Die R-Welle kann wie die Q-Welle in allen Standard- und erweiterten Extremitätenableitungen aufgezeichnet werden. Von V1 bis V4 nimmt die Amplitude zu (während die rV1-Welle möglicherweise fehlt) und nimmt dann in V5 und V6 ab. Die S-Welle kann sehr unterschiedliche Amplituden haben, meist jedoch nicht mehr als 20 mm. Die S-Welle nimmt von V1 bis V4 ab und kann in V5–V6 sogar fehlen. In Ableitung V3 (oder zwischen V2 – V4)“ Übergangszone"(Gleichheit von R- und S-Wellen). RS-T-Segmentanalyse Das S-T-Segment (RS-T) ist ein Segment vom Ende des QRS-Komplexes bis zum Beginn der T-Welle. Das S-T-Segment wird bei koronarer Herzkrankheit besonders sorgfältig analysiert, da es den Sauerstoffmangel (Ischämie) widerspiegelt. im Myokard. Normalerweise liegt das S-T-Segment in den Extremitätenableitungen auf der Isolinie ( ± 0,5 mm). In den Ableitungen V1–V3 kann sich das S-T-Segment nach oben verschieben (nicht mehr als 2 mm) und in den Ableitungen V4–V6 nach unten (nicht mehr als 0,5 mm). Der Punkt, an dem der QRS-Komplex in das S-T-Segment übergeht, wird als Punkt bezeichnet (vom Wort Junction – Verbindung). Der Grad der Abweichung des Punktes j von der Isolinie wird beispielsweise zur Diagnose einer Myokardischämie verwendet. T-Wellen-Analyse. Die T-Welle spiegelt den Prozess der Repolarisation des ventrikulären Myokards wider. In den meisten Ableitungen, in denen ein hohes R gemessen wird, ist auch die T-Welle positiv. Normalerweise ist die T-Welle in I, II, aVF, V2-V6 immer positiv, mit TI > TIII und TV6 > TV1. Bei aVR ist die T-Welle immer negativ. Q-T-Intervallanalyse. Das Q-T-Intervall wird aufgerufen elektrische ventrikuläre Systole, weil zu diesem Zeitpunkt alle Teile der Herzkammern erregt sind. Manchmal gibt es nach der T-Welle eine kleine U-Welle, die aufgrund einer kurzfristig erhöhten Erregbarkeit des ventrikulären Myokards nach ihrer Repolarisation entsteht. 6) Elektrokardiographischer Bericht. Rhythmusquelle (Sinus oder nicht). Regelmäßigkeit des Rhythmus (richtig oder nicht). Normalerweise ist der Sinusrhythmus normal, obwohl Atemrhythmusstörungen möglich sind. Pulsschlag. Lage der elektrischen Achse des Herzens. Das Vorliegen von 4 Syndromen: Rhythmusstörung, Reizleitungsstörung, Hypertrophie und/oder Überlastung der Ventrikel und Vorhöfe, Myokardschädigung (Ischämie, Dystrophie, Nekrose, Narben) Beispiele für Schlussfolgerungen(nicht ganz vollständig, aber echt): Sinusrhythmus mit Herzfrequenz 65. Normale Lage der elektrischen Achse des Herzens. Es wurde keine Pathologie festgestellt. Sinustachykardie mit Herzfrequenz 100. Einzelne supraventrikuläre Extrasystole. Sinusrhythmus mit einer Herzfrequenz von 70 Schlägen/Minute. Unvollständige Blockade des rechten Schenkels. Mäßige Stoffwechselveränderungen im Myokard. Beispiele für EKG bei bestimmten Erkrankungen des Herz-Kreislauf-Systems – nächstes Mal. Aufgrund häufiger Fragen in den Kommentaren zur Art des EKGs erzähle ich Ihnen davon Interferenz die im Elektrokardiogramm erscheinen können: Drei Arten von EKG-Störungen(unten erklärt). Im Lexikon des Gesundheitspersonals wird „Eingriff in ein EKG“ genannt Hinweis: Das Gerät zur Aufzeichnung der elektrischen Aktivität des Herzens wurde in den 70er Jahren des 19. Jahrhunderts vom Engländer A. Waller praktisch eingesetzt und leistet bis heute treue Dienste für die Menschheit. Natürlich hat es im Laufe von fast 150 Jahren zahlreiche Veränderungen und Verbesserungen erfahren, aber das Funktionsprinzip, das auf der Aufzeichnung elektrischer Impulse basiert, die sich im Herzmuskel ausbreiten, ist dasselbe geblieben. Mittlerweile ist fast jedes Rettungsteam mit einem tragbaren, leichten und mobilen Elektrokardiographen ausgestattet, der es Ihnen ermöglicht, schnell ein EKG zu erstellen, keine kostbaren Minuten zu verschwenden, akute Herzerkrankungen zu diagnostizieren und den Patienten schnell ins Krankenhaus zu transportieren. Bei großherdigem Myokardinfarkt, Lungenembolie und anderen Erkrankungen, die Notfallmaßnahmen erfordern, zählen Minuten, sodass ein dringend durchgeführtes Elektrokardiogramm jeden Tag mehr als ein Leben rettet. Die Entschlüsselung eines EKGs für einen Arzt des Kardiologieteams ist eine übliche Sache, und wenn es auf das Vorliegen einer akuten kardiovaskulären Pathologie hinweist, schaltet das Team sofort die Sirene ein und geht ins Krankenhaus, wo es den Patienten unter Umgehung der Notaufnahme entbindet zur Notfallversorgung auf die Intensivstation. Die Diagnose wurde bereits per EKG gestellt und es ist keine Zeit verloren gegangen. Ja, Patienten möchten wissen, was die seltsamen Zähne auf dem Band, die der Rekorder hinterlassen hat, bedeuten. Bevor sie zum Arzt gehen, möchten sie das EKG selbst entziffern. Allerdings ist nicht alles so einfach und um die „anspruchsvolle“ Aufzeichnung zu verstehen, muss man wissen, was der menschliche „Motor“ ist. Das Herz von Säugetieren, zu denen auch der Mensch gehört, besteht aus 4 Kammern: zwei Vorhöfen, die mit Hilfsfunktionen ausgestattet sind und relativ dünne Wände haben, und zwei Ventrikeln, die die Hauptlast tragen. Auch der linke und der rechte Teil des Herzens sind unterschiedlich. Für den rechten Ventrikel ist es weniger schwierig, den Lungenkreislauf mit Blut zu versorgen, als das Blut über den linken in den großen Kreislauf zu drücken. Daher ist die linke Herzkammer stärker entwickelt, leidet aber auch stärker. Unabhängig vom Unterschied müssen jedoch beide Teile des Herzens gleichmäßig und harmonisch arbeiten. Das Herz ist in seiner Struktur und elektrischen Aktivität heterogen, da sich kontraktile Elemente (Myokard) und nichtkontraktile Elemente (Nerven, Gefäße, Klappen, Fettgewebe) in unterschiedlichem Ausmaß der elektrischen Reaktion unterscheiden. Typischerweise machen sich Patienten, insbesondere ältere, Sorgen darüber, ob im EKG Anzeichen eines Herzinfarkts zu erkennen sind, was durchaus verständlich ist. Dazu müssen Sie jedoch mehr über das Herz und das Kardiogramm erfahren. Und wir werden versuchen, diese Gelegenheit zu bieten, indem wir über Wellen, Intervalle und Ableitungen und natürlich über einige häufige Herzerkrankungen sprechen. Über die spezifischen Funktionen des Herzens erfahren wir zunächst aus Schulbüchern, also stellen wir uns vor, dass das Herz Folgendes hat: Automatisch, verursacht durch die spontane Erzeugung von Impulsen, die dann zu ihrer Erregung führen; Erregbarkeit oder die Fähigkeit des Herzens, sich unter dem Einfluss aufregender Impulse zu aktivieren; Leitfähigkeit oder die „Fähigkeit“ des Herzens, die Weiterleitung von Impulsen vom Ursprungsort zu den kontraktilen Strukturen sicherzustellen; Kontraktilität, das heißt die Fähigkeit des Herzmuskels, sich unter der Kontrolle von Impulsen zusammenzuziehen und zu entspannen; Tonizität, bei dem das Herz in der Diastole seine Form nicht verliert und eine kontinuierliche zyklische Aktivität gewährleistet. Im Allgemeinen ist der Herzmuskel in einem ruhigen Zustand (statische Polarisation) elektrisch neutral und Bioströme Unter dem Einfluss erregender Impulse entstehen darin elektrische Prozesse. Elektrische Prozesse im Herzen werden durch die Bewegung von Natriumionen (Na+), die sich ursprünglich außerhalb der Myokardzelle befinden, in die Myokardzelle und die Bewegung von Kaliumionen (K+) verursacht, die vom Inneren der Zelle nach außen strömen. Diese Bewegung schafft die Voraussetzungen für Veränderungen der Transmembranpotentiale während des gesamten Herzzyklus und wiederholt sich Depolarisationen(Erregung, dann Kontraktion) und Repolarisationen(Übergang in den ursprünglichen Zustand). Alle Myokardzellen haben elektrische Aktivität, eine langsame spontane Depolarisation ist jedoch nur für die Zellen des Reizleitungssystems charakteristisch, weshalb sie zum Automatismus fähig sind. Durch die Erregung, die an der Außenfläche des Myokards auftritt, bleibt dieser Teil im Vergleich zu Bereichen, die nicht von der Erregung betroffen sind, elektronegativ. Aufgrund der Tatsache, dass Körpergewebe jedoch über eine elektrische Leitfähigkeit verfügen, werden Bioströme auf die Körperoberfläche projiziert und können auf einem sich bewegenden Band in Form einer Kurve – einem Elektrokardiogramm – aufgezeichnet und aufgezeichnet werden. Das EKG besteht aus Wellen, die sich nach jedem Herzschlag wiederholen und durch sie die Störungen im menschlichen Herzen aufzeigen. Viele Menschen können diese Frage wahrscheinlich beantworten. Auch die Durchführung eines EKGs wird bei Bedarf kein Problem sein – in jeder Klinik gibt es einen Elektrokardiographen. EKG-Technik? Es scheint nur auf den ersten Blick, dass es jedem so vertraut ist, aber mittlerweile kennen es nur noch medizinische Fachkräfte, die eine spezielle Ausbildung für die Erstellung eines Elektrokardiogramms absolviert haben. Auf Einzelheiten müssen wir aber kaum eingehen, da uns ohne Vorbereitung ohnehin niemand erlauben wird, solche Arbeiten durchzuführen. Patienten müssen wissen, wie sie sich richtig vorbereiten: Das heißt, es ist ratsam, vor dem Eingriff nicht zu viel zu essen, nicht zu rauchen, keine alkoholischen Getränke und Medikamente zu sich zu nehmen, keine schwere körperliche Arbeit zu verrichten und keinen Kaffee zu trinken, da sonst das EKG auftritt kann getäuscht werden. Tachykardie wird auf jeden Fall gewährleistet sein, wenn nicht sogar etwas anderes. Ein völlig ruhiger Patient zieht sich also bis zur Taille aus, befreit seine Beine und legt sich auf die Couch. Die Krankenschwester schmiert die erforderlichen Stellen (Leitungen) mit einer speziellen Lösung und bringt Elektroden an, von denen Drähte unterschiedlicher Farbe zum Gerät führen. und ein Kardiogramm machen. Der Arzt wird es später entschlüsseln, aber wenn Sie interessiert sind, können Sie versuchen, Ihre Zähne und Intervalle selbst herauszufinden. Dieser Abschnitt ist möglicherweise nicht für jeden von Interesse. In diesem Fall können Sie ihn überspringen. Für diejenigen, die versuchen, ihr EKG selbst zu verstehen, kann er jedoch nützlich sein. Die Wellen im EKG werden mit lateinischen Buchstaben bezeichnet: P, Q, R, S, T, U, wobei jede von ihnen den Zustand verschiedener Teile des Herzens widerspiegelt: P – Vorhofdepolarisation; QRS-Wellenkomplex – ventrikuläre Depolarisation; T – ventrikuläre Repolarisation; Eine schwache U-Welle kann auf eine Repolarisation der distalen Teile des ventrikulären Reizleitungssystems hinweisen. Zur Aufzeichnung eines EKG werden üblicherweise 12 Ableitungen verwendet: 3 Standard – I, II, III; 3 verstärkte unipolare Extremitätenableitungen (nach Goldberger); 6 verstärkte unipolare Brust (nach Wilson). In einigen Fällen (Arrhythmien, abnormale Lage des Herzens) besteht die Notwendigkeit, zusätzliche unipolare Brust- und bipolare Elektroden nach Neb zu verwenden (D, A, I). Bei der Interpretation der EKG-Ergebnisse wird die Dauer der Intervalle zwischen seinen Komponenten gemessen. Diese Berechnung ist notwendig, um die Rhythmusfrequenz zu beurteilen, wobei die Form und Größe der Zähne in verschiedenen Ableitungen ein Indikator für die Art des Rhythmus, die im Herzen auftretenden elektrischen Phänomene und (in gewissem Maße) die elektrische Aktivität des Individuums sind Abschnitte des Myokards, das heißt das Elektrokardiogramm zeigt, wie unser Herz zu diesem Zeitpunkt oder zu einem anderen Zeitpunkt funktioniert.
Eine strengere Interpretation des EKG erfolgt durch die Analyse und Berechnung der Zahnfläche bei Verwendung spezieller Ableitungen (Vektortheorie), in der Praxis begnügt man sich jedoch meist mit einem Indikator wie Richtung der elektrischen Achse, das ist der gesamte QRS-Vektor. Es ist klar, dass jeder Brustkorb anders aufgebaut ist und das Herz keine so strenge Anordnung hat, auch das Gewichtsverhältnis der Ventrikel und die Leitfähigkeit in ihnen sind bei jedem unterschiedlich, daher muss bei der Entschlüsselung die horizontale oder vertikale Richtung dieses Vektors berücksichtigt werden angegeben ist. Ärzte führen die EKG-Analyse in sequentieller Reihenfolge durch und bestimmen die Norm und Verstöße: Beurteilen Sie den Herzrhythmus und messen Sie die Herzfrequenz (bei normalem EKG - Sinusrhythmus, Herzfrequenz - von 60 bis 80 Schlägen pro Minute); Es werden Intervalle (QT, Norm – 390-450 ms) berechnet, die die Dauer der Kontraktionsphase (Systole) anhand einer speziellen Formel charakterisieren (ich verwende oft die Bazett-Formel). Wenn sich dieses Intervall verlängert, hat der Arzt das Recht, eine ischämische Herzkrankheit, Arteriosklerose, Myokarditis oder Rheuma zu vermuten. Hyperkalzämie hingegen führt zu einer Verkürzung des QT-Intervalls. Die Leitfähigkeit der durch die Intervalle reflektierten Impulse wird mit einem Computerprogramm berechnet, was die Zuverlässigkeit der Ergebnisse deutlich erhöht; Die Position des EOS beginnt aus der Isolinie entlang der Höhe der Zähne zu berechnen (normalerweise ist R immer höher als S), und wenn S R überschreitet und die Achse nach rechts abweicht, denken sie an Störungen in der Aktivität des rechter Ventrikel, wenn im Gegenteil – nach links und die Höhe von S größer als R in den Ableitungen II und III ist – wird eine linksventrikuläre Hypertrophie vermutet; Untersucht wird der QRS-Komplex, der bei der Weiterleitung elektrischer Impulse an den Ventrikelmuskel entsteht und dessen Aktivität bestimmt (die Norm ist das Fehlen einer pathologischen Q-Welle, die Breite des Komplexes beträgt nicht mehr als 120 ms) . Verschiebt sich dieses Intervall, so spricht man von Blockaden (ganz oder teilweise) der Schenkeläste oder Erregungsleitungsstörungen. Darüber hinaus ist eine unvollständige Blockade des rechten Schenkels ein elektrokardiographisches Kriterium für eine rechtsventrikuläre Hypertrophie, und eine unvollständige Blockade des linken Schenkels kann auf eine linksventrikuläre Hypertrophie hinweisen. Sie beschreiben die ST-Segmente, die den Zeitraum der Wiederherstellung des Ausgangszustands des Herzmuskels nach seiner vollständigen Depolarisation (normalerweise auf der Isolinie gelegen) widerspiegeln, und die T-Welle, die den nach oben gerichteten Prozess der Repolarisation beider Ventrikel charakterisiert , asymmetrisch, seine Amplitude ist geringer als die Dauer der Welle und länger als der QRS-Komplex. Die Entschlüsselungsarbeiten werden nur von einem Arzt durchgeführt. Einige Rettungssanitäter erkennen jedoch häufige Pathologien perfekt, was in Notfällen sehr wichtig ist. Aber zuerst müssen Sie noch die EKG-Norm kennen. normales EKG So sieht das Kardiogramm eines gesunden Menschen aus, dessen Herz rhythmisch und korrekt arbeitet, aber nicht jeder weiß, was diese Aufzeichnung bedeutet, die sich unter verschiedenen physiologischen Bedingungen, beispielsweise einer Schwangerschaft, ändern kann. Bei schwangeren Frauen nimmt das Herz eine andere Position in der Brust ein, sodass sich die elektrische Achse verschiebt. Darüber hinaus kommt je nach Dauer die Belastung des Herzens hinzu. Ein EKG während der Schwangerschaft wird diese Veränderungen widerspiegeln. Auch die Kardiogrammindikatoren bei Kindern sind hervorragend; sie „wachsen“ mit dem Baby und verändern sich daher je nach Alter; erst nach 12 Jahren beginnt das Elektrokardiogramm des Kindes, sich dem EKG eines Erwachsenen anzunähern. private Formen des Herzinfarkts im EKG Die schwerwiegendste Diagnose im EKG ist natürlich der Myokardinfarkt, bei dessen Erkennung das Kardiogramm die Hauptrolle spielt, denn es (das erste!) findet Nekrosebereiche und bestimmt den Ort und die Tiefe der Läsion und kann einen akuten Infarkt von Aneurysmen und Narben der Vergangenheit unterscheiden. Die klassischen Anzeichen eines Myokardinfarkts im EKG sind die Registrierung einer tiefen Q-Welle (OS), SegmenthöheST, wodurch R verformt, geglättet wird und anschließend ein negativ spitzer gleichschenkliger Zahn T entsteht. Diese Erhebung des ST-Segments ähnelt optisch dem Rücken einer Katze („Katze“). Es wird jedoch zwischen einem Herzinfarkt mit und ohne Q-Welle unterschieden.
In EKG-Befunden findet man häufig den Ausdruck: „Linksventrikuläre Hypertrophie“. In der Regel wird ein solches Kardiogramm von Menschen erstellt, deren Herzen über längere Zeit beispielsweise durch Fettleibigkeit zusätzlich belastet waren. Es ist klar, dass es die linke Herzkammer in solchen Situationen schwer hat. Dann weicht die elektrische Achse nach links ab und S wird größer als R. Hypertrophie der linken (linken) und rechten (rechten) Herzkammer im EKG
Sinusarrhythmien sind ein interessantes Phänomen und Sie sollten keine Angst davor haben, da es bei gesunden Menschen vorhanden ist und keine Symptome oder Folgen hervorruft, sondern vielmehr dazu dient, das Herz auszuruhen, daher gilt es als Kardiogramm eines gesunden Menschen.
Eine Verletzung der intraventrikulären Reizleitung äußert sich in atrioventrikulären Blockaden und Schenkelblockaden. Rechtsschenkelblock – hohe und breite R-Zacke in den rechten präkordialen Ableitungen, mit linker Beinblock- Kleines R und breite, tiefe S-Welle in den rechten Brustableitungen, in den linken Brustableitungen - R ist verbreitert und gezackt. Beide Beine sind durch eine Erweiterung des Ventrikelkomplexes und dessen Verformung gekennzeichnet. Atrioventrikuläre Blockaden, die eine Störung der intraventrikulären Erregungsleitung verursachen, werden in drei Graden ausgedrückt, die davon abhängen, wie die Erregungsleitung die Ventrikel erreicht: langsam, manchmal oder überhaupt nicht. Aber all dies sind, könnte man sagen, „Blumen“, da es entweder überhaupt keine Symptome gibt oder sie keine so schreckliche Manifestation haben, zum Beispiel können bei einer atrioventrikulären Blockade Atemnot, Schwindel und Müdigkeit auftreten, und selbst dann nur bis zum 3. Grad, davon 1 Grad, ist bei jungen, ausgebildeten Menschen generell sehr verbreitet.
Bei Rhythmus- und Erregungsleitungsstörungen ist eine tägliche Holter-Überwachung vorgeschrieben, schmerzlose Formen der koronaren Herzkrankheit, Prinzmetal-Angina und andere pathologische Zustände. Indikationen für den Einsatz von Holter sind außerdem das Vorhandensein eines künstlichen Herzschrittmachers beim Patienten (Kontrolle über dessen Funktion) und der Einsatz von Antiarrhythmika und Medikamenten zur Behandlung von Ischämie. Bereit machen Die Holter-Überwachung ist ebenfalls einfach, Männer sollten jedoch die Elektrodenbefestigungspunkte rasieren, da Haare die Aufzeichnung verzerren. Obwohl angenommen wird, dass die tägliche Überwachung keine besondere Vorbereitung erfordert, wird der Patient in der Regel darüber informiert, was er tun kann und was nicht. Natürlich kann man nicht in ein Bad eintauchen, das Gerät mag keine Wasserprozeduren. Es gibt diejenigen, die nicht einmal Duschen akzeptieren, man muss es leider nur aushalten. Das Gerät reagiert empfindlich auf Magnete, Mikrowellen, Metalldetektoren und Hochspannungsleitungen Daher ist es besser, es nicht auf Stärke zu testen, da es trotzdem falsch geschrieben wird. Es gefällt ihm nicht Kunststoffe und alle Arten von Metallschmuck, daher sollten Sie für eine Weile darauf umsteigen Baumwollkleidung, und vergessen Sie Schmuck.
Jeder hat etwas von einem solchen Fahrrad gehört, aber nicht jeder ist damit gefahren (und nicht jeder kann es). Tatsache ist, dass latente Formen der Herzkranzgefäßinsuffizienz, Erregbarkeits- und Erregungsleitungsstörungen im Ruhe-EKG schlecht erkannt werden. Daher ist es üblich, den sogenannten Fahrradergometertest zu verwenden, bei dem das Kardiogramm mit dosierten Erhöhungen (manchmal) aufgezeichnet wird konstante) Belastungen. Bei einem Belastungs-EKG werden gleichzeitig die allgemeine Reaktion des Patienten auf diesen Eingriff sowie Blutdruck und Puls überwacht. Belastungsarten EKG: mit Heimtrainer und Laufband Die maximale Herzfrequenz bei einem Fahrradergometertest ist altersabhängig und beträgt 200 Schläge minus der Anzahl der Jahre, d. h. 20-Jährige können sich 180 Schläge/Minute leisten, mit 60 Jahren sind jedoch 130 Schläge/Minute die Grenze . Bei Bedarf wird ein Fahrradergometertest verordnet: Zur Abklärung der Diagnose einer koronaren Herzkrankheit, latent auftretenden Rhythmus- und Erregungsleitungsstörungen; Bewertung der Wirksamkeit der Behandlung koronarer Herzkrankheiten; Wählen Sie Medikamente für eine gesicherte Diagnose einer koronaren Herzkrankheit aus; Wählen Sie Trainings- und Belastungsprogramme während der Rehabilitationsphase für Patienten aus, die einen Herzinfarkt erlitten haben ( vor Ablauf eines Monats nach Beginn des Herzinfarkts ist dies nur in spezialisierten Kliniken möglich!); Bereitstellung einer prognostischen Beurteilung des Zustands von Patienten mit koronarer Herzkrankheit. Allerdings hat die Durchführung eines EKGs unter Belastung auch Kontraindikationen, insbesondere der Verdacht auf Herzinfarkt, Angina pectoris, Aortenaneurysmen, einige Extrasystolen, chronische Herzinsuffizienz in einem bestimmten Stadium, Schlaganfall und Thrombophlebitis stellen ein Hindernis für die Untersuchung dar. Diese Kontraindikationen sind absolut. Darüber hinaus gibt es eine Reihe relativ Kontraindikationen: einige Herzfehler, arterielle Hypertonie, paroxysmale Tachykardie, häufige Extrasystole, atrioventrikuläre Blockade usw. Die FCG- oder phonokardiographische Forschungsmethode ermöglicht es, die Geräuschsymptome des Herzens grafisch darzustellen, zu objektivieren und Töne und Geräusche (ihre Formen und Dauer) korrekt mit den Phasen des Herzzyklus zu korrelieren. Darüber hinaus hilft die Phonographie bei der Bestimmung einiger Zeitintervalle, zum Beispiel Q-I-Ton, Mitralklappenöffnungs-Ton II usw. Während der PCG wird gleichzeitig auch ein Elektrokardiogramm aufgezeichnet (eine zwingende Voraussetzung). Die Methode der Phonokardiographie ist einfach; moderne Geräte ermöglichen es, hoch- und niederfrequente Komponenten von Geräuschen zu isolieren und sie so darzustellen, dass sie für die Wahrnehmung des Forschers am bequemsten sind (vergleichbar mit der Auskultation). Bei der Erfassung pathologischer Geräusche ist die FCG der auskultatorischen Methode jedoch nicht überlegen, da sie keine höhere Empfindlichkeit aufweist und daher den Arzt mit einem Phonendoskop nicht ersetzt. Die Phonokardiographie wird in Fällen verordnet, in denen die Abklärung der Ursache von Herzgeräuschen oder die Diagnose von Herzklappenfehlern erforderlich ist, um die Indikation für einen chirurgischen Eingriff bei Herzfehlern zu ermitteln und auch, wenn nach einem Myokardinfarkt ungewöhnliche auskultatorische Symptome auftreten. Bei aktiver rheumatischer Karditis ist eine dynamische Studie mit PCG erforderlich, um das Entstehungsmuster von Herzfehlern sowie bei infektiöser Endokarditis zu klären. Schritt 1: Bezahlen Sie die Beratung über das Formular → Schritt 2: Stellen Sie nach der Zahlung Ihre Frage im untenstehenden Formular ↓ Schritt 3: Sie können dem Spezialisten zusätzlich mit einer weiteren Zahlung in beliebiger Höhe danken Ein geringes R-Wellen-Wachstum ist ein häufiges EKG-Symptom, das von Ärzten oft falsch interpretiert wird. Obwohl dieses Symptom normalerweise mit einem vorderen Myokardinfarkt verbunden ist, kann es durch andere Erkrankungen verursacht werden, die nicht mit dem Infarkt zusammenhängen. Ein kleiner Anstieg der R-Zacke wird ungefähr bei festgestellt 10 % der hospitalisierten erwachsenen Patienten
und ist die sechsthäufigste EKG-Anomalie (19.734 EKGs, die von der Metropolitan Life Insurance Company über einen Zeitraum von 5 ¼ Jahren gesammelt wurden). Außerdem, ein Drittel der Patienten mit früherem vorderen Myokardinfarkt
möglicherweise nur dieses Symptom im EKG. Daher ist die Aufklärung der spezifischen anatomischen Äquivalente dieses elektrokardiographischen Phänomens von großer klinischer Bedeutung. Die normale Höhe der R-Welle in Ableitung V3 beträgt normalerweise mehr als 2 mm
. Wenn die Höhe der R-Zacken in den Ableitungen V1–V4 extrem gering ist, spricht man von einer „unzureichenden oder geringen Zunahme der R-Zacke“. Bei einer Myokardnekrose aufgrund eines Infarkts wird ein bestimmter Teil des Myokardgewebes elektrisch inert und kann keine normale Depolarisation erzeugen. Zu diesem Zeitpunkt nimmt die Depolarisation des umgebenden Ventrikelgewebes zu (da ihnen kein Widerstand mehr entgegensteht) und der resultierende Depolarisationsvektor wird von der Nekrosezone weg (in Richtung der ungehinderten Ausbreitung) umorientiert. Bei einem vorderen Myokardinfarkt treten Q-Wellen in der rechten und mittleren Ableitung (V1-V4) auf. Bei einer erheblichen Anzahl von Patienten bleiben die Q-Wellen jedoch nicht erhalten. In dokumentierten Fällen eines früheren vorderen Myokardinfarkts, In 20–30 % der Fälle wird ein geringfügiger Anstieg der R-Welle festgestellt
. Die durchschnittliche Zeit bis zum vollständigen Verschwinden pathologischer Q-Wellen beträgt 1,5 Jahre.
Zieht Aufmerksamkeit auf sich Abnahme der Amplitude der R-Welle in Ableitung I
. Bis zu 85 % der Patienten mit vorderem Myokardinfarkt und einem leichten Anstieg der R-Welle haben beides Amplitude der R-Zacken in Ableitung I<= 4 мм
, oder Amplitude der R-Zacken in Ableitung V3<= 1,5 мм
. Das Fehlen dieser Amplitudenkriterien macht die Diagnose eines vorderen Myokardinfarkts unwahrscheinlich (außer in 10–15 % der Fälle eines vorderen Myokardinfarkts). Wenn die R-Wellen in den präkordialen Ableitungen leicht ansteigen, Repolarisationsstörung (ST-T-Änderungen) in den Ableitungen V1-V3
erhöht die Wahrscheinlichkeit, einen alten vorderen Myokardinfarkt zu diagnostizieren. Weitere mögliche Ursachen für ein unzureichendes Wachstum der R-Welle in den präkordialen Ableitungen Sind: Ein weiterer häufiger Grund für einen leichten Anstieg der R-Welle ist die falsche Platzierung der Elektroden: Die Brustelektroden sind zu hoch oder zu niedrig, die Elektroden befinden sich von den Gliedmaßen bis zum Rumpf. Es wurde ein Zusammenhang zwischen einem leichten Anstieg der R-Welle im EKG und einer diastolischen Dysfunktion bei Patienten mit Diabetes festgestellt, sodass dieses Symptom ein frühes Anzeichen einer LV-Dysfunktion und DCM bei Diabetikern sein kann. 7.2.1. Myokardhypertrophie Die Ursache einer Hypertrophie ist in der Regel eine übermäßige Belastung des Herzens, sei es durch Widerstand (arterielle Hypertonie) oder Volumen (chronische Nieren- und/oder Herzinsuffizienz). Eine erhöhte Herzarbeit führt zu einer Steigerung der Stoffwechselvorgänge im Myokard und geht in der Folge mit einer Zunahme der Muskelfaserzahl einher. Die bioelektrische Aktivität des hypertrophierten Teils des Herzens nimmt zu, was sich im Elektrokardiogramm widerspiegelt. 7.2.1.1. Hypertrophie des linken Vorhofs Ein charakteristisches Zeichen einer Hypertrophie des linken Vorhofs ist eine Zunahme der Breite der P-Welle (mehr als 0,12 s). Das zweite Zeichen ist eine Veränderung der Form der P-Welle (zwei Höcker mit überwiegendem zweiten Peak) (Abb. 6). Reis. 6. EKG für Hypertrophie des linken Vorhofs Die Hypertrophie des linken Vorhofs ist ein typisches Symptom einer Mitralklappenstenose und daher wird die P-Welle bei dieser Erkrankung P-Mitral genannt. Ähnliche Veränderungen werden in den Ableitungen I, II, aVL, V5, V6 beobachtet. 7.2.1.2. Hypertrophie des rechten Vorhofs Bei einer Hypertrophie des rechten Vorhofs wirken sich Veränderungen auch auf die P-Welle aus, die eine spitze Form annimmt und an Amplitude zunimmt (Abb. 7). Reis. 7. EKG für Hypertrophie des rechten Vorhofs (P-pulmonale), rechter Ventrikel (S-Typ) Eine Hypertrophie des rechten Vorhofs wird bei einem Vorhofseptumdefekt und einer Hypertonie des Lungenkreislaufs beobachtet. Am häufigsten wird eine solche P-Welle bei Erkrankungen der Lunge nachgewiesen; sie wird oft als P-pulmonale bezeichnet. Eine Hypertrophie des rechten Vorhofs ist ein Zeichen für Veränderungen der P-Welle in den Ableitungen II, III, aVF, V1, V2. 7.2.1.3. Linke ventrikuläre Hypertrophie Die Herzkammern sind besser an Stress angepasst und in den frühen Stadien erscheint ihre Hypertrophie möglicherweise nicht im EKG, aber mit der Entwicklung der Pathologie werden charakteristische Anzeichen sichtbar. Bei einer ventrikulären Hypertrophie zeigt das EKG deutlich mehr Veränderungen als bei einer Vorhofhypertrophie. Die Hauptzeichen einer linksventrikulären Hypertrophie sind (Abb. 8): Abweichung der elektrischen Achse des Herzens nach links (Levogramm); Verschiebung der Übergangszone nach rechts (in den Ableitungen V2 oder V3); Die R-Zacke in den Ableitungen V5, V6 ist hoch und hat eine größere Amplitude als RV4; Tiefes S in den Ableitungen V1, V2; Erweiterter QRS-Komplex in den Ableitungen V5, V6 (bis zu 0,1 s oder mehr); Verschiebung des S-T-Segments unterhalb der isoelektrischen Linie mit Konvexität nach oben; Negative T-Welle in den Ableitungen I, II, aVL, V5, V6. Reis. 8. EKG für linksventrikuläre Hypertrophie Eine linksventrikuläre Hypertrophie wird häufig bei arterieller Hypertonie, Akromegalie, Phäochromozytom sowie Mitral- und Aortenklappeninsuffizienz und angeborenen Herzfehlern beobachtet. 7.2.1.4. Rechtsventrikuläre Hypertrophie In fortgeschrittenen Fällen treten im EKG Anzeichen einer rechtsventrikulären Hypertrophie auf. Die Diagnose im Frühstadium einer Hypertrophie ist äußerst schwierig. Anzeichen einer Hypertrophie (Abb. 9): Abweichung der elektrischen Achse des Herzens nach rechts (Pravogramm); Tiefe S-Welle in Ableitung V1 und hohe R-Welle in den Ableitungen III, aVF, V1, V2; Die Höhe des RV6-Zahns ist geringer als normal; Erweiterter QRS-Komplex in den Ableitungen V1, V2 (bis zu 0,1 s oder mehr); Tiefe S-Welle in Ableitung V5 und auch V6; Verschiebung des S-T-Segments unterhalb der Isolinie mit Konvexität nach oben rechts III, aVF, V1 und V2; Vollständige oder unvollständige Blockade des rechten Schenkels; Verschieben Sie die Übergangszone nach links. Reis. 9. EKG für rechtsventrikuläre Hypertrophie Eine rechtsventrikuläre Hypertrophie ist am häufigsten mit einem erhöhten Druck im Lungenkreislauf bei Lungenerkrankungen, Mitralklappenstenose, Wandthrombose und Lungenstenose sowie angeborenen Herzfehlern verbunden. 7.2.2. Rhythmusstörungen Schwäche, Kurzatmigkeit, schneller Herzschlag, häufiges und erschwertes Atmen, Störungen der Herzfunktion, Erstickungsgefühl, Ohnmacht oder Episoden von Bewusstlosigkeit können Anzeichen von Herzrhythmusstörungen aufgrund von Herz-Kreislauf-Erkrankungen sein. Ein EKG hilft, ihr Vorhandensein zu bestätigen und vor allem ihren Typ zu bestimmen. Es sollte daran erinnert werden, dass die Automatik eine einzigartige Eigenschaft der Zellen des Reizleitungssystems des Herzens ist und der Sinusknoten, der den Rhythmus steuert, die größte Automatik aufweist. Rhythmusstörungen (Arrhythmien) werden diagnostiziert, wenn im EKG kein Sinusrhythmus erkennbar ist. Anzeichen eines normalen Sinusrhythmus: P-Wellen-Frequenz – im Bereich von 60 bis 90 (pro 1 Minute); Identische Dauer der R-R-Intervalle; Positive P-Welle in allen Ableitungen außer aVR. Herzrhythmusstörungen sind sehr vielfältig. Alle Arrhythmien werden in nomotopische (Veränderungen treten im Sinusknoten selbst) und heterotope unterteilt. Im letzteren Fall entstehen erregende Impulse außerhalb des Sinusknotens, also in den Vorhöfen, im atrioventrikulären Übergang und in den Ventrikeln (in den Ästen des His-Bündels). Zu den nomotopen Arrhythmien zählen Sinusbrady und Tachykardie sowie ein unregelmäßiger Sinusrhythmus. Heterotop – Vorhofflimmern und -flattern und andere Störungen. Wenn das Auftreten von Arrhythmien mit einer Erregbarkeitsstörung verbunden ist, werden solche Rhythmusstörungen in Extrasystole und paroxysmale Tachykardie unterteilt. Angesichts der Vielfalt der Arten von Arrhythmien, die im EKG erkannt werden können, erlaubte sich der Autor, den Leser nicht mit den Feinheiten der medizinischen Wissenschaft zu langweilen, nur die Grundkonzepte zu definieren und die wichtigsten Rhythmus- und Erregungsleitungsstörungen zu betrachten. 7.2.2.1. Sinustachykardie Verstärkte Impulserzeugung im Sinusknoten (mehr als 100 Impulse pro Minute). Im EKG äußert es sich durch das Vorhandensein einer normalen P-Welle und einer Verkürzung des R-R-Intervalls. 7.2.2.2. Sinusbradykardie Die Impulserzeugungsfrequenz im Sinusknoten überschreitet nicht 60. Im EKG äußert es sich durch das Vorhandensein einer normalen P-Welle und einer Verlängerung des R-R-Intervalls. Es ist zu beachten, dass bei einer Kontraktionsfrequenz von weniger als 30 eine Bradykardie kein Sinus ist. Sowohl bei Tachykardie als auch bei Bradykardie wird der Patient wegen der Krankheit behandelt, die die Rhythmusstörung verursacht hat. 7.2.2.3. Unregelmäßiger Sinusrhythmus Im Sinusknoten werden unregelmäßig Impulse erzeugt. Das EKG zeigt normale Wellen und Intervalle, die Dauer der R-R-Intervalle unterscheidet sich jedoch um mindestens 0,1 s. Diese Art von Herzrhythmusstörungen kann bei gesunden Menschen auftreten und erfordert keine Behandlung. 7.2.2.4. Idioventrikulärer Rhythmus Heterotope Arrhythmie, bei der der Schrittmacher entweder die Schenkel oder die Purkinje-Fasern sind. Extrem schwere Pathologie. Ein seltener Rhythmus im EKG (d. h. 30–40 Schläge pro Minute), die P-Welle fehlt, die QRS-Komplexe sind deformiert und verbreitert (Dauer 0,12 s oder mehr). Tritt nur bei schwerer Herzerkrankung auf. Ein Patient mit einer solchen Störung benötigt eine Notfallversorgung und muss sofort auf einer Herz-Intensivstation stationär behandelt werden. 7.2.2.5. Extrasystole Außergewöhnliche Kontraktion des Herzens, verursacht durch einen einzelnen ektopischen Impuls. Von praktischer Bedeutung ist die Einteilung der Extrasystolen in supraventrikuläre und ventrikuläre. Eine supraventrikuläre (auch atriale) Extrasystole wird im EKG aufgezeichnet, wenn der Herd, der eine außerordentliche Erregung (Kontraktion) des Herzens verursacht, in den Vorhöfen liegt. Die ventrikuläre Extrasystole wird im Kardiogramm aufgezeichnet, wenn sich in einem der Ventrikel ein ektopischer Herd bildet. Extrasystolen können selten, häufig (mehr als 10 % der Herzkontraktionen in 1 Minute), paarweise (Bigämenie) und gruppiert (mehr als drei hintereinander) auftreten. Lassen Sie uns die EKG-Anzeichen einer Vorhofextrasystole auflisten: P-Welle veränderte sich in Form und Amplitude; Das P-Q-Intervall wird verkürzt; Ein vorzeitig erfasster QRS-Komplex unterscheidet sich in seiner Form nicht vom normalen (Sinus-)Komplex; Das R-R-Intervall, das auf die Extrasystole folgt, ist länger als gewöhnlich, aber kürzer als zwei normale Intervalle (unvollständige kompensatorische Pause). Vorhofextrasystolen treten häufiger bei älteren Menschen vor dem Hintergrund einer Kardiosklerose und einer koronaren Herzkrankheit auf, können aber auch bei nahezu gesunden Menschen beobachtet werden, beispielsweise wenn eine Person große Sorgen hat oder unter Stress steht. Wenn bei einer praktisch gesunden Person eine Extrasystole festgestellt wird, besteht die Behandlung in der Verschreibung von Valocordin, Corvalol und der Gewährleistung vollständiger Ruhe. Bei der Registrierung einer Extrasystole bei einem Patienten sind außerdem die Behandlung der Grunderkrankung und die Einnahme von Antiarrhythmika aus der Isoptingruppe erforderlich. Anzeichen einer ventrikulären Extrasystole: Die P-Welle fehlt; Der außerordentliche QRS-Komplex ist deutlich verbreitert (mehr als 0,12 s) und deformiert; Volle Ausgleichspause. Eine ventrikuläre Extrasystole weist immer auf eine Herzschädigung hin (ischämische Herzkrankheit, Myokarditis, Endokarditis, Herzinfarkt, Arteriosklerose). Bei einer ventrikulären Extrasystole mit einer Frequenz von 3–5 Kontraktionen pro Minute ist eine antiarrhythmische Therapie zwingend erforderlich. Lidocain wird am häufigsten intravenös verabreicht, es können jedoch auch andere Medikamente eingesetzt werden. Die Behandlung erfolgt unter sorgfältiger EKG-Überwachung. 7.2.2.6. Paroxysmale Tachykardie Ein plötzlicher Anfall extrem häufiger Wehen, der einige Sekunden bis mehrere Tage andauern kann. Der heterotope Schrittmacher befindet sich entweder in den Ventrikeln oder supraventrikulär. Bei einer supraventrikulären Tachykardie (in diesem Fall werden Impulse in den Vorhöfen oder im atrioventrikulären Knoten gebildet) wird im EKG der korrekte Rhythmus mit einer Frequenz von 180 bis 220 Kontraktionen pro Minute aufgezeichnet. QRS-Komplexe werden nicht verändert oder erweitert. Bei der ventrikulären Form der paroxysmalen Tachykardie können die P-Wellen ihre Position im EKG verändern, die QRS-Komplexe werden deformiert und verbreitert. Eine supraventrikuläre Tachykardie tritt beim Wolff-Parkinson-White-Syndrom auf, seltener bei akutem Myokardinfarkt. Die ventrikuläre Form der paroxysmalen Tachykardie wird bei Patienten mit Myokardinfarkt, ischämischer Herzkrankheit und Störungen des Elektrolytstoffwechsels festgestellt. 7.2.2.7. Vorhofflimmern (Vorhofflimmern) Eine Art supraventrikulärer Arrhythmien, die durch asynchrone, unkoordinierte elektrische Aktivität der Vorhöfe mit anschließender Verschlechterung ihrer kontraktilen Funktion verursacht werden. Der Impulsfluss wird nicht vollständig zu den Ventrikeln geleitet und diese ziehen sich unregelmäßig zusammen. Diese Arrhythmie ist eine der häufigsten Herzrhythmusstörungen. Sie tritt bei mehr als 6 % der Patienten über 60 Jahre und bei 1 % der Patienten unter diesem Alter auf. Anzeichen von Vorhofflimmern: R-R-Intervalle sind unterschiedlich (Arrhythmie); Es gibt keine P-Wellen; Es werden Flimmerwellen aufgezeichnet (besonders deutlich sichtbar in den Ableitungen II, III, V1, V2); Elektrischer Wechsel (unterschiedliche Amplituden der I-Wellen in einer Ableitung). Vorhofflimmern tritt bei Mitralstenose, Thyreotoxikose und Kardiosklerose sowie häufig auch bei Myokardinfarkt auf. Die medizinische Versorgung besteht darin, den Sinusrhythmus wiederherzustellen. Zum Einsatz kommen Procainamid, Kaliumpräparate und andere Antiarrhythmika. 7.2.2.8. Vorhofflattern Es wird viel seltener beobachtet als Vorhofflimmern. Beim Vorhofflattern fehlen die normale Erregung und Kontraktion der Vorhöfe und es wird eine Erregung und Kontraktion einzelner Vorhoffasern beobachtet. 7.2.2.9. Kammerflimmern Die gefährlichste und schwerste Rhythmusstörung, die schnell zum Stillstand der Blutzirkulation führt. Tritt während eines Myokardinfarkts sowie in den Endstadien verschiedener Herz-Kreislauf-Erkrankungen bei Patienten auf, die sich im Zustand des klinischen Todes befinden. Bei Kammerflimmern sind dringend Wiederbelebungsmaßnahmen erforderlich. Anzeichen von Kammerflimmern: Fehlen aller Zähne des Ventrikelkomplexes; Registrierung von Flimmerwellen in allen Ableitungen mit einer Frequenz von 450–600 Wellen pro 1 Minute. 7.2.3. Leitungsstörungen Veränderungen im Kardiogramm, die bei einer Störung der Impulsleitung in Form einer Verlangsamung oder eines völligen Ausfalls der Erregungsübertragung auftreten, werden als Blockaden bezeichnet. Die Klassifizierung der Blockaden richtet sich nach der Ebene, auf der der Verstoß stattgefunden hat. Es gibt sinusförmige, atriale, atrioventrikuläre und intraventrikuläre Blockaden. Jede dieser Gruppen ist weiter unterteilt. Beispielsweise gibt es Sinusblockaden I, II und III Grad, Blockaden des rechten und linken Schenkels. Es gibt auch eine detailliertere Einteilung (Blockade des vorderen Astes des linken Schenkels, unvollständige Blockade des rechten Schenkels). Unter den mittels EKG erfassten Erregungsleitungsstörungen sind folgende Blockaden von größter praktischer Bedeutung: Sinoatrieller Grad III; Atrioventrikulärer Grad I, II und III; Blockade des rechten und linken Schenkels. 7.2.3.1. Sinusblock III Grad Eine Erregungsleitungsstörung, bei der die Erregungsleitung vom Sinusknoten zu den Vorhöfen blockiert ist. Bei einem scheinbar normalen EKG verschwindet die nächste Kontraktion plötzlich (wird blockiert), also der gesamte P-QRS-T-Komplex (oder 2-3 Komplexe gleichzeitig). An ihrer Stelle wird eine Isolinie aufgezeichnet. Die Pathologie wird bei Patienten mit koronarer Herzkrankheit, Herzinfarkt, Kardiosklerose und bei der Einnahme einer Reihe von Medikamenten (z. B. Betablockern) beobachtet. Die Behandlung besteht aus der Behandlung der Grunderkrankung und der Anwendung von Atropin, Isadrin und ähnlichen Mitteln. 7.2.3.2. Atrioventrikulärer Block Gestörte Erregungsleitung vom Sinusknoten über die atrioventrikuläre Verbindung. Eine Verlangsamung der atrioventrikulären Überleitung ist ein atrioventrikulärer Block ersten Grades. Manifestiert sich im EKG als Verlängerung des P-Q-Intervalls (mehr als 0,2 s) bei normaler Herzfrequenz. Ein atrioventrikulärer Block zweiten Grades ist ein unvollständiger Block, bei dem nicht alle vom Sinusknoten kommenden Impulse das ventrikuläre Myokard erreichen. Im EKG werden die folgenden zwei Arten von Blockaden unterschieden: die erste ist Mobitz-1 (Samoilov-Wenckebach) und die zweite ist Mobitz-2. Anzeichen einer Blockade vom Typ Mobitz-1: Ständig verlängerndes P-Intervall Aufgrund des ersten Anzeichens verschwindet der QRS-Komplex irgendwann nach der P-Welle. Ein Zeichen für einen Mobitz-2-Block ist der periodische Verlust des QRS-Komplexes vor dem Hintergrund eines verlängerten P-Q-Intervalls. Ein atrioventrikulärer Block dritten Grades ist ein Zustand, bei dem kein einziger Impuls vom Sinusknoten zu den Ventrikeln weitergeleitet wird. Das EKG zeichnet zwei Rhythmusarten auf, die nicht miteinander zusammenhängen: Die Arbeit der Ventrikel (QRS-Komplexe) und der Vorhöfe (P-Wellen) ist nicht koordiniert. Eine Blockade dritten Grades tritt häufig bei Kardiosklerose, Myokardinfarkt und unsachgemäßer Anwendung von Herzglykosiden auf. Das Vorliegen einer solchen Blockade bei einem Patienten ist ein Hinweis auf seine dringende Einweisung in ein kardiologisches Krankenhaus. Zur Behandlung werden Atropin, Ephedrin und in einigen Fällen Prednisolon eingesetzt. 7.2.Z.Z. Bündelverzweigungsblöcke Bei einem gesunden Menschen erregt ein vom Sinusknoten ausgehender elektrischer Impuls, der durch die Äste des His-Bündels verläuft, gleichzeitig beide Ventrikel. Bei einer Blockade des rechten oder linken Schenkels verändert sich der Impulsweg und damit verzögert sich die Erregung des entsprechenden Ventrikels. Auch unvollständige Blockaden und sogenannte Blockaden der vorderen und hinteren Schenkeläste sind möglich. Anzeichen einer vollständigen Blockade des rechten Schenkels (Abb. 10): Deformierter und erweiterter (mehr als 0,12 s) QRS-Komplex; Negative T-Welle in den Ableitungen V1 und V2; Verschiebung des S-T-Segments von der Isolinie; Verbreiterung und Aufspaltung des QRS in den Ableitungen V1 und V2 in Form von RsR. Reis. 10. EKG mit vollständigem Block des rechten Schenkels Anzeichen einer vollständigen Blockade des linken Schenkels: Der QRS-Komplex ist deformiert und verbreitert (mehr als 0,12 s); Versatz des S-T-Segments von der Isolinie; Negative T-Welle in den Ableitungen V5 und V6; Erweiterung und Aufspaltung des QRS-Komplexes in den Ableitungen V5 und V6 in Form von RR; Verformung und Erweiterung des QRS in den Ableitungen V1 und V2 in Form von rS. Solche Blockaden treten bei Herzverletzungen, akutem Myokardinfarkt, atherosklerotischer und myokardialer Kardiosklerose sowie bei unsachgemäßer Anwendung einer Reihe von Medikamenten (Herzglykoside, Novocainamid) auf. Patienten mit intraventrikulärem Block benötigen keine spezielle Therapie. Sie werden zur Behandlung der Krankheit, die die Blockade verursacht hat, ins Krankenhaus eingeliefert. 7.2.4. Wolff-Parkinson-White-Syndrom Dieses Syndrom (WPW) wurde erstmals 1930 von den oben genannten Autoren als eine Form der supraventrikulären Tachykardie beschrieben, die bei jungen gesunden Menschen beobachtet wird („funktioneller Schenkelblock“). Es wurde nun festgestellt, dass es im Körper manchmal zusätzlich zum normalen Weg der Impulsleitung vom Sinusknoten zu den Ventrikeln zusätzliche Bündel gibt (Kent, James und Mahaim). Auf diesen Wegen gelangt die Erregung schneller in die Herzkammern. Es gibt verschiedene Arten des WPW-Syndroms. Wenn die Erregung früher in den linken Ventrikel gelangt, wird das WPW-Syndrom Typ A im EKG erfasst. Bei Typ B gelangt die Erregung früher in den rechten Ventrikel. Anzeichen des WPW-Syndroms Typ A: Die Deltawelle auf dem QRS-Komplex ist in den rechten präkordialen Ableitungen positiv und in der linken negativ (das Ergebnis einer vorzeitigen Erregung eines Teils des Ventrikels); Die Richtung der Hauptzähne in den Brustableitungen ist ungefähr die gleiche wie bei der Blockade des linken Schenkels. Anzeichen des WPW-Syndroms Typ B: Verkürztes (weniger als 0,11 s) P-Q-Intervall; Der QRS-Komplex ist verbreitert (mehr als 0,12 s) und deformiert; Negative Deltawelle für die rechten Brustableitungen, positiv für die linken; Die Richtung der Hauptzähne in den Brustableitungen ist ungefähr die gleiche wie bei der Blockade des rechten Schenkels. Es ist möglich, ein stark verkürztes P-Q-Intervall mit einem undeformierten QRS-Komplex und dem Fehlen einer Deltawelle zu registrieren (Lown-Ganong-Levin-Syndrom). Zusätzliche Bundles werden vererbt. In etwa 30–60 % der Fälle manifestieren sie sich nicht. Bei manchen Menschen kann es zu Anfällen von Tachyarrhythmien kommen. Bei Herzrhythmusstörungen erfolgt die medizinische Versorgung nach den allgemeinen Regeln. 7.2.5. Frühe ventrikuläre Repolarisation Dieses Phänomen tritt bei 20 % der Patienten mit kardiovaskulärer Pathologie auf (am häufigsten bei Patienten mit supraventrikulären Herzrhythmusstörungen). Dabei handelt es sich nicht um eine Krankheit, aber Patienten mit Herz-Kreislauf-Erkrankungen, bei denen dieses Syndrom auftritt, leiden zwei- bis viermal häufiger an Rhythmus- und Erregungsleitungsstörungen. Zu den Anzeichen einer frühen ventrikulären Repolarisation (Abb. 11) gehören: ST-Strecken-Hebung; Späte Deltawelle (Kerbe im absteigenden Teil der R-Welle); Zähne mit hoher Amplitude; Doppelhöckerige P-Welle normaler Dauer und Amplitude; Verkürzung der PR- und QT-Intervalle; Es kommt zu einem schnellen und starken Anstieg der Amplitude der R-Welle im Brustkorb. Reis. 11. EKG für frühes ventrikuläres Repolarisationssyndrom 7.2.6. Herzischämie Bei der koronaren Herzkrankheit (KHK) ist die Blutversorgung des Herzmuskels beeinträchtigt. In den frühen Stadien kann es zu keinen Veränderungen im Elektrokardiogramm kommen, in späteren Stadien sind sie jedoch sehr auffällig. Mit der Entwicklung einer Myokarddystrophie treten Veränderungen der T-Welle und Anzeichen diffuser Veränderungen im Myokard auf. Diese beinhalten: Reduzierte Amplitude der R-Zacke; Depression des S-T-Segments; Biphasische, mäßig verbreiterte und flache T-Welle in fast allen Ableitungen. IHD tritt bei Patienten mit Myokarditis unterschiedlicher Genese sowie dystrophischen Veränderungen des Myokards und atherosklerotischer Kardiosklerose auf. 7.2.7. Angina pectoris Mit der Entwicklung eines Angina pectoris-Anfalls kann das EKG eine Verschiebung des S-T-Segments und Veränderungen der T-Welle in den Ableitungen erkennen, die über dem Bereich mit beeinträchtigter Blutversorgung liegen (Abb. 12). Reis. 12. EKG bei Angina pectoris (während eines Anfalls) Die Ursachen für Angina pectoris sind Hypercholesterinämie und Dyslipidämie. Darüber hinaus können arterielle Hypertonie, Diabetes mellitus, psycho-emotionale Überlastung, Angst und Fettleibigkeit die Entwicklung eines Anfalls auslösen. Je nachdem, in welcher Schicht des Herzmuskels eine Ischämie auftritt, gibt es: Subendokardiale Ischämie (über dem ischämischen Bereich liegt die S-T-Verschiebung unterhalb der Isolinie, die T-Welle ist positiv und hat eine große Amplitude); Subepikardiale Ischämie (Anstieg des S-T-Segments über die Isolinie, T negativ). Das Auftreten einer Angina pectoris geht mit dem Auftreten typischer Brustschmerzen einher, die meist durch körperliche Aktivität hervorgerufen werden. Dieser Schmerz ist von Natur aus drückend, dauert mehrere Minuten und verschwindet nach der Einnahme von Nitroglycerin. Wenn der Schmerz länger als 30 Minuten anhält und durch die Einnahme von Nitromedikamenten nicht gelindert wird, ist höchstwahrscheinlich von akuten Herdveränderungen auszugehen. Bei der Notfallversorgung bei Angina pectoris geht es darum, Schmerzen zu lindern und wiederkehrenden Anfällen vorzubeugen. Es werden Analgetika (von Analgin bis Promedol), Nitromedikamente (Nitroglycerin, Sustak, Nitrong, Monocinque usw.) sowie Validol und Diphenhydramin, Seduxen verschrieben. Bei Bedarf wird eine Sauerstoffinhalation durchgeführt. 7.2.8. Herzinfarkt Unter einem Myokardinfarkt versteht man die Entwicklung einer Nekrose des Herzmuskels als Folge längerer Durchblutungsstörungen im ischämischen Bereich des Myokards. In mehr als 90 % der Fälle wird die Diagnose anhand eines EKG gestellt. Darüber hinaus können Sie mit einem Kardiogramm das Stadium eines Herzinfarkts bestimmen sowie dessen Ort und Art herausfinden. Ein unbedingtes Zeichen eines Herzinfarkts ist das Auftreten einer pathologischen Q-Welle im EKG, die durch eine übermäßige Breite (mehr als 0,03 s) und eine größere Tiefe (ein Drittel der R-Welle) gekennzeichnet ist. Mögliche Optionen: QS, QrS. Es werden eine S-T-Verschiebung (Abb. 13) und eine T-Wellen-Inversion beobachtet. Reis. 13. EKG bei anterolateralem Myokardinfarkt (akutes Stadium). Es gibt narbige Veränderungen in den hinteren unteren Teilen des linken Ventrikels Manchmal kommt es zu einer S-T-Verschiebung, ohne dass eine pathologische Q-Welle vorliegt (kleinfokaler Myokardinfarkt). Anzeichen eines Herzinfarkts: Pathologische Q-Welle in Ableitungen oberhalb des Infarktbereichs; Verschiebung des S-T-Segments um einen Bogen nach oben (Anhebung) relativ zur Isolinie in den Ableitungen oberhalb des Infarktbereichs; Diskordante Verschiebung unterhalb der S-T-Segment-Isolinie in Ableitungen gegenüber dem Infarktbereich; Negative T-Welle in Ableitungen oberhalb des Infarktbereichs. Mit fortschreitender Krankheit verändert sich das EKG. Dieser Zusammenhang wird durch die Stadien der Veränderungen während eines Herzinfarkts erklärt. Es gibt vier Stadien in der Entwicklung eines Myokardinfarkts: Akut; Subakut; Narbenstadium. Das akuteste Stadium (Abb. 14) dauert mehrere Stunden. Zu diesem Zeitpunkt steigt das S-T-Segment in den entsprechenden Ableitungen im EKG stark an und verschmilzt mit der T-Welle. Reis. 14. Reihenfolge der EKG-Veränderungen während eines Myokardinfarkts: 1 – Q-Infarkt; 2 – kein Q-Infarkt; A – das akuteste Stadium; B – akutes Stadium; B – subakutes Stadium; D – Narbenstadium (Kardiosklerose nach Infarkt) Im akuten Stadium bildet sich eine Nekrosezone und es erscheint eine pathologische Q-Welle. Die R-Amplitude nimmt ab, das S-T-Segment bleibt erhöht und die T-Welle wird negativ. Die Dauer des akuten Stadiums beträgt durchschnittlich etwa 1–2 Wochen. Das subakute Infarktstadium dauert 1–3 Monate und ist durch eine narbige Organisation des Nekroseherdes gekennzeichnet. Im EKG kommt es zu diesem Zeitpunkt zu einer allmählichen Rückkehr des S-T-Segments zur Isolinie, die Q-Welle nimmt ab und die R-Amplitude nimmt im Gegenteil zu. Die T-Welle bleibt negativ. Das Narbenstadium kann mehrere Jahre dauern. Zu diesem Zeitpunkt findet die Organisation des Narbengewebes statt. Im EKG nimmt die Q-Welle ab oder verschwindet vollständig, S-T liegt auf der Isolinie, negatives T wird allmählich isoelektrisch und dann positiv. Diese Phasenlage wird oft als die natürliche Dynamik des EKG während eines Myokardinfarkts bezeichnet. Ein Herzinfarkt kann in jedem Teil des Herzens lokalisiert sein, am häufigsten tritt er jedoch in der linken Herzkammer auf. Je nach Lokalisation wird zwischen einem Infarkt der vorderen Seiten- und Hinterwand des linken Ventrikels unterschieden. Die Lokalisation und das Ausmaß der Veränderungen werden durch die Analyse der EKG-Veränderungen in den entsprechenden Ableitungen aufgedeckt (Tabelle 6). Tabelle 6. Lokalisierung des Myokardinfarkts Große Schwierigkeiten bei der Diagnose eines wiederkehrenden Infarkts entstehen, wenn neue Veränderungen einem bereits veränderten EKG überlagert werden. Dabei hilft ein dynamisches Monitoring mit der Aufzeichnung eines Kardiogramms in kurzen Abständen. Ein typischer Herzinfarkt ist durch brennende, starke Brustschmerzen gekennzeichnet, die auch nach der Einnahme von Nitroglycerin nicht verschwinden. Es gibt auch atypische Formen des Herzinfarkts: Abdominal (Herz- und Magenschmerzen); Asthmatiker (Herzschmerzen und Herzasthma oder Lungenödem); Arrhythmisch (Herzschmerzen und Rhythmusstörungen); Kollaptoid (Herzschmerzen und starker Blutdruckabfall mit starkem Schwitzen); Schmerzlos. Die Behandlung eines Herzinfarkts ist eine äußerst schwierige Aufgabe. Generell gilt: Je schwieriger es wird, desto weiter verbreitet sich die Läsion. Gleichzeitig, so die treffende Bemerkung eines der russischen Zemstvo-Ärzte, verläuft die Behandlung eines extrem schweren Herzinfarkts manchmal unerwartet reibungslos, und manchmal macht ein unkomplizierter, einfacher Mikroinfarkt den Arzt zum Zeichen der Impotenz. Die Notfallversorgung besteht in der Linderung von Schmerzen (zu diesem Zweck werden Betäubungsmittel und andere Analgetika eingesetzt), außerdem in der Beseitigung von Ängsten und psycho-emotionalen Erregungen mit Hilfe von Beruhigungsmitteln, in der Verkleinerung des Herzinfarktbereichs (mit Heparin) und in der sequentiellen Beseitigung andere Symptome je nach Grad ihrer Gefährdung. Nach Abschluss der stationären Behandlung werden Patienten, die einen Herzinfarkt erlitten haben, zur Rehabilitation in ein Sanatorium geschickt. Die letzte Phase ist die Langzeitbeobachtung in einer örtlichen Klinik. 7.2.9. Syndrome aufgrund von Elektrolytstörungen Bestimmte EKG-Veränderungen ermöglichen eine Beurteilung der Dynamik des Elektrolytgehalts im Myokard. Fairerweise muss man sagen, dass nicht immer ein eindeutiger Zusammenhang zwischen dem Elektrolytgehalt im Blut und dem Elektrolytgehalt im Myokard besteht. Dennoch sind im EKG festgestellte Elektrolytstörungen eine wichtige Hilfe für den Arzt bei der Diagnosesuche und bei der Auswahl der richtigen Behandlung. Die am besten untersuchten Veränderungen im EKG sind Störungen des Kalium- und Kalziumstoffwechsels (Abb. 15). Reis. 15. EKG-Diagnose von Elektrolytstörungen (A. S. Vorobyov, 2003): 1 – normal; 2 – Hypokaliämie; 3 – Hyperkaliämie; 4 – Hypokalzämie; 5 – Hyperkalzämie 7.2.9.1. Hyperkaliämie Anzeichen einer Hyperkaliämie: Hohe, spitze T-Welle; Verkürzung des Q-T-Intervalls; Verringerte R-Amplitude. Bei schwerer Hyperkaliämie werden intraventrikuläre Erregungsleitungsstörungen beobachtet. Hyperkaliämie tritt bei Diabetes (Azidose), chronischem Nierenversagen, schweren Verletzungen mit Muskelzerrungen, Nebenniereninsuffizienz und anderen Erkrankungen auf. 7.2.9.2. Hypokaliämie Anzeichen einer Hypokaliämie: Vermindertes S-T-Segment nach unten; Negatives oder biphasisches T; Der Auftritt von U. Bei schwerer Hypokaliämie treten atriale und ventrikuläre Extrasystolen sowie intraventrikuläre Erregungsleitungsstörungen auf. Hypokaliämie tritt auf, wenn es bei Patienten mit starkem Erbrechen, Durchfall, nach längerer Einnahme von Diuretika, Steroidhormonen und bei einer Reihe endokriner Erkrankungen zu einem Verlust von Kaliumsalzen kommt. Die Behandlung besteht darin, den Kaliummangel im Körper auszugleichen. 7.2.9.3. Hyperkalzämie Anzeichen einer Hyperkalzämie: Verkürzung des Q-T-Intervalls; Verkürzung des S-T-Segments; Erweiterung des Ventrikelkomplexes; Rhythmusstörungen mit deutlichem Anstieg des Kalziums. Hyperkalzämie wird bei Hyperparathyreoidismus, Knochenzerstörung durch Tumoren, Hypervitaminose D und übermäßiger Gabe von Kaliumsalzen beobachtet. 7.2.9.4. Hypokalzämie Anzeichen einer Hypokalzämie: Verlängerung der Dauer des QT-Intervalls; Verlängerung des S-T-Segments; Verminderte T-Amplitude. Hypokalzämie tritt bei verminderter Funktion der Nebenschilddrüsen, bei Patienten mit chronischem Nierenversagen, bei schwerer Pankreatitis und Hypovitaminose D auf. 7.2.9.5. Glykosidvergiftung Herzglykoside werden seit langem erfolgreich zur Behandlung von Herzinsuffizienz eingesetzt. Diese Werkzeuge sind unersetzlich. Ihre Einnahme trägt dazu bei, die Herzfrequenz (Herzfrequenz) zu senken und das Blut während der Systole kräftiger auszustoßen. Dadurch verbessern sich die hämodynamischen Parameter und die Manifestationen eines Kreislaufversagens nehmen ab. Bei einer Überdosierung von Glykosiden treten charakteristische EKG-Anzeichen auf (Abb. 16), die je nach Schwere der Vergiftung entweder eine Dosisanpassung oder ein Absetzen des Arzneimittels erfordern. Bei Patienten mit einer Glykosidvergiftung kann es zu Übelkeit, Erbrechen und Unterbrechungen der Herzfunktion kommen. Reis. 16. EKG bei Überdosierung von Herzglykosiden Anzeichen einer Glykosidvergiftung: Verminderte Herzfrequenz; Verkürzung der elektrischen Systole; Vermindertes S-T-Segment nach unten; Negative T-Welle; Ventrikuläre Extrasystolen. Eine schwere Vergiftung mit Glykosiden erfordert das Absetzen des Arzneimittels und die Verschreibung von Kaliumpräparaten, Lidocain und Betablockern.


linksventrikuläre Myokardhypertrophie
 – Linksschenkelblock:
– Linksschenkelblock:
 – Rechtsschenkelblock:
– Rechtsschenkelblock:

 Verkürzung des PQ-Intervalls;
Verkürzung des PQ-Intervalls;

Bildung eines EKG beim WPW-Syndrom


 IHD (subepikardiale Ischämie, reziproke Veränderungen);
IHD (subepikardiale Ischämie, reziproke Veränderungen);
Pulsschlag Relative QT–Dauer
80%
90%
100%
110%
120%
130%
140%
Dauer des QT-Intervalls in ms
0,38
0,43
0,48
0,53
0,57
–
–
0,36
0,41
0,45
0,50
0,54
0,59
–
0,34
0,38
0,43
0,47
0,51
0,56
–
0,33
0,37
0,41
0,45
0,49
0,53
0,57
0,31
0,35
0,39
0,43
0,47
0,51
0,55
0,30
0,34
0,37
0,41
0,45
0,49
0,52
0,29
0,32
0,36
0,40
0,43
0,47
0,51
0,28
0,31
0,35
0,38
0,42
0,45
0,49
0,27
0,30
0,34
0,37
0,41
0,44
0,47
0,26
0,29
0,33
0,36
0,39
0,43
0,46
0,25
0,29
0,32
0,35
0,38
0,41
0,45
0,25
0,28
0,31
0,34
0,37
0,40
0,43
0,24
0,27
0,30
0,33
0,36
0,39
0,42
0,23
0,26
0,29
0,32
0,35
0,37
0,40
0,22
0,25
0,28
0,30
0,33
0,36
0,39
0,21
0,24
0,27
0,29
0,32
0,34
0,37
0,20
0,23
0,26
0,28
0,31
0,33
0,36
0,20
0,22
0,25
0,27
0,30
0,32
0,35
–
0,21
0,24
0,26
0,29
0,31
0,33
–
0,20
0,23
0,25
0,27
0,29
0,32
Elemente eines normalen EKG
Es ist merkwürdig, dass im Ausland normalerweise das P-Q-Intervall genannt wird P-R.
Im EKG werden folgende Wellen unterschieden:
Ein Segment in einem EKG wird aufgerufen gerades Liniensegment(Isolinien) zwischen zwei benachbarten Zähnen. Die wichtigsten Segmente sind P-Q und S-T. Beispielsweise entsteht das P-Q-Segment aufgrund einer Verzögerung der Erregungsleitung im atrioventrikulären (AV-)Knoten.
Das Intervall besteht aus Zahn (Zahnkomplex) und Segment. Somit ist Intervall = Zahn + Segment. Am wichtigsten sind die P-Q- und Q-T-Intervalle.
Achten Sie auf große und kleine Zellen (mehr dazu weiter unten).QRS-Komplexwellen

EKG-Analyse

Bei einer Bandgeschwindigkeit von 25 mm/s: HR = 300 (Anzahl der großen Quadrate).
Die Quelle der Erregung liegt in Sinusknoten. Anzeichen im EKG:
Um die Leitfähigkeit richtig zu berücksichtigen, wird die Aufzeichnungsgeschwindigkeit berücksichtigt.
Im ersten Teil der EKG-Reihe wurde erklärt, was die elektrische Achse des Herzens ist und wie sie in der Frontalebene bestimmt wird.
Normalerweise befindet sich in den Ableitungen I, II, aVF, V2 – V6 die P-Welle immer positiv. In den Ableitungen III, aVL, V1 kann die P-Welle positiv oder zweiphasig sein (ein Teil der Welle ist positiv, ein Teil ist negativ). Bei Lead-aVR ist die P-Welle immer negativ.

Eine Verlängerung dieses Intervalls tritt auf, wenn die Impulsleitung durch den Atrioventrikularknoten beeinträchtigt ist ( atrioventrikulärer Block, AV-Block).
Sollte beinhalten:
EKG-Interferenz

a) Einschaltströme: Netzwerkabholung in Form regelmäßiger Schwingungen mit einer Frequenz von 50 Hz, entsprechend der Frequenz des elektrischen Wechselstroms in der Steckdose.
B) " Baden„(Drift) der Isolinie aufgrund schlechten Kontakts der Elektrode mit der Haut;
c) Störungen verursacht durch Muskelzittern(unregelmäßig häufige Vibrationen sind sichtbar).Patienten wollen wissen...

Herzfähigkeiten
Bioströme im Herzen können aufgezeichnet werden
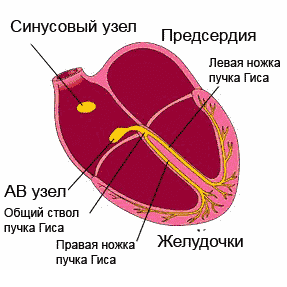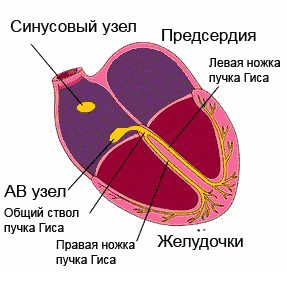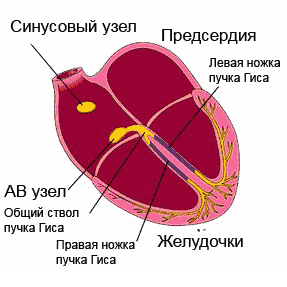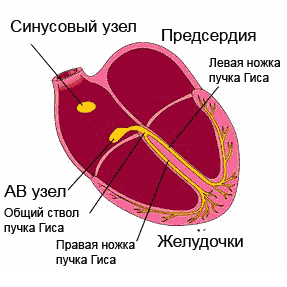 Aufregung macht sich breit Leitungssystem, deckt nacheinander die Teile des Herzens ab. Ausgehend vom Sinusknoten (der Wand des rechten Vorhofs), der maximale Automatizität aufweist, verläuft der Impuls durch die Vorhofmuskulatur, den Atrioventrikularknoten, das His-Bündel mit seinen Beinen und wird zu den Ventrikeln geleitet, die Teile stimulieren des Reizleitungssystems bereits vor der Manifestation seiner eigenen Automatizität.
Aufregung macht sich breit Leitungssystem, deckt nacheinander die Teile des Herzens ab. Ausgehend vom Sinusknoten (der Wand des rechten Vorhofs), der maximale Automatizität aufweist, verläuft der Impuls durch die Vorhofmuskulatur, den Atrioventrikularknoten, das His-Bündel mit seinen Beinen und wird zu den Ventrikeln geleitet, die Teile stimulieren des Reizleitungssystems bereits vor der Manifestation seiner eigenen Automatizität.Wie wird ein EKG erstellt?

Zähne, Ableitungen, Intervalle


Video: Lektion zu EKG-Wellen, Segmenten und Intervallen
EKG-Analyse

Die enttäuschendste Diagnose: Herzinfarkt


Video: Anzeichen eines Herzinfarkts im EKG
Wenn mit deinem Herzen etwas nicht stimmt

Video: Herzhypertrophie im EKG

Video: Arrhythmien im EKG


Video: EKG-Blockaden
Video: Schenkelblock im EKG
Holter-Methode
 HM ECG – was ist das denn für eine Abkürzung, so unverständlich? Dies ist die Bezeichnung für die langfristige und kontinuierliche Aufzeichnung eines Elektrokardiogramms mit einem tragbaren tragbaren Tonbandgerät, das das EKG auf Magnetband aufzeichnet (Holter-Methode). Eine solche Elektrokardiographie dient der Erkennung und Registrierung verschiedener Störungen, die periodisch auftreten, sodass ein normales EKG sie nicht immer erkennen kann. Darüber hinaus kann es zu bestimmten Zeitpunkten oder unter bestimmten Bedingungen zu Abweichungen kommen. Um diese Parameter mit der EKG-Aufzeichnung zu vergleichen, führt der Patient daher sehr viel durch ausführliches Tagebuch. Darin beschreibt er seine Gefühle, zeichnet die Ruhe-, Schlaf-, Wachheits- und jede aktive Aktivität auf und notiert die Symptome und Manifestationen der Krankheit. Die Dauer einer solchen Überwachung hängt jedoch vom Zweck ab, für den die Studie verordnet wurde, da die Aufzeichnung eines EKGs während des Tages jedoch am häufigsten vorkommt, heißt es Tagegeld, obwohl moderne Geräte eine Überwachung von bis zu 3 Tagen ermöglichen. Und ein unter die Haut implantiertes Gerät dauert noch länger.
HM ECG – was ist das denn für eine Abkürzung, so unverständlich? Dies ist die Bezeichnung für die langfristige und kontinuierliche Aufzeichnung eines Elektrokardiogramms mit einem tragbaren tragbaren Tonbandgerät, das das EKG auf Magnetband aufzeichnet (Holter-Methode). Eine solche Elektrokardiographie dient der Erkennung und Registrierung verschiedener Störungen, die periodisch auftreten, sodass ein normales EKG sie nicht immer erkennen kann. Darüber hinaus kann es zu bestimmten Zeitpunkten oder unter bestimmten Bedingungen zu Abweichungen kommen. Um diese Parameter mit der EKG-Aufzeichnung zu vergleichen, führt der Patient daher sehr viel durch ausführliches Tagebuch. Darin beschreibt er seine Gefühle, zeichnet die Ruhe-, Schlaf-, Wachheits- und jede aktive Aktivität auf und notiert die Symptome und Manifestationen der Krankheit. Die Dauer einer solchen Überwachung hängt jedoch vom Zweck ab, für den die Studie verordnet wurde, da die Aufzeichnung eines EKGs während des Tages jedoch am häufigsten vorkommt, heißt es Tagegeld, obwohl moderne Geräte eine Überwachung von bis zu 3 Tagen ermöglichen. Und ein unter die Haut implantiertes Gerät dauert noch länger.Video: Arzt über Holter-Überwachung
Fahrrad und EKG

Was ist Phonokardiographie?

Vor der Analyse von R-Wellen-Änderungen ist es notwendig, sich an mehrere theoretische Rahmenbedingungen zu erinnern, die zum Verständnis der Entstehung der ventrikulären Aktivierung in den präkordialen Ableitungen erforderlich sind. Die ventrikuläre Depolarisation beginnt normalerweise in der Mitte der linken Seite des interventrikulären Septums und bewegt sich nach vorne und von links nach rechts. Dieser anfängliche Vektor elektrischer Aktivität erscheint in den rechten und mittleren Brustableitungen (V1-V3) als kleine R-Welle (genannt „ Septumwelle r").
Ein geringfügiger Anstieg der R-Welle kann auftreten, wenn der anfängliche Depolarisationsvektor an Stärke abnimmt oder nach hinten gerichtet ist. Sobald das Septum aktiviert ist, dominiert die linksventrikuläre Depolarisation den Rest des Depolarisationsprozesses. Obwohl die Depolarisation des rechten Ventrikels gleichzeitig mit der des linken auftritt, ist ihr Ausmaß im Herzen eines normalen Erwachsenen vernachlässigbar. Der resultierende Vektor wird von den Ableitungen V1–V3 geleitet und erscheint als tiefe S-Wellen im EKG.
Normale Verteilung der R-Zacken in den präkordialen Ableitungen.
In Ableitung V1 werden ventrikuläre Komplexe durch den rS-Typ mit einer stetigen Zunahme der relativen Größe der R-Wellen zu den linken Ableitungen und einer Abnahme der Amplitude der S-Wellen dargestellt. Die Ableitungen V5 und V6 weisen typischerweise einen qR-Typ auf komplex, wobei die Amplitude der R-Zacken in V5 höher ist als in V6 Signaldämpfung durch Lungengewebe.
Zu den normalen Variationen gehören schmale QS- und rSr“-Muster in V1 sowie qRs- und R-Muster in V5 und V6. Ab einem bestimmten Punkt, normalerweise bei V3 oder V4, beginnt der QRS-Komplex von überwiegend negativ zu überwiegend positiv zu wechseln und das R/S Verhältnis wird > 1. Diese Zone wird als „ Übergangszone
". Bei einigen gesunden Menschen ist die Übergangszone bereits bei V2 zu erkennen. Dies wird als " bezeichnet. frühe Übergangszone
". Manchmal kann sich die Übergangszone bis V4-V5 verzögern, das nennt man " späte Übergangszone
", oder " Verzögerung der Übergangszone
".
In der Literatur gibt es verschiedene Definitionen für einen geringen Anstieg der R-Zacken, Kriterien wie zR-Wellen weniger als 2–4 mm in den Ableitungen V3 oder V4und/oder das Vorhandensein eines umgekehrten Wachstums der R-Welle (RV4< RV3 или RV3 < RV2 или RV2 < RV1 или любая их комбинация).
Es wird davon ausgegangen, dass die AnwesenheitR-Welle in Ableitung I<= 4,0 мм или зубцов R в отведении V3 <= 1,5 мм, указывает на старый передний инфаркт миокарда.

Akuter vorderer MI
Am häufigsten wird ein unzureichendes Wachstum der R-Wellen durch die hohe Platzierung der rechten Brustelektroden verursacht. Wenn die Elektroden jedoch in ihre normale Position gebracht werden, wird das normale Wachstum der R-Zacken wiederhergestellt Bei einem alten vorderen Myokardinfarkt bleiben die QS-Komplexe erhalten
.
Leider erwiesen sich diese Kriterien als wenig brauchbar für die Diagnose und führten zu vielen falsch-negativen und falsch-positiven Ergebnissen.
Verweise.