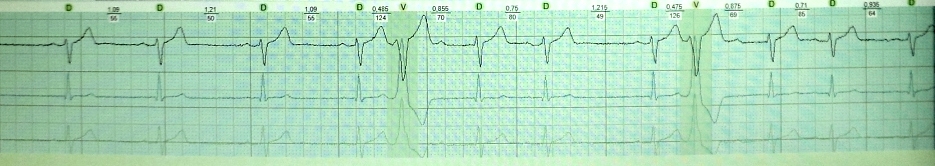
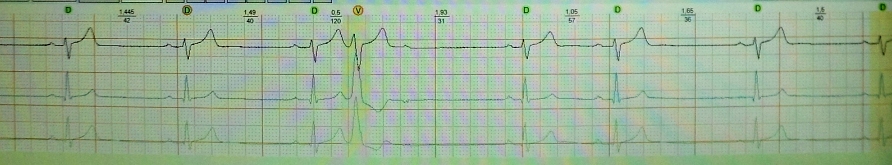
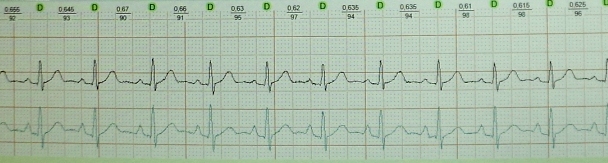
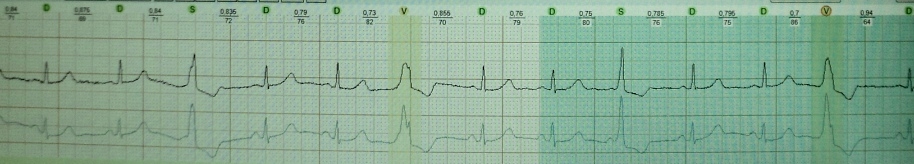
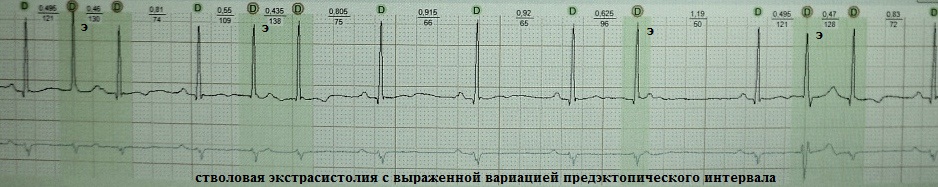
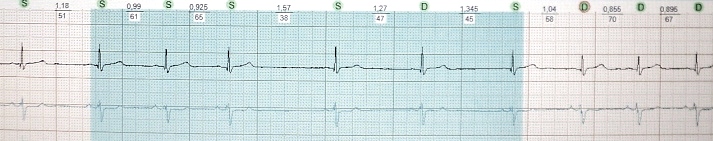
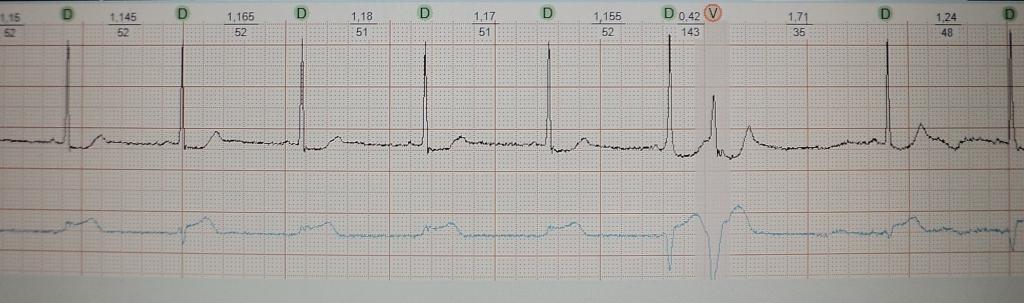
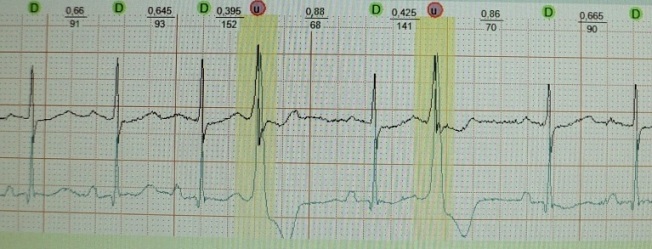
v1 v3 では r 波の成長が不十分です。 高齢者における心電図診断の特徴。 心電図の取り方
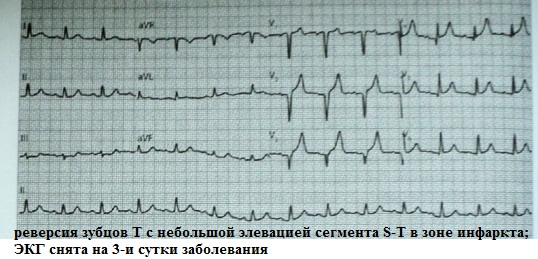
偽陰性ECGダイナミクスの発現として、急性心筋梗塞患者における陰性T波の復帰。
ケッカー症候群は、心筋梗塞の 2 ~ 5 日目に発生します。 再血栓症および左心室不全の臨床徴候の出現(増強)とは関連していません。 言い換えると、 これは再発ではありません心筋梗塞。 ケッカー症候群の期間は、原則として3日を超えません。 その後、ECG 画像は元の画像に戻り、T 波は陰性または等電性になります。 この ECG パターンの理由は不明です。 私は、これが心膜炎の症状であるという観点に感銘を受けました。 ただし、この症候群では特徴的な心膜痛は観察されません。 ケヒカー症候群を正しく解釈すれば、血栓溶解療法や PCI などの不必要な医療介入を避けることができます。 有病率: 心筋梗塞の 50 件に 1 件程度。
(同義語:記憶現象) - 長期にわたる人工(人工)右心室刺激中に現れる、自発収縮における心室複合体の最終部分(主にT波)の非特異的変化。

心室の人工的な刺激には、心室の収縮の形状の違反が伴います。 多かれ少なかれ長期的な刺激(2 ~ 3 か月)により、QRS 群の変化が、多くの ECG リードで負の T 波の形で自発収縮として現れることがあります。 このようなダイナミクスは虚血性変化をシミュレートします。 一方、本当に狭心症のような痛みが存在する場合、この現象により小限局性心筋梗塞を診断することがほとんど不可能になります。 シャテリエ現象を正しく解釈すれば、不必要な入院や不当な医療介入を避けることができます。
シャテリエ現象は、心臓の長期にわたる人工刺激の背景だけでなく現れる可能性があることを理解することが重要です。これが主な理由ですが、唯一の理由ではありません。 束枝の慢性閉塞、頻繁な心室期外収縮、または WPW 現象により、正常な収縮における心室複合体の最後の部分も変化する可能性があり、陰性または低振幅の T 波が形成されます。
したがって、心室内インパルスの異常な伝導による心室収縮の形状の長期的な乱れは、シャテリエ現象を伴う可能性があります。
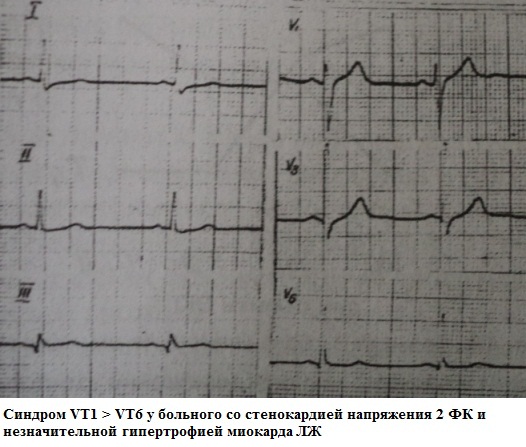
健康な人の ECG では、V6 の T 波の振幅は常に V1 の T 波の振幅よりも約 1.5 ~ 2 倍大きいことが注目されています。 また、V1 の T 波の極性は関係ありません。 V1 と V6 の T 波の振幅が「均等になる」、またはで V1 が V で T を超える6は標準からの逸脱です。 この症候群は、高血圧症 (LV 心筋肥大の初期の兆候である場合もあります) および冠状動脈疾患のさまざまな臨床形態で最もよく観察されます。 また、ジギタリス中毒の初期の兆候である可能性もあります。
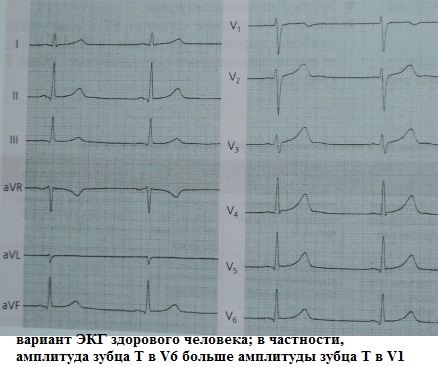


この症候群の臨床的重要性により、「正常ではない」ことを疑い、必要に応じて「単純なものから複雑なものまで」診断検索を続けることができます。
ほとんどの場合、「右」胸部誘導の R 波の振幅は増加し、V3 誘導までに少なくとも 3 mm に達します。 V3 の R 波の振幅が 3 mm 未満の状況では、V1 から V3 への R 波の成長が不十分であるという症候群について話すのが合理的です。 この症候群は 2 つのカテゴリに分類できます。
1. ECG 上に他の異常はありません。
標準の変形 (過敏体質の場合に多くみられます)、
LV心筋肥大の兆候、
胸部電極 (V1 ~ V3) が上の肋間腔に正しく配置されていない。
2. ECG に他の異常がある。
以下のような臨床状況に典型的です。
- 進行中の心筋梗塞(この場合、心臓発作に特徴的な V1 ~ V3 誘導の ECG ダイナミクスが存在します)、
梗塞後の心硬化症、
他のECG肥大基準を伴う重度のLV心筋肥大、
LBPの遮断(完全または不完全)、LBPの前枝の遮断、
- S 型の右心室肥大 (まれ)。




V1 から V3 への R 波の不十分な成長症候群を解釈することは、原則として、独立した無症候性の ECG パターンとして診断され、他の ECG 異常がない場合に生じます。 胸部電極が正しく適用され、心臓病歴がない場合、その主な原因は左室心筋の中程度の肥大です。
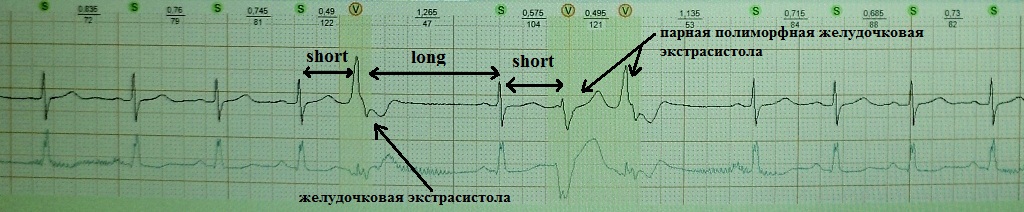
ご存知のように、心臓の期外収縮は期外収縮と呼ばれます。 余励磁結合間隔が短くなります( 短い)本陣痛の間隔。 これに代償的な一時停止が続きます ( 長さ)、これは心臓不応性の延長とその分散(不応性分散)の増加を伴います。 ちなみに、期外収縮後の洞収縮の直後には、再度期外収縮が起こる可能性があります( 短い) - 耐火性分散の「生成物」。 「繰り返される」期外収縮のメカニズム: 再突入または脱分極後の早期。 例:
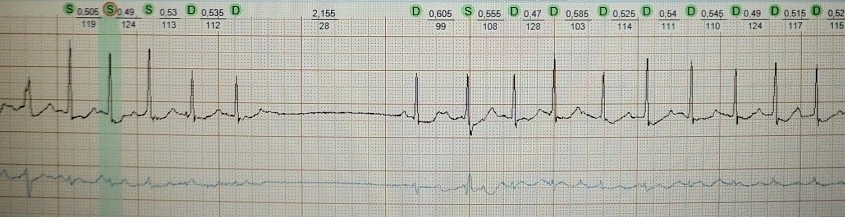
機能的徐脈依存性期外収縮を伴う患者における短-長-短。この場合、特別な臨床的意義はありません。
重度の睡眠時無呼吸症候群、肥満、ステージ 3 の高血圧を患う患者におけるショート-ロング-ショート。 見てわかるように、代償性休止の後、一対の多形性心室期外収縮が現れました。 この患者では、短長短現象が多形性心室頻拍を引き起こし、突然死につながる可能性があります。
QT延長症候群患者における短-長-短:「ピルエット」タイプの心室頻拍の誘発。 この症候群では、短長短現象が心室頻拍性不整脈の開始の前提条件となる場合があります。
機能性期外収縮の患者では、短長短現象は臨床的に重要ではありません。 それは徐脈依存性の期外収縮の発生を「促進」するだけです。 重度の器質性心疾患やチャネル障害のある患者では、この現象が生命を脅かす心室不整脈を引き起こす可能性があります。
この用語は、心周期において、時期尚早の衝動の伝導が不可能になる(または遅くなる)期間を指しますが、時期尚早の衝動の少ない衝動は伝導されます。 心臓伝導系のさまざまなレベルにおける不応性の違いが、この現象の電気生理学的基礎を提供します。
最初の ECG では、早期の心房期外収縮が異常なく心室に達していることがわかります。 2 回目の ECG では、心房期外収縮の結合間隔は長くなりますが、期外収縮は遅れて心室に伝わります (異常)。
ほとんどの場合、「ギャップ」現象は心臓電気生理学を行う専門家によって遭遇されます。
- 短周期異常(第 3 相ブロック)。これは、以前の 2 つの収縮の間の間隔が突然延長したために、AV 接続の不応期が増加したときに発生します。 収縮の間隔が長ければ長いほど、次の上室性衝動の異常伝導(またはブロック)の可能性が高くなります。
心房細動におけるアッシュマン現象の典型的な例:
アシュマン現象は、期外収縮後の代償性休止後に発生します。
洞収縮の間隔が自然に延長した後に起こる心房性期外収縮のブロック:
アシュマン現象の臨床的重要性: その正しい解釈により、a) 心室期外収縮および b) 房室接合部の器質的伝導障害の過剰診断を回避できます。
発作性心房細動が継続的に再発し、1回の発作が終わった後、1~2回の副鼻腔収縮後に新たな発作が始まります。
迷走神経依存性心房細動の特徴。 一方では、この現象は肺静脈の筋肉結合の高い異所性活動を反映し、他方では心房心筋の高い細動準備状態を反映している。
心房の逆行性興奮に加えて、放電に伴って心室衝動が房室接合部にさまざまな深さまで浸透する可能性があります(不応性の延長、遮断)。 その結果、後続の上室性衝動(通常は 1 ~ 3)が遅延(異常)するか、ブロックされます。
PVC による隠れた VA 伝導により、ステージ 1 の機能的な AV ブロックが引き起こされます。
PVC による隠れた VA 伝導により、ステージ 2 の機能的な AV ブロックが引き起こされます。
PVC による隠れた VA 伝導。位置決め後の (変位した) 代償休止を伴います。

隠れた房室伝導の臨床的重要性: この現象を正しく解釈することで、機能的な房室遮断と器質的な房室遮断を区別することができます。
ほとんどの人では、房室結節は均一です。 いくつかの場合、AV結節は電気生理学的に速い伝導ゾーンと遅い伝導ゾーンに分かれています(解離しています)。 人が主観的に健康であれば、この現象は臨床的に重要ではありません。 しかし、患者によっては、房室結節の解離に伴って結節性逆房房室頻拍の発作が発生することもあります。 頻脈の引き金は上室性期外収縮であり、これは速い経路に沿って実行され、遅い経路に沿って逆行性にのみ移動します - 再突入ループは閉じています。 房室結節解離の現象は、心臓電気生理学によって確実に確立されています。 ただし、定期的な心電図によって解離性疾患の兆候が検出される場合があります。
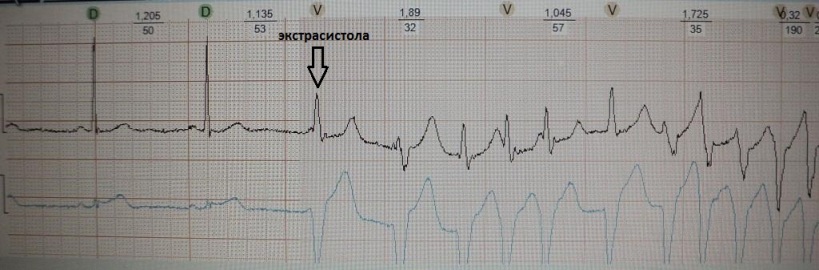
次の臨床例を考えてみましょう。 30歳の女性患者は、やる気のない動悸の発作を訴えています。 毎日の心電図モニタリングを実施した。
ECG の断片 - 正常なバリエーション:
ECG フラグメント - 第 1 段階の AV ブロック。 洞性頻脈を背景にしている - まったく標準的ではありません。
ECG フラグメント - 第 2 段階 AV ブロック、タイプ 1。P-R 間隔の「急速な」延長とそれに続く心室波の損失に注目してください。
P-R 間隔が 80 ミリ秒を超えて突然増加すると、AV 結節が異なるインパルス伝導速度を持つゾーンに分離することが考えられます。 これがこの例で見られることです。 その後、患者は心臓電気生理学的検査を受け、房室結節逆性頻脈が確認されました。 房室結節の緩徐経路の切除が実施され、良好な臨床効果が得られた。
したがって、表面 ECG 上の AV 結節解離の兆候 (正常な P-R 間隔と延長された P-R 間隔の交互; ヴェンケバッハ周期で 80 ミリ秒を超える P-R 間隔の 1 回の増加) と不整脈の病歴を組み合わせると、次のことを確立することが可能になります。心臓電気生理学的検査の前であっても、高い確率で診断されます。
この現象は一見信じられないような性質を持っていますが、それほど珍しいことではありません。 ケント束は、心房から心室にインパルスを伝導するための追加の経路として機能するだけでなく、自動化(自発的な拡張期脱分極)も可能です。 ケント束からの期外収縮は、ECG 上で WPW 現象の兆候が拡張後期期外収縮と組み合わされ、心室期外収縮をシミュレートする場合に疑われる可能性があります。 この場合、拡張された心室複合体は連続的なデルタ波を表します。
次の臨床例を考えてみましょう。 42歳の女性が、やる気のない動悸の発作を訴えました。 2日間のECGモニタリングを実施した。 研究の初日には、約500個の「拡張した」心室複合体が記録され、拡張期後期に出現し、心拍数の増加とともに消失した。 一見すると、無害な機能的な心室期外収縮です。 しかし、拡張期後期の心室期外収縮はカルシウム依存性であり、主に頻収縮を背景に、または頻収縮の終了直後に現れます。 この場合、後期心室収縮は正常な心拍数と徐脈で記録されますが、それ自体が奇妙です。
状況はモニタリングの 2 日目に完全に明らかになり、断続的な心室前興奮の兆候が現れました。 拡張後期の心室複合体はケント束からの期外収縮にすぎないことが明らかになりました。
ケント束からの期外収縮の臨床的重要性: この現象を正しく解釈することで、心室期外収縮の診断を除外し、診断と治療のプロセスを必要な方向に導くことができます。
これは、上室性頻脈性不整脈、特に心房細動で観察されます。 この現象の本質は、上室インパルスが房室接合部に頻繁かつ不規則に到達し、さまざまな深さまで浸透することです。 心室に到達せずに排出します。 その結果、1)後続の上室性衝動の伝導が遅くなり、2)置換異所性衝動が遅くなる(脱落する)。
表面 ECG では、隠れた AV 伝導現象は次の兆候に基づいて示されます。
心房細動における短い R-R 間隔と長い R-R 間隔の交互変化:
過度に長い間隔で避難施設を設置しない R-R 心房細動の場合:
洞調律が回復したときの数秒間の休止中に逃避複合体が存在しない場合:
規則的な心房粗動が不規則または心房細動に移行すると、次のことが起こります。
房室接合部遠位部(ヒス束幹)からの期外収縮は心室期外収縮の一種であり、「幹」と呼ばれます。 私がこのタイプの期外収縮を不整脈現象と呼んでいるのは、第一にその比較的まれな理由、第二に典型的な頭頂部心室期外収縮との外観の類似性、そして第三に従来の抗不整脈薬に対する抵抗性のためです。
体幹部期外収縮の臨床的および心電図的兆候: 1) QRS 群は、しばしば上室の外観を示すか、または散発性の異常または束枝の 1 つの近位部分への近接によりわずかに広がっています。 2) 心房の逆行性活性化は典型的ではありません。 3)期外収縮病巣の脳幹局在化はカルシウム依存性の脱分極、すなわち異常な自動症を示唆するため、結合間隔は可変である。 4) クラス I および III 抗不整脈薬に対して絶対的な抵抗性。
例:
体幹部期外収縮では、クラス II または IV の抗不整脈薬を長期間使用する場合にのみ良好な臨床効果が得られます。
- 予想される遮断ではなく衝動を引き起こす(異常)。
例 #1:
考えられるメカニズム: 心房インパルスが超常相で LAP を捉えた。
例2:
考えられるメカニズム: ヒス・プルキンエ系における自発拡張電位の大きさは、「洞」収縮の再分極終了直後に最大になります (この場合、洞収縮はLBP遮断により拡張されます)。したがって、初期の心房インパルスが最大の可能性を持っています。 「通常の」伝導の。
例 #3 (逆アッシュマン現象):

考えられるメカニズム: 伝導における「ギャップ」(障害) の現象。 前のサイクルの長さが変化すると、不応性が短縮されます。
ECG 上の突然の洞停止は、常に明確に解釈できるわけではありません。 場合によっては、現象を正しく解釈するには、心電図自体の徹底的な分析に加えて、包括的な臨床評価および既往歴の評価が必要になります。 例:
洞性不整脈中の一時停止は非常に顕著であるため、SA 遮断の存在について誤解が生じることがあります。 洞性不整脈は無症状であることを覚えておく必要があります。 主観的には健康な人を含む、主に若年者と中年者に典型的です。 徐脈(通常は夜間)を伴って出現(激化)します。 休止自体は長すぎることはなく、それによって滑る複合体の出現を引き起こすことはありません。 心臓神経症状は一般的な臨床症状です。
第2度洞房ブロック:

1次または2次の封鎖の種類を調べる必要があります。 予後が異なるため、これは根本的な問題です。 SA 遮断、ステージ 2、タイプ 1 は、若い健康な人の安静時 (特に夜間) に起こることがよくあります。 古典的な場合、臨床的にも心電図的にも、ウェンキバッハの定期刊行物が先行します。 原則として、一時停止の長さは、以前の収縮の R-R 間隔の 2 倍を超えません。 滑り複合体の存在は一般的ではありません。 失神の既往はない。

SA 封鎖、ステージ 2、タイプ 2 は、ウェンキバッハ周期性なしに突然現れます。 多くの場合、器質的心筋損傷が併発しており、機器によって検出されます。 高齢者の場合、ECHO中に心臓に明らかな変化が見られない場合、主な原因は心硬化症です。 一時停止は、以前の収縮の R-R 間隔の 2 倍より長くなる場合があります。 滑り複合体が頻繁に発生します。 失神歴または同等の病歴が典型的です。


ブロックされた心房期外収縮:
原則として、ブロックされた期外収縮の数が少なく、通常の(ブロックされていない)期外収縮の数が統計的標準を超えない場合にのみ診断が困難になります。これは医師の警戒心を鈍らせます。 ECG を分析するときに基本的なケアを行うことで、ブロックされた心房期外収縮を確実に確認できます。 私の経験では、非常に早期にブロックされた異所性 P 波は常に T 波をある程度変形させるため、EPI なしでこの現象を診断することが可能になります。
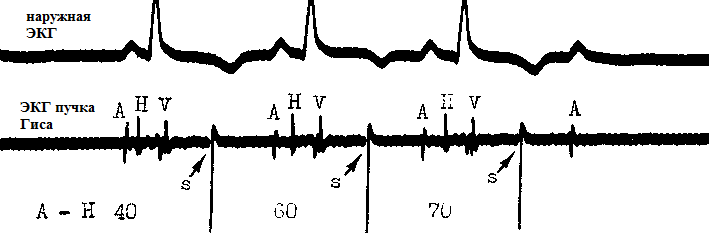
このセクションで隠れた期外収縮について言及しますが、私はこの現象の極めて異常な点に敬意を表します。 私たちは、前行性および逆行性の伝導が遮断される幹性期外収縮について話しています。 したがって、表面心電図には表示されません。 その診断はヒス束心電図検査でのみ可能です。 上の図では、幹性期外収縮が人為的に誘発されます: 刺激 S. ご覧のとおり、S 刺激は AV 接合部を超えて拡張されないため、ECG 上には表示されません。 3 番目に加えられた刺激は、一過性の第 2 度房室ブロック (") を引き起こします。外部 ECG では、従来の (有線) 房室期外収縮と第 2 度房室ブロックと同様の突然の心臓停止の組み合わせがある場合、隠れた脳幹期外収縮が疑われる可能性があります。
未熟児の増加に伴う異常は誰も驚かない - 伝導系の不応性がまだ短縮する時間がない場合、心拍数の急速な増加に関連しているため。 心拍数が低下するとき、つまり不応期が明らかに終わったと思われるとき、この異常はさらに異常に見えます。

長周期異常の基礎は、ヒス・プルキンエ系の細胞が自発的に拡張期脱分極する能力にあります。 したがって、心臓の働きが一時停止すると、心臓の伝導系の一部の膜電位が静止電位の値(「臨界低分極」)に達し、速度が低下したり、心臓の活動が不可能になったりする可能性があります。次の衝動を導きます。 最初に房室接合部の細胞が低分極状態(最大拡張期電位の低い値)にある場合、このような状況はほとんどの場合、伝導系の器質的病理を反映していることを理解する必要があります。 徐脈依存性の遮断現象は、健康な心臓では典型的なものではなく、多くの場合、より重度の伝導障害に先行します。
文字通り、より頻繁な衝動によるペースメーカーの抑制を意味します。 この現象は、自動セルが自身の励起周波数よりも頻繁に活性化を受けるという事実による、自動セルの過分極に基づいています。 洞結節がすべての下位レベルのペースメーカーを抑制するとき、健康な人の心電図でこの生理現象を観察できます。 洞調律周波数が高いほど、期外収縮を含む異所性インパルスの可能性は低くなります。 一方、異所性焦点のインパルスの周波数が洞結節の自動性を超える場合、洞結節自体が超周波数抑制を受けます。 後者の事実は、洞調律の回復後の休止時間が過度に長くなる可能性があるため、医師の診察を受けることがよくあります。 例えば:
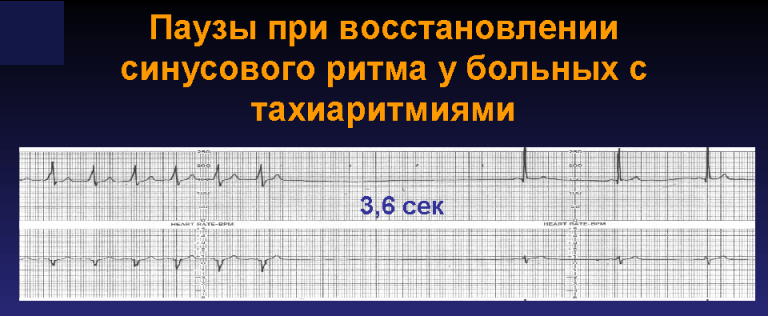

EPI では、「オーバードライブ抑制」現象を通じて洞結節の機能不全が検出されます。
初期は心室期外収縮 R on T 型、心房期外収縮 P on T 型と呼ばれます。
健康な人(特に心房の人)でもこのような期外収縮が発生する可能性は十分にありますが、期外興奮の時期尚早が短ければ短いほど、正常な心筋の場合には典型的ではないことを覚えておく必要があります。 したがって、初めて早期の期外収縮に遭遇した場合、心筋不応性の変動の存在、つまり期外収縮によって頻脈性不整脈が引き起こされる可能性を臨床的かつ機器的に評価する必要があります。 肺静脈の口の筋肉結合に起因する早期の心房性期外収縮は、中年の人で多くの場合検出され始めます。 ほとんどの場合、それは心臓外疾患の一部として反射機構によって現れます。 間違ったライフスタイル。 そして、不整脈の原因が除去されない場合、遅かれ早かれ早期の心房期外収縮が心房細動を引き起こし始めます。 初期の心房性期外拍、左心房拡張、および高血圧(または潜在性動脈高血圧)の組み合わせは、将来の心房性頻脈性不整脈の最も信頼できる臨床予測因子です。 高齢者では、ほとんどの場合、早期の心房期外収縮が記録されます。
生命を脅かす心室調律障害は、ほとんどの場合、R on T 現象によって引き起こされるため、早期心室期外収縮の臨床分析においては、医師の肩にはるかに大きな責任がかかっています。健康な人の場合、早期心室期外収縮は、速いリズムの背景。 速度が低下すると、拡張期中期になります。
正常または徐脈を背景とした孤立した R on T 現象は、その特殊な電気生理学的起源、つまり早期後脱分極に関して常に疑わしいものです。 知られているように、健康な心筋では、早期に脱分極が起こる条件はありません(特に心室心筋では)。 したがって、心筋への急性または慢性の器質的損傷の形での早期心室期外収縮の明白な原因が拒否された場合、他のもの、つまり先天性のものを除外する必要があります。 いわゆる電気的心臓病では、長期間にわたって早期の心室期外収縮が隠れた病状の唯一の症状である可能性があることを思い出してください。
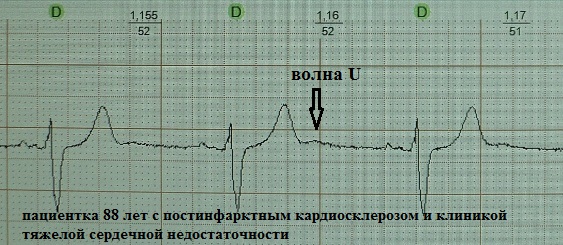
U波の起源についてはまだ統一見解がありません。 その臨床的意義については依然として議論の余地がある。 その起源にはいくつかの説があります。
1) U 波は、自身の活動電位に続く遅発電位によって引き起こされます。
2) U 波は、拡張期初期の心室の急速な充満期間中の心室の筋肉組織の伸張から生じる電位によって引き起こされます。
3) U 波は、拡張期に左心室の壁が伸びるときに遅延した後期再分極によって誘発される電位によって引き起こされます。
4) U 波は、乳頭筋またはプルキンエ線維の再分極によって引き起こされます。
5) U 波は、閉じた「動脈 - 静脈」回路に沿って通常の動脈拍動が通過した後、静脈の入り口で十分な強度の機械波によって引き起こされる電気振動によって引き起こされます。
したがって、すべての理論は、拡張期初期の心筋の膜内外電位差を低分極方向に一時的にシフトさせる特定の後期振動の存在に基づいています。 私は理論 2 に近いです。中程度に低分極した心筋は興奮性を高めます。知られているように、ECG 上の U 波は、心周期のいわゆる超正常相と時間的に一致します。この相では、たとえば、期外収縮が容易に発生します。
U 波の臨床的重要性は不明です (私の意見では、重要ではありません)。 通常、U 波は小さく (ECG 上で約 1.5 ~ 2.5 mm)、T 波の 0.02 ~ 0.04 秒後に続く、正の緩やかな傾斜の波で、誘導 V3、V4 で最もよく視覚化されます。 多くの場合、U 波はまったく検出されないか、T 波に「重なって」います。また、たとえば、心拍数が 95 ~ 100 拍/分を超える場合、心房と重なるため、U 波の検出はほとんど不可能です。 P 波 通常、健康な若者の振幅が最も大きいと考えられています。 ただし、理論的には、どのような臨床状況でも発生する可能性があり、頻収縮中に振幅が増加します。

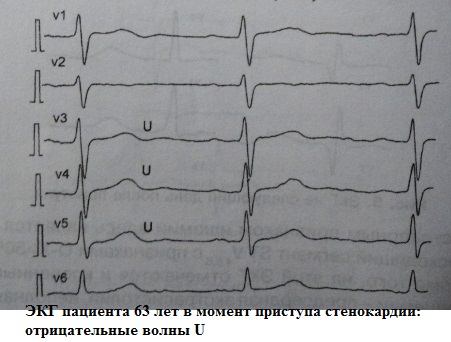
負の U 波は絶対に標準的なものではないと考えられています。 負の U 振動は、ほとんどの場合、何らかの病状に関連しています。 もう 1 つは、このような復帰の診断値はまったく異なる可能性があるということです。
心室調律の代替(「保存」)役割について話すのは、それが「発作性」SAまたはAV遮断中、または受動的AV解離中に心停止を背景に現れる場合にのみであることが正しい。 別の状況では、私たちは、あたかもやる気のない (「活動的」な) ように見える、加速された固有心室調律 (AVR) に対処しています。 その頻度が1分あたり110〜120回を超えない場合、心室頻拍と診断されます。 UIR が表示される理由はいくつかあります。
急性心筋梗塞における再灌流症候群、
左心室収縮機能の低下を伴う既知の器質性心疾患(悪性の可能性のある大型異所性疾患の一部として)、
ジギタリス中毒、
健康な人における特発性のケース。
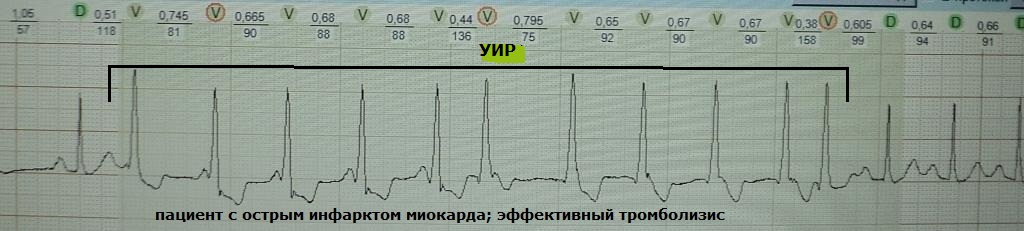
ほとんどの場合、URI は急性心筋梗塞の際、冠状動脈の完全または部分的な再開通時に発生します。 このような状況では、気絶した心筋細胞に大量のカルシウムが流入し、膜内外電位差が閾値レベルにシフトします(細胞低分極)。 その結果、心筋細胞は自動性の特性を獲得します。 URI は再灌流の成功の信頼できる基準ではないことを知っておくことが重要です。再開通は部分的または断続的である可能性があります。 しかし、他の臨床徴候と組み合わせると、冠血流の回復のマーカーとしての UIR の予後価値は非常に高くなります。 「再灌流」心室細動のケースは非常にまれです。 例:
再灌流症候群は、主に心臓集中治療室で働く病院の医師が遭遇します。 クリニックの心臓専門医や機能診断医は、URI の他の原因を扱うことが多くなります。
UID の原因としてのジギタリス中毒は、近年ますます一般的ではなくなりました。 ただ覚えておけばいいのです。
左心室収縮機能不全を背景とする器質性心疾患患者におけるUIRを同定することは、臨床的に非常に重要である。 このような状況における心室異所性は、悪性の可能性があるものとして扱う必要があります。特に運動後の回復期に発症した場合、心室細動の開始による心臓突然死のリスクが確実に高まります。 例:
10〜15年前でさえ、器質性心疾患のない人々にUIDを登録する際、心臓専門医は臨床予後が「不確実」であるとの評決を下しており、そのような被験者は医療の後援を受けていた。 しかし、それらの長期観察により、URI は心臓突然死のリスクを増加させず、そのような場合は「表面上の」不整脈であることが示されています。 健康な人の URI は、他の心臓異常や心臓以外の異常、つまり WPW 現象、副索、早期心室再分極症候群、症状と関連していることがよくあります。 結合組織異形成症候群。 URI の臨床的重要性は、不整脈の主観的な忍容性と心臓内の血行動態に対する不整脈の影響 (不整脈原性心臓拡張の発生の可能性) によって決定されます。 例:

医師は、心室複合体の周波数変動や多型などの URI パラメータによって混乱するべきではありません。 リズムの不規則性は、異所性中枢の内部自動作用、またはヴェンケバッハの周期性による出口の遮断によって決定されます。 異所性複合体の見かけのポリトピック性は、実際には、異常な興奮伝導に他なりません。 一般的なコンセンサスは、健康な人における URI のメカニズムは異常な自動性であるということです。
心室調律の加速の鑑別診断では、アッシュマン現象、WPW 現象、および頻脈または徐脈に依存する脚ブロックは除外される必要があります。
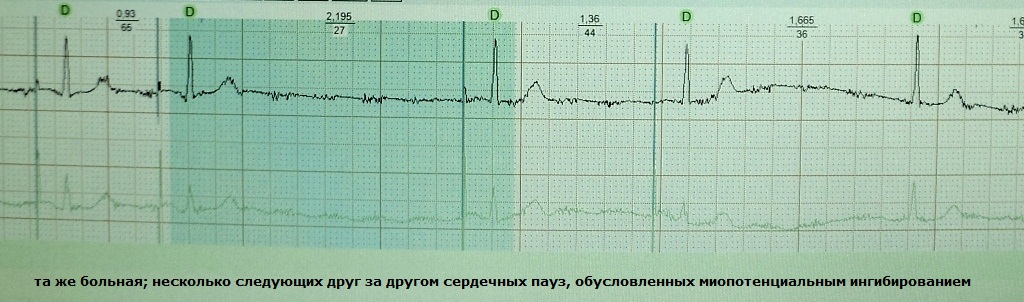
これは、胸部、肩帯、腹筋、または横隔膜の骨格筋の電位に対してペースメーカーを過敏に反応させることの一種です。 その結果、心外信号を感知した検出電極は、次の人工インパルスを抑制する指令を出し、心臓の停止が起こり、患者が失神する可能性があります。 一般に、筋電位抑制は、手を使った積極的な作業など、何らかの行為によって引き起こされます。 この現象は、単極電極構成のペースメーカーに特有の現象です。 近年、インプラントの移植はますます少なくなってきています。 例:
筋電位抑制を修正するためのオプション: 1) 電極の感度閾値を下げる、2) システムを双極バージョンの感知に再プログラムする、3) 電極を双極コアを備えた新しいものに交換する。
知られているように、デルタ波は、AV 結節のインパルス遅延特性のない追加の順行性伝導経路の存在による、心室前興奮の特定の兆候です。 デルタ波の形をしたよく知られた ECG 画像は、早期興奮により QRS 群が拡大し、P-Q 間隔が短縮され、WPW 現象と呼ばれます。 しかし、実際にはデルタ波が存在しないが、その始まりが前興奮に非常に似ている心室期外収縮が存在する場合に、デルタ波を検出したいという「誘惑」が起こることがあります。 これがいわゆる擬似デルタ波です。 このような心室複合体は、連続デルタ波(同義語:連続逆行伝導、ケント束からの期外収縮)を模倣します。 疑似デルタ波を伴う心室期外収縮が標準 ECG に記録されると、診断が困難になります。 長期にわたる ECG モニタリングを分析すると、ケント束からの期外収縮を伴う WPW 現象 (実線のデルタ波) がすべて適切に当てはまります。 いつも真のデルタ波を伴う心室複合体の存在と組み合わされます。 逆に、疑似デルタ波で心室期外収縮を記録すると、WPW 現象の古典的な兆候 (断続的な前興奮を含む) は検出されません。 例:
疑似デルタ波の「幅」によって、期外収縮病巣の位置が心内膜か心外膜であるかを判断できます。 アルゴリズムは次のとおりです。1) 疑似デルタ波が 50 ms を超える場合は、PVC の心外膜起源について話すことができます。2) 疑似デルタ波が 50 ms 未満の場合は、注意を払います。 12 チャネル ECG での期外収縮の最短 RS 間隔までの 115 ms 未満の持続時間は、病巣が心内膜に局在していることを示しますが、115 ms 以上の持続時間では、第 3 のステップ、つまり心臓の存在を示します。 aVL 誘導における q 波、3) aVL 誘導における q 波の存在は PVC の心外膜起源を示し、その欠如 - 心内膜について。 たとえば、以下の ECG では、最も大まかな計算によっても、疑似デルタ波の幅は 50 ミリ秒を超えています。
期外収縮病巣の局在化は、侵襲性不整脈専門医だけでなく興味深いものです。心外膜期外収縮が頻繁に起こると、不整脈原性心臓拡張のリスクがはるかに高くなります。
. 心拍数が頻繁になると、心筋のエネルギー資源が動員されます。 頻収縮のエピソードがあまりにも長く続くか、心拍数が非常に高い場合、細胞内代謝が破壊され(負荷に対処できなくなり)、一過性の心筋ジストロフィーが形成されます。 このような場合、頻脈の終了後に、頻脈後症候群と呼ばれる再分極の非特異的変化が ECG 上で検出されることがあります。 理論的には、回復期に頻脈(洞、上室、または心室)が発生した後、頻脈後症候群の症状が現れる可能性があります。 古典的な形式では、前胸部誘導における TV 波の一時的な反転を表します。 ただし、実際の経験では、頻脈後の ECG 変化は S-T セグメントにも影響を与える可能性があることを示しています。 したがって、臨床現場では、次のような頻脈後症候群の症状が現れます。
上に凸のS-Tセグメントの斜め上行性の窪み(「収縮期過負荷」のような)、
- S-T セグメントの「ゆっくりとした」斜め上向きのくぼみ、
マイナスのT波。
後頻脈症候群の持続期間は、数分から数日まで、予測できないほど変化します。 交感神経緊張が持続すると、頻脈後症候群の症状が何か月から何年も続くことがあります。 典型的な例は、精神が不安定な青年や若者に特徴的な若年型の心電図(V1~V3誘導の陰性T波)です。
頻脈後症候群の選択肢を簡単に考えてみましょう。
頻脈後に上向きに凸になったS-Tセグメントの斜めの陥没は、原則として、左心室心肥大の初期症状を示す個体に形成されます。 このような患者では、標準的な安静時 ECG のパラメータは完全に正常です。 最も顕著な低下は V5、V6 誘導で観察されます。 その外観は誰もがよく知っています。

原則として、頻脈の発症後 1 時間以内に ECG は正常に戻ります。 心筋肥大が進行すると、S-Tセグメントの正常化が数時間または数日遅れ、その後、収縮期過負荷の症状が安静時に「固定」されます。
S-T セグメントの「ゆっくりとした」斜め上行性のくぼみはまれです。 ほとんどの場合、それはNCDタイプの機能性心筋障害を背景に頻脈の後に現れます。

陰性 T 波は、頻脈後症候群の最も一般的な変種です。 極めて非具体的です。 3つの例を挙げます。
持続的な交感神経緊張を背景とした、21 歳の少年の前胸部誘導における陰性 T 波 (若年型の ECG と考えられます):

心室頻拍後に形成される前胸誘導の陰性 T 波:
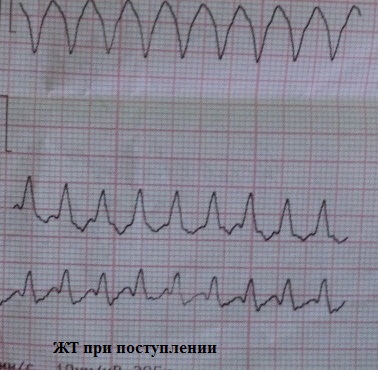
上室性頻拍後に形成される前胸部誘導の陰性 T 波:
臨床的な意義 頻脈後症候群はすごいよ!不必要な入院や健康診断の一般的な原因です。 特に虚血性変化をシミュレートすることにより、 心臓症候群、頻脈後症候群は冠状動脈の病状を「模倣」する可能性があります。 彼のことを覚えていてください! 診断も頑張ってください!
約 2/3 の人では、左脚枝が 2 つの枝に分岐するのではなく、前方、後方、後方の 3 つに分岐します。 中央値。 正中枝に沿って、電気的興奮はIVSの前部および左心室の前壁の一部にまで広がります。
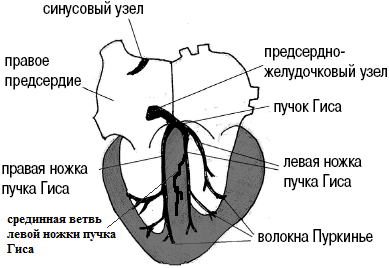
その孤立した封鎖は非常にまれな出来事です。 しかし、それが起こると、IVSの一部と左心室の前壁が、左心室の後壁と側壁から異常に興奮します。 その結果、水平面では電気ベクトル全体が前方に向き、V1~V3誘導では高いR波(qR、R、Rsなどの複合体)の形成が観察されます。 この状態は次の状態と区別する必要があります。
WPW症候群
右心室肥大
後基底部心筋梗塞、
自然な理由で右心室の電位が優勢になる、生後数年間の子供の正常な心電図。
左脚の正中枝の閉塞は、機能的伝導障害の一部として発生する可能性があり、また、例えば、冠状動脈疾患の無症候性 ECG マーカーである前下行動脈のアテローム性動脈硬化病変を間接的に反映することもあります。
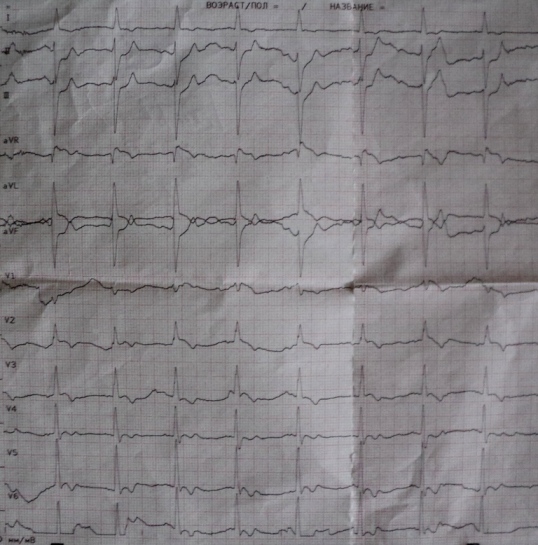

これらのセリフの作者は文字通り、職業上のキャリアの中で何度かこの伝導障害に遭遇しました。 そのような観察を一つ挙げておきます。 重度の胸痛のある患者では、次の ECG パターンが確認されました (図 A): aVL、V2、および V3 誘導における S-T セグメントの斜めの上昇。 前上半ブロックと左脚の正中枝のブロック(V2、V3誘導の高振幅R波)。 発作以外では、心電図は正常に戻りました(図B)。
冠動脈造影検査により、患者の中央 3 分の 1 に前下行動脈のけいれんが明らかになりましたが、硝酸塩の冠動脈内投与により解消されました。 同心性冠動脈アテローム性動脈硬化症は存在しなかった。 冠攣縮性狭心症と診断されました。 したがって、正中枝の遮断は狭心症発作の時にのみ現れ、「深い」心筋虚血を反映している。
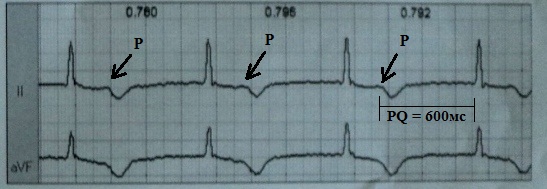
知られているように、 ペースメーカー症候群たとえば、心室心房伝導や不適切に長い房室遅延による、心房と心室の正常な収縮順序の慢性的な違反によって引き起こされる可能性があります。 またはその発現は以下に関連しています 自然な(自身の)心臓収縮と強制的な心臓収縮の血行力学的非同等性。
偽ペースメーカー症候群は、心室心房伝導または重度の第 1 度房室ブロックの存在によって引き起こされる血行動態障害であり、ペースメーカー症候群と同様の臨床症状を示しますが、心臓ペーシングは存在しません。 この「偽症候群」の発症は、心電図的に P 波が前の心室複合体の S-T 間隔と重なり始めるとき、350 ~ 400 ミリ秒を超える長期の第 1 度房室ブロックで最もよく観察されます。 この場合、心房収縮は僧帽弁が閉じていることを背景に発生します。
文学的な考察をしてみます。 この患者は、基本刺激周波数 50/分での DDDR モードでのペースメーカー植込み後 4 年後に非代償性 CHF の症状を訴えて来院しました。 ECGにより、第1度房室ブロックを伴う洞調律が明らかになった。 約600ミリ秒続きます:
心房刺激の全体的な割合は 5% を超えず、心室刺激の割合は 7% を超えませんでした。 ダイナミクスでは、心室の強制されたリズムまたは P 同期刺激のまれなエピソードが心室期外収縮によって中断され、その後に再び第 1 度の顕著な房室ブロックを伴う洞調律が続くことがわかりました。
このペースメーカーの動作アルゴリズムは、心室収縮後、450 ミリ秒の心房不応期がトリガーされ、P 波が心室収縮後約 200 ミリ秒で現れる、つまり非常に早いため検出されないというものでした。 これにより、心室刺激がほぼ完全に抑制されました。 この場合、心房不応期を短縮するか、完全な房室ブロックの発症を引き起こす必要がありました。 この患者は、心不全の基本的な治療に加えて、高用量のベラパミルを処方されました。これにより、房室伝導が遮断され、心室収縮が 100% 強制的に行われました (P 同期刺激)。 薬物のAV遮断が決定的な要因であることが判明しました。これにより、心房と心室の収縮の脱同期を排除することが可能になり、その後、心不全の症状が停止しました。
この例では、第 1 度の重度の房室ブロックがどれだけ長期間続いているかがわかります。 心不全の発症を引き起こす可能性があります。
偽ペースメーカー症候群では、「飛び跳ねる」P 波の現象が観察されることがあります ( Pスキップ)房室伝導の顕著な減速を背景に、P 波が QRS 群内で単に「溶解」するのではなく、QRS 群に先行する場合。
- 心室心房伝導がない場合の心室収縮の影響によるP-P間隔の長さの変化。 この不整脈は、正弦波 P の数が心室 QRS 群の数を超えた場合、つまり 2 度または 3 度の房室ブロックで発生すると考えられています。 この場合、QRS 群を含む P-P 間隔は、心室収縮のない P-P 間隔より短くなります。

同時に、 心室相洞性不整脈は、心室期外収縮や人工心室刺激により観察できます。 例えば:
この現象の最も可能性の高いメカニズムは、心室収縮期に心房が伸張し、 洞耳結節の機械的刺激.
近年、早期心室再分極症候群に対する臨床的および心電図的アプローチは大幅に変化しました。 専門家のコンセンサスによれば、臨床症状(多形性心室頻拍または心室細動の発作)がなければ、この症候群を正しく呼ぶことができます。 初期の心室再分極のパターン、したがって、無害な心電図異常の枠組み内での現在の良性が強調されます。 学期 症候群 RRGの使用を推奨しますのみ 心室頻脈性不整脈のメカニズムによる失神や心臓突然死を患う症状のある患者。 RGC 現象のこの経過が非常に稀であること (10,000 人に 1 人) を考慮すると、この用語の使用は パターン単なる優先事項ではなく、唯一の正しいものであると考えるべきです。
RGC パターンの診断基準はより厳格になりました。 S-T セグメントの凹状の隆起が RGC のマーカーの 1 つであると信じるのは間違いです。分析対象 R波の下降部分のみの変形: RJ パターンは、その上のノッチ (波 j) の存在またはその滑らかさを指します。 標準 ECG の 2 つ以上の連続する誘導 (aVR、V1 誘導を除く) の等値線 (レポート ポイントは P-Q 間隔の位置) からノッチの上部または滑らかさの始まりまでの距離は、少なくとも 1 mm でなければなりません。 -V3); QRS コンプレックスの幅は 120 ミリ秒未満である必要があり、QRS 持続時間は RR パターンが存在しない誘導でのみ計算されます。


上記の基準によれば、ECG No. 1 のみが RGC パターンを持ちます。
残念ながら、RGC パターンの潜在的な悪性度と症候群への移行の可能性について信頼できる基準はまだありません。 ただし、以下の臨床徴候が存在する場合、RGC パターンを持つ被験者は医療を受ける必要があります。
心拍数の変化がない場合の j ポイント上昇の動的変化、
「R to T」タイプの心室期外収縮の存在
血管迷走神経性失神(つまり、「突然床に座った」タイプの失神)とはおそらく臨床経過が異なる失神の存在。
RGCのパターンが記録されている45歳未満の一親等親族の原因不明の死亡、
ほとんどのリードに RGC パターンが存在する (aVR、V1 ~ V3 - 考慮されていない)、
波 j が水平または下向きの S-T セグメントに遷移します。
S-T セグメントの性質 (昇順、水平または降順) を判断するには、点 Jt の位置と、そこから 100 ミリ秒離れた S-T セグメント上の点が比較されます。
モビッツ II 型の第 2 度房室ブロックの検出は、ほとんどの場合、予後不良の兆候です。なぜなら、その存在は、第一に、房室結節より遠位の伝導障害を反映しており、第二に、より重度の房室結節の発症の前触れとして機能することが多いためです。降下機能不全、たとえば完全な房室ブロック。
同時に、実際の心臓病学では、第 2 度房室ブロックの重大な過剰診断が存在します。 モビッツⅡタイプ。 このようなブロック、いわゆる疑似モビッツ II (第 2 度の偽 AV ブロック、タイプ II) をシミュレートできる状況を考えてみましょう。
タイプ I の第 2 度房室ブロックを伴う長い房室結節周期。

迷走神経の緊張が突然一時的に増加します。
隠れた ;

心室期外収縮後。

症候群 W.PW;

心周期の再分極期中の心筋合胞体の隣接領域間の電位差。 健康な心筋では、不応性の分散は最小限であり、その臨床的意義はゼロになる傾向があります。 患者の心筋不応性の分散の存在について言えば、私たちは、 アプリオリこれは、プロ細動性不整脈を発症するリスクが高いことを示唆しています。
臨床的に有意な不応性の変動は、次の 2 つのケースで発生する可能性があります。1) 重度の収縮機能障害を伴う器質性心疾患の存在。 2) イオン輸送障害(チャネル障害、電解質の不均衡)。 どちらの場合も、心周期のすべての段階での電気的興奮の分布は均一ではありません。これは、再分極(相対的不応性)の瞬間に、心電図的に次の現象と同等の早期活動電位が発生する条件が生じることを意味します。期外収縮。 期外収縮の興奮前線は同じ非同期であるため、再分極中は、次の電波がいくつかの波に分割され、心房または心房内で細動活動が発生するまで、別の期外収縮などが現れる可能性が高くなります。心室。
例 1. 急性心筋梗塞中に、別の PVC が多形性 VT を引き起こし、VF に変化しました。
例 2. 重度の低カリウム血症 (1.7 mmol/l) の患者。 「巨大な」Q-T 間隔 (~750 ミリ秒)。 このような背景から、多局性の異所性収縮が頻繁に発生します。 心室細動を発症するリスクが高い:

不応性の分散は電気生理学的概念ですが、臨床医によって説明的な意味で使用されることが多く、生命を脅かす心室頻拍性不整脈のリスク増加のマーカーとして、左心室収縮機能不全の計器的兆候の存在に基づいて検証されます。 いくつかのイオン輸送障害を除いて、不応性の分散は直接的な心電図症状を呈しません。
1.ショートインターバル「PQ」(< 0,12 с):
CLC症候群:
2. 長い間隔「PQ」(>0.2 秒):
・第1度房室ブロック。

· 第 2 度房室ブロック、PQ 間隔が継続的に増加するタイプ 2 (「徐脈」のセクションを参照)。

3. QRS コンプレックスの直後の「P」は負です。
· 心室の以前の興奮と AV 接続のリズム (「徐脈」のセクションを参照)。

P波とQRSの間には関係がありません
・3度AVブロックまたは完全AVブロック(PP間隔あり) · AV 解離 (PP>RR の間隔) - 「徐脈」のセクションを参照。 IV. 「R」波 胸部の「R」波の振幅のダイナミクスの変化は次のようになります。 A) V5 ~ 6 の高振幅「R」波と V1 ~ 2 の深い「S」波 + 心臓の電気軸の左への偏位 (RI>RII>RIII および SIII>SI)。 V5(V6)のR > 25 mm; V1 の S + V5(V6) の R > 35 mm; avL > 11 mm の R: · B) V1、V2 および深部での高いまたは分割された R 波、幅は広くない (0.04 秒未満) V5 ~ 6 の S 波 + 心臓の電気軸の右への偏位 (RIII>RII>RI および SI> SIII) V1 の R > 7 mm; V5(V6) > 7 mm の S: · 右心室心筋の肥大。 V.Q波 A) 波の幅が 0.03 秒未満、および/または振幅がこのリードの R 波の 1/4 未満である – 普通「Q」波。 B) 波の幅が 0.03 秒を超えている、および/または振幅がこのリードの R 波の 1/4 を超えている – 病的な Q波: 急性巨巣性心筋梗塞。 心筋の瘢痕性変化。 診断は、QRS 群、ST セグメント、および T 波の変化のダイナミクスの評価に基づいて行われます。 VI. QRSコンプレックス QRS コンプレックスの幅 A. 狭い複合施設(QRS)<0,12 с):
上室性(上室性)リズム(ヒス束の枝に沿ったインパルス伝達の中断なし - 心室内遮断): – 洞調律(洞調律「P」波は「QRS」群の前に記録されます)。 – 心房調律(QRS波の前に、非洞起源の「P」波が記録されます)。 – AV接続リズム: · 以前の心室興奮がある場合: 「QRS」群が記録され、その直後または負の「P」波が記録されます。 · 心室と心房の同時興奮:「QRS」波は記録されますが、「P」波は記録されません。 B. ワイドコンプレックス (QRS >0.12 秒): 1. ヒス束枝の遮断を伴う上室性(上室性)リズム。
任意の起源(任意の極性、構成)の「P」波は、心室複合体の前、または幅の広い「QRS」複合体上の陰性、またはその直後に記録され、次のタイプのいずれかに従って変形されます。 A) V5、V6 (I、aVL) 誘導では、R 波は幅が広く、頂点が丸くなっています。V1、V2 (III、aVF) では、S 波は深く、電気軸が左に偏っています (RI>RII>RIII およびSIII>SI): · フル - 「QRS」コンプレックスの幅 > 0.12 秒。 · 不完全 – 「QRS」コンプレックスの幅を持つ< 0,12 с. B) V1、V2誘導(III、aVF)におけるQRS群の「M」字型の分割。 幅は広い (0.04 秒以上) が、浅い (< 7 мм) зубец S в отведениях V5, V6 (I, аVL) + отклонение электрической оси вправо (RIII>RII>RI および SI>SIII): * フル – QRS コンプレックス幅 > 0.12 秒。 * 不完全 – QRS コンプレックスの幅あり< 0,12 с. 2.固有の心室(心室)リズム。
「P」波はなく、幅が広く変形した「QRS」群が記録され、神経束枝の完全なブロックと同様に、30 拍/分以下の徐脈周波数が続きます。 左心室の調律(心電図による BE の兆候 P NPG) :
右心室のリズム(心電図による BE の兆候 L NPG) :
3. ウォルフ・パーキンソン・ホワイト症候群または現象 (WPW または VPU 症候群または現象)。
· · デルタ波(「バレリーナの足」、「ステップ」)。 · ST セグメントと T 波の不一致な変位を伴う、広範囲に変形した QRS 群。 追加のケント束に沿った興奮は、AV結節を介するよりも速く心室に伝わり、心室の基底部の脱分極の追加の波、つまりデルタ波を形成します。 その結果、P-Q(R) 間隔が短縮され、QRS 群の持続時間が長くなり、変形します。 ECG 徴候のみが記録される場合、これは WPW 現象と呼ばれ、ECG 変化が発作性心拍リズム障害と組み合わされる場合、これは WPW 症候群と呼ばれます。 VI. STセグメント 1. 等値線の上の ST セグメントのシフト
– 心筋梗塞の急性期
: いくつかの誘導では、T 波への移行に伴い上向きに凸状に ST セグメントが上昇し、逆の誘導では ST セグメントが低下します。 Q 波は頻繁に記録され、その変化は動的です。 T 波は、ST セグメントがベースラインに戻る前に負になります。 – 急性心膜炎、心筋炎
: 多くの誘導(I ~ III、aVF、V 3 ~ V 6)での ST セグメントの上昇、相互誘導(aVR を除く)での ST 低下の欠如、Q 波の欠如、PQ セグメントの低下。 変更は動的です。 ST セグメントがベースラインに戻った後、T 波は負になります。 – PVR (心室性期外再分極症候群):
一致する T 波への凸状の下向き移行を伴う ST セグメントの上昇 R 波の下降膝部のノッチ 幅の広い対称的な T 波 ST セグメントと T 波の変化は永続的です。 標準のバリエーションです。 – バゴトニア
. 2. 等値線の下の ST セグメントの変位:
– IHD
: ・心内膜下MIまたは相反性(大きな焦点または経壁MIの領域が局在する壁の反対側の壁に対応するリードにおけるSTセグメントの下方への変位)。 · 狭心症の発作中。 – 心室肥大における収縮期過負荷
: 負の T 波への凸状の上向き移行を伴う ST セグメントの斜めの低下。 – 強心配糖体による飽和
または配糖体中毒 :
ST セグメントの谷型のくぼみ。 二相性または陰性 T 波。変化は左前胸部誘導でより顕著です。 – 低カリウム血症
: PQ間隔の延長、QRS波の拡大(まれに)、顕著なU波、平坦化した逆T波、STセグメントの低下、QT間隔のわずかな延長。 STセグメント低下の変異型 VI. 「T」波 1. V1 ~ V3 の正の高振幅の尖った「T」波: – – バゴトニア; – 高カリウム血症; – アドレナリン作動性の影響; – アルコール性心筋ジストロフィー; – 心室肥大を伴う拡張期過負荷。 2. V1 ~ V3 (V4) の負の「T」波: A) 健康な人の場合: – 小児および「青少年」の心電図; – 過呼吸を伴う。 – 炭水化物食品を食べた後。 B) 主な原因: – 虚血性心疾患の症状: – 心膜炎および心筋炎; – 僧帽弁逸脱を伴う。 – 右心室の不整脈原性異形成およびHCM、アルコール性心疾患を伴う。 – 急性および慢性肺性心症の場合。 – ホルモン異常性心筋ジストロフィーを伴う。 B) 二次的な原因: – 心室肥大中の収縮期過負荷。 – WPW シンドロームまたはバンドル ブランチ ブロックのコンポーネント。 – 脳血管障害; – 頻脈後症候群およびシャテリエ症候群(心刺激後症候群)。 – 胃腸疾患(膵炎); – 中毒(CO、有機リン化合物); – 気胸; – 強心配糖体による飽和。 VII. QT間隔 QT間隔の延長。 男性のQTc > 0.46、女性のQTc > 0.47。 (QTc = QT/ÖRR)。 a. 先天性 QT 間隔延長:ロマーノ・ウォード症候群(聴覚障害なし)、エルベル・ランゲ・ニールセン症候群(難聴あり)。 b. 獲得されたQT延長:特定の薬剤の服用(キニジン、プロカインアミド、ジソピラミド、アミオダロン、ソタロール、フェノチアジン、三環系抗うつ薬、リチウム)、低カリウム血症、低マグネシウム血症、重度の徐脈性不整脈、心筋炎、僧帽弁逸脱、心筋虚血、甲状腺機能低下症、低体温、低カロリー液体タンパク質食。 QT間隔の短縮。 QT< 0,35 с при ЧСС 60-100 мин –1 . Наблюдается при гиперкальциемии, гликозидной интоксикации. 心拍数に応じた適切な QT 間隔とその偏差 (%) 新しいメッセージを作成します。 すでに登録済みの場合は、「ログイン」してください (サイト右上のログイン フォーム)。 初めての方はご登録をお願いいたします。 登録すると、メッセージへの反応をさらに追跡し、興味深いトピックについて他のユーザーやコンサルタントと対話を続けることができます。 さらに、登録すると、コンサルタントやサイトの他のユーザーとプライベートなやり取りを行うことができます。 登録する登録せずにメッセージを作成する 質問、回答、その他の意見についての意見を書いてください。 これは、ECG (一般的には - 心臓の心電図)。 今日のトピックを理解するには、以下を読む必要があります。 心臓伝導システム (必須)、パート 1: 心電図検査の理論的基礎 心電図が反映する 電気プロセスのみ心筋内:心筋細胞の脱分極(興奮)と再分極(回復)。 比率 心電図間隔と 心周期の段階(心室収縮期と拡張期)。 通常、脱分極は筋細胞の収縮につながり、再分極は弛緩につながります。 さらに単純化するために、「脱分極-再分極」の代わりに「収縮-弛緩」を使用することもありますが、これは完全に正確ではありません。「」という概念があります。 電気機械解離この場合、心筋の脱分極と再分極は目に見える収縮と弛緩を引き起こしません。 この現象については以前にもう少し詳しく書きました。 ECG の解読に進む前に、ECG がどのような要素で構成されているかを理解する必要があります。 ECG 上の波形と間隔. あらゆる ECG は次のものから構成されます。 歯, セグメントそして 間隔. 歯- 心電図上の凹凸です。 (心房の収縮)、(3 つの波すべてが心室の収縮を特徴づけます)、(心室の弛緩)、(非定常波、めったに記録されません)。 セグメント 間隔 ECG 上の波形、セグメント、間隔。 心室心筋は心房心筋よりも大きく、壁だけでなく巨大な心室中隔もあるため、その中での興奮の広がりは複雑な複合体の出現を特徴とします。 QRS心電図上で。 正しく行う方法 その中の歯を強調表示します? まず第一に彼らは評価します 個々の歯の振幅(サイズ) QRSコンプレックス。 振幅が超えると 5mm、歯が示しています 大文字 Q、R、または S; 振幅が 5 mm 未満の場合、 小文字(小さい): q、r、または s。 R波(r)はと呼ばれます 何らかのポジティブな QRS コンプレックスの一部である (上向き) 波。 歯が複数ある場合は、後続の歯が示す ストローク: R、R’、R” など QRS 群の負(下向き)波、位置 R波の前、Q(q) として表され、 後 - S のように(s)。 QRS 群に正の波がまったくない場合、心室群は次のように指定されます。 QS. QRS コンプレックスのバリアント。 通常、歯は心室中隔の脱分極を反映し、歯は心室心筋の大部分を反映し、歯は心室中隔の基底部(つまり、心房近く)の部分を反映します。 RV1、V2 波は心室中隔の興奮を反映し、RV4、V5、V6 波は左心室と右心室の筋肉の興奮を反映します。 心筋領域の壊死(たとえば、心筋梗塞時)により Q 波が広くなり、深くなるため、この波には常に細心の注意が払われます。 一般的な ECG デコード図 ECG 登録の正確性をチェックします。 心拍数と伝導率の分析: 心臓の収縮の規則性の評価、心拍数 (HR) のカウント、興奮源の特定、伝導率の評価。 心臓の電気軸の決定。 心房 P 波および P-Q 間隔の分析 心室 QRST 複合体の分析: QRS 複合体分析、RS-T セグメント分析、T 波分析、Q-T 間隔分析 心電図レポート。 正常な心電図。 1) 正しい ECG 登録を確認する 各 ECG テープの先頭には、 校正信号- いわゆる 基準ミリボルト。 これを行うには、記録の開始時に 1 ミリボルトの標準電圧が適用されます。これにより、偏差が表示されます。 10mm。 キャリブレーション信号がないと、ECG 記録は不正確であると見なされます。 通常、標準または強化された四肢誘導の少なくとも 1 つでは、振幅は次の値を超える必要があります。 5mm、そして胸の中で導かれます - 8mm。 振幅が低い場合は、と呼ばれます。 ECG電圧の低下、これはいくつかの病的状態で発生します。 基準ミリボルト ECG上(記録の開始時)。 2) 心拍数と伝導分析: 心拍数の規則性の評価 リズムの規則性が評価されます R-R間隔による。 歯が互いに等しい距離にある場合、そのリズムは規則的、または正しいと呼ばれます。 個々の R-R 間隔の期間の変動は、以下の範囲内で許容されます。 ±10%平均持続時間から。 リズムが正弦波であれば、通常は規則的です。 心拍数計測(心拍数) ECG フィルムには大きな正方形が印刷されており、各正方形には 25 個の小さな正方形 (縦 5 個 x 横 5 個) が含まれています。 正しいリズムで心拍数をすばやく計算するには、隣接する 2 つの歯 R - R の間にある大きな正方形の数を数えます。 ベルト速度 50 mm/s の場合: HR = 600 (大きな正方形の数)。 上にある ECG では、R-R 間隔は約 4.8 個の大きなセルであり、25 mm/s の速度で次のようになります。 300 / 4.8 = 62.5 拍/分 それぞれ25mm/sの速度で スモールセルに等しい 0.04秒、速度 50 mm/s - 0.02秒。 これは、歯の長さと間隔を決定するために使用されます。 リズムが間違っている場合、通常は次のように考えられます。 最大心拍数と最小心拍数それぞれ最小および最大の R-R 間隔の継続時間に応じて。 励振源の決定 言い換えれば、彼らはどこにあるのかを探しています。 ペースメーカー、心房と心室の収縮を引き起こします。 興奮性と伝導のさまざまな障害が非常に混乱して組み合わされる可能性があり、誤った診断や誤った治療につながる可能性があるため、これは場合によっては最も困難な段階の 1 つです。 ECG 上の興奮源を正確に判断するには、心臓の伝導システムについての十分な知識が必要です。 洞調律(これは正常なリズムであり、他のすべてのリズムは病的です)。 標準誘導 II では、P 波は常に正であり、各 QRS 群の前に位置し、同じ誘導内の P 波は一定の同一形状を持ちます。 洞調律の P 波。 心房リズム。 興奮源が心房の下部にある場合、興奮波は心房に下から上に伝播します (逆行性)。 II 誘導と III 誘導では P 波は負であり、各 QRS 群の前に P 波があります。 心房調律中の P 波。 AV接続によるリズム。 ペースメーカーが房室にある場合 ( 房室結節)ノード、その後、心室は通常どおり(上から下に)興奮し、心房は逆行します(つまり、下から上に)。 同時に、心電図では次のことが行われます。 P 波は通常の QRS 群に重畳されるため存在しない可能性があり、P 波は QRS 群の後に位置する負の値になる場合があります。 房室接合部からのリズム、QRS 群への P 波の重ね合わせ。 房室接合部からのリズム、P 波は QRS 群の後に位置します。 房室接合部からのリズムの心拍数は洞調律より小さく、毎分約 40 ~ 60 拍です。 心室性リズム、または心室性リズム(ラテン語の ventriculus - 心室から)。 この場合、リズムの源は心室伝導系です。 興奮は心室を通じて間違った方向に広がるため、速度が遅くなります。 心室固有調律の特徴: QRS コンプレックスは広がって変形します (「怖く」見えます)。 通常、QRS 群の持続時間は 0.06 ~ 0.10 秒であるため、このリズムでは QRS は 0.12 秒を超えます。 房室接合部は心室からインパルスを放出せず、通常どおり心房は洞結節から興奮する可能性があるため、QRS 波と P 波の間にパターンはありません。 心拍数が毎分 40 拍未満。 固有心室調律。 P 波は QRS 群とは関連しません。 導電率評価. 導電性を評価するには、以下を測定します。 間隔 P波(心房を通るインパルス伝達の速度を反映します)、通常は最大 0.1秒。 間隔 間隔 P - Q(心房から心室心筋へのインパルス伝導の速度を反映します)。 間隔 P - Q = (波 P) + (セグメント P - Q)。 大丈夫 0.12~0.2秒。 間隔 QRSコンプレックス(心室を通じた興奮の広がりを反映します)。 大丈夫 0.06~0.1秒. 内部偏差間隔リード V1 と V6 にあります。 これは、QRS 群の開始から R 波までの時間です。 V1 では最大 0.03 秒そしてで V6 最大 0.05 秒。 これは主に、脚ブロックを認識し、心室期外収縮 (心臓の異常な収縮) の場合に心室の興奮源を特定するために使用されます。 内部偏差間隔を測定します。 3) 心臓の電気軸の決定. 4) 心房P波解析. 通常、P 波の持続時間は次を超えません。 0.1秒、その振幅は 1.5 ~ 2.5 mm です。 P 波の病理学的逸脱: II、III、aVF 誘導における通常持続時間の尖った高 P 波は、 右心房肥大たとえば「肺心」。 2つの頂点で分割され、I、aVL、V5、V6誘導の幅が広がったP波が特徴的です。 左心房肥大たとえば、僧帽弁欠損の場合です。 P 波 (P 肺) の形成右心房の肥大を伴います。 P波(P-僧帽弁)の形成左心房の肥大を伴います。 P-Q間隔: 大丈夫 0.12~0.20秒. AVブロック 3 度があります: I 度 - P-Q 間隔は増加しますが、各 P 波には独自の QRS 群があります ( 複合体を失わない)。 II 度 - QRS 群 部分的に抜け落ちる、つまり すべての P 波が独自の QRS 群を持っているわけではありません。 Ⅲ度 - 完全な伝導遮断 AV ノード内。 心房と心室は、互いに独立して独自のリズムで収縮します。 それらの。 心室固有調律が発生します。 5) 心室 QRST 分析: QRS複合解析. 心室複合体の最大持続時間は、 0.07~0.09秒(最大0.10秒)。 持続時間はバンドル分岐ブロックごとに増加します。 通常、Q 波は、V4 ~ V6 だけでなく、すべての標準および強化された四肢誘導でも記録できます。 通常、Q 波の振幅は次を超えません。 1/4R波高、持続時間は 0.03秒。 リード aVR では、通常、深くて広い Q 波があり、QS 複合体さえあります。 R 波は、Q 波と同様、すべての標準および強化された四肢誘導で記録できます。 V1 から V4 まで、振幅は増加し (rV1 波は存在しない可能性があります)、その後 V5 と V6 で減少します。 S 波の振幅は非常に異なる場合がありますが、通常は 20 mm を超えません。 S 波は V1 から V4 に減少し、V5 から V6 には存在しないこともあります。 リード V3 (または V2 - V4 間) 移行ゾーン」(R波とS波の等しい)。 RS-Tセグメント分析 S-T セグメント (RS-T) は、QRS 群の終わりから T 波の始まりまでのセグメントであり、冠動脈疾患の場合、S-T セグメントは酸素不足 (虚血) を反映するため、特に注意深く分析されます。心筋で。 通常、S-T セグメントは等値線上の四肢誘導に位置します ( ±0.5mm)。 リード V1 ~ V3 では、S-T セグメントが上方に (2 mm 以下)、リード V4 ~ V6 では下に (0.5 mm 以下) シフトする可能性があります。 QRS 群が S-T セグメントに移行する点は、点と呼ばれます (ジャンクション - 接続という言葉から)。 点 j の等値線からの逸脱の度合いは、心筋虚血の診断などに使用されます。 T波解析. T 波は心室心筋の再分極のプロセスを反映します。 高い R が記録されるほとんどのリードでは、T 波もプラスになります。 通常、T 波は I、II、aVF、V2 ~ V6 で常に正であり、TI > TIII、TV6 > TV1 です。 aVR では、T 波は常に負です。 Q-T間隔分析. Q-T間隔と呼ばれます 電気的心室収縮期、この時点では心臓の心室のすべての部分が興奮しているためです。 時々、T波の後に小さな波が起こります。 U波、これは、再分極後の心室心筋の興奮性が短期的に増加するために形成されます。 6) 心電図レポート. リズムのソース(洞かどうか)。 リズムの規則性(正しいかどうか)。 通常、洞調律は正常ですが、呼吸性不整脈が発生する可能性があります。 心拍数。 心臓の電気軸の位置。 4つの症候群の存在:調律障害、伝導障害、心室および心房の肥大および/または過負荷、心筋損傷(虚血、ジストロフィー、壊死、瘢痕) 結論の例(完全ではありませんが、実際のものです): 心拍数に応じた洞調律 65。心臓の電気軸の正常な位置。 病理は特定されなかった。 心拍数 100 の洞性頻脈。単一の上室性期外収縮。 心拍数 70 ビート/分の洞調律。 右脚の遮断が不完全。 心筋における中程度の代謝変化。 心臓血管系の特定の疾患に対する ECG の例 - 次回。 心電図の種類についてコメントでよく質問があったため、説明します。 干渉心電図に現れる可能性があります。 3 種類の ECG 干渉(以下で説明します)。 医療従事者の用語集における ECG への干渉は、 密告: 19 世紀の 70 年代にイギリス人 A. ウォーラーによって実用化された、心臓の電気活動を記録する装置は、今日に至るまで忠実に人類に貢献し続けています。 もちろん、ほぼ 150 年にわたって多くの変更や改良が加えられてきましたが、心筋内を伝播する電気インパルスの記録に基づく動作原理は変わっていません。 現在、ほぼすべての救急車チームには、軽量で持ち運び可能なポータブル心電計が装備されており、貴重な時間を無駄にすることなく、迅速に心電図を測定し、急性心臓病状を診断し、患者を迅速に病院に搬送することができます。 広範囲の限局性心筋梗塞、肺塞栓症、その他の緊急処置が必要な病気の場合は一刻を争うため、緊急に心電図検査を行うことで、毎日複数の命が救われます。 心臓病チームの医師が心電図を解読することは一般的なことであり、それが急性心血管病変の存在を示している場合、チームはすぐにサイレンを鳴らして病院に行き、救急治療室を迂回して患者を搬送します。緊急治療のため集中治療室へ。 診断は心電図を使用してすでに行われており、時間のロスはありません。 そうです、患者はレコーダーが残したテープに残った奇妙な歯が何を意味するのか知りたいので、医者に行く前に自分で心電図を解読したいと考えています。 しかし、すべてはそれほど単純ではなく、「洗練された」記録を理解するには、人間の「モーター」が何であるかを知る必要があります。 人間を含む哺乳類の心臓は、補助的な機能を備え壁が比較的薄い 2 つの心房と、主な負荷を担う 2 つの心室の 4 つの部屋で構成されています。 心臓の左右の部分も異なります。 右心室にとって、肺循環に血液を供給することは、左心室で体循環に血液を押し込むよりも難しくありません。 したがって、左心室はより発達しますが、より多くの損傷を受けます。 しかし、違いに関係なく、心臓の両方の部分は均等かつ調和して機能する必要があります。 収縮要素(心筋)と非収縮要素(神経、血管、弁、脂肪組織)の電気的反応の程度が互いに異なるため、心臓はその構造と電気活動が不均一です。 通常、患者、特に高齢者の患者は、心電図に心筋梗塞の兆候があるかどうかを心配しますが、これは非常に理解できます。 ただし、これを行うには、心臓と心電図について詳しく学ぶ必要があります。 そして、波、間隔、リード、そしてもちろん、いくつかの一般的な心臓病について話すことで、この機会を提供しようと努めます。 心臓の具体的な機能については、まず学校の教科書で学ぶので、心臓には次のような機能があると想像します。 自動的に、インパルスの自発的発生によって引き起こされ、その後その励起が引き起こされます。 興奮性または興奮した衝動の影響下で活性化する心臓の能力。 導電率または、インパルスの発生場所から収縮構造への伝導を確実にする心臓の「能力」。 収縮性つまり、インパルスの制御下で収縮および弛緩する心筋の能力。 張性、心臓は拡張期にその形状を失わず、継続的な周期的活動を保証します。 一般に、穏やかな状態(静電気分極)の心筋は電気的に中性であり、 生体電流(電気プロセス)は、励起インパルスの影響下でその中で形成されます。 心臓における電気的プロセスは、最初は心筋細胞の外側に存在するナトリウムイオン (Na+) の心筋細胞内への移動と、細胞内から外側へ勢いよく流れるカリウムイオン (K+) の移動によって引き起こされます。 この動きは、心周期全体を通して膜内外電位差の変化の条件を作り出し、繰り返されます。 脱分極(興奮、その後収縮)そして 再分極(元の状態に遷移します)。 すべての心筋細胞は電気活動を持っていますが、ゆっくりとした自発的脱分極は伝導系の細胞にのみ特徴的であり、それが自動化が可能な理由です。 心筋の外表面で興奮が起こると、この部分は興奮の影響を受けない領域と比較して電気陰性になります。 しかし、体の組織は導電性を持っているという事実により、生体電流は体の表面に投影され、曲線の形で移動するテープ、つまり心電図に記録および記録されます。 ECG は各心拍の後に繰り返される波形で構成されており、それらを通じて人間の心臓に存在する障害を示します。 おそらく多くの人がこの質問に答えることができるでしょう。 必要に応じて心電図検査を行うことも難しくありません。すべての診療所に心電計があります。 心電図技術? 一見すると、誰もがよく知っているように見えますが、心電図検査について特別な訓練を受けた医療従事者だけが知っています。 しかし、いずれにしても準備なしにそのような作業を行うことを誰も許可しないため、詳細に入る必要はほとんどありません。 患者は、適切な準備方法を知る必要があります。つまり、過食、喫煙、アルコール飲料や薬の摂取、重労働、手術前にコーヒーを飲まないことをお勧めします。騙される可能性がある。 別の何かではないにしても、頻脈は確実に発生します。 したがって、完全に落ち着いた患者は上半身まで服を脱ぎ、足を解放してソファに横たわり、看護師は必要な場所(リード)を特別な溶液で潤滑し、さまざまな色のワイヤーが装置に接続される電極を適用します。そして心電図を撮ります。 後で医師が解読しますが、興味がある場合は、自分で歯と間隔を調べてみることもできます。 このセクションはすべての人にとって興味深いものではない可能性があります。その場合は読み飛ばしていただいてもかまいませんが、自分で心電図を理解しようとしている人にとっては役に立つかもしれません。 ECG の波形は、ラテン文字 P、Q、R、S、T、U を使用して指定され、それぞれが心臓のさまざまな部分の状態を反映しています。 P – 心房脱分極。 QRS波複合体 - 心室脱分極。 T – 心室再分極。 弱い U 波は、心室伝導系の遠位部分の再分極を示している可能性があります。 ECG を記録するには、通常 12 個のリードが使用されます。 3 つの標準 – I、II、III; 3つの強化された単極肢リード(Goldbergerによる)。 6 強化された単極胸部 (ウィルソンによる)。 場合によっては(不整脈、心臓の位置の異常)、Neb によれば、追加の単極胸部リードと双極リードを使用する必要があります (D、A、I)。 ECG 結果を解釈するとき、その成分間の間隔の継続時間が測定されます。 この計算はリズム周波数を評価するために必要であり、さまざまなリードの歯の形状とサイズがリズムの性質、心臓で発生する電気現象、および(ある程度は)個人の電気活動の指標となります。心筋の部分、つまり心電図は、その時点または別の期間で心臓がどのように機能するかを示します。
ECGのより厳密な解釈は、特別なリード(ベクトル理論)を使用して歯の面積を分析および計算することによって行われますが、実際には、主に次のような指標で対応します。 電気軸方向、これは合計 QRS ベクトルです。 胸部の構造は人それぞれ異なり、心臓の配置はそれほど厳密ではないことは明らかです。心室の重量比とその内部の伝導率も人によって異なります。したがって、解読する際には、このベクトルの水平方向または垂直方向が重要になります。と示されている。 医師は順番に心電図分析を実行し、基準と違反を判断します。 心臓のリズムを評価し、心拍数を測定します(通常の ECG - 洞調律、心拍数 - 1 分あたり 60 ~ 80 拍)。 間隔 (QT、標準 – 390 ~ 450 ミリ秒) が計算され、特別な式 (私はよくバゼットの式を使用します) を使用して収縮期 (収縮期) の期間を特徴付けます。 この間隔が長くなる場合、医師は虚血性心疾患、アテローム性動脈硬化症、心筋炎、リウマチを疑う権利があります。 逆に、高カルシウム血症は QT 間隔の短縮につながります。 インターバルを通じて反射されたパルスの導電率はコンピューター プログラムを使用して計算され、結果の信頼性が大幅に向上します。 EOS の位置は、歯の高さに沿った等値線から計算され始めます (通常、R は常に S よりも高い)。S が R を超えて軸が右にずれると、EOS の活動の乱れが考えられます。右心室が逆の場合 - 左心室、IIおよびIII誘導でSの高さがRより大きい場合 - 左心室肥大が疑われます。 QRS複合体が研究されます。QRS複合体は、心室筋への電気インパルスの伝導中に形成され、心室筋の活動を決定します(標準は病的なQ波がないこと、複合体の幅は120ミリ秒以下です) 。 この間隔が変化する場合、束の枝の(完全または部分的な)遮断または伝導障害について話します。 さらに、右脚の不完全な遮断は右心室肥大の心電図基準であり、左脚の不完全な遮断は左心室肥大を示している可能性があります。 これらは、完全な脱分極後の心筋の初期状態の回復期間を反映する ST セグメント (通常は等値線上に位置します) と、上向きの両心室の再分極のプロセスを特徴付ける T 波について説明します。 、非対称であり、その振幅は持続時間が波よりも低く、QRS 群よりも長くなります。 解読作業は医師のみが行いますが、一部の救急車救急隊員は一般的な病状を完全に認識しており、これは緊急事態において非常に重要です。 ただし、その前に、ECG の基準を知る必要があります。 正常な心電図 これは、心臓がリズミカルかつ正確に機能する健康な人の心電図の様子ですが、この記録が何を意味するのか誰もが知っているわけではなく、妊娠などのさまざまな生理学的条件によって変化する可能性があります。 妊娠中の女性では、胸部内の心臓の位置が異なるため、電気軸が移動します。 また、持続時間に応じて心臓への負担も加わります。 妊娠中の心電図にはこれらの変化が反映されます。 小児の心電図指標も優れています。乳児の成長とともに成長するため、年齢に応じて変化します。12 歳を過ぎて初めて、小児の心電図は成人の心電図に近づき始めます。 心電図上の非公開型心臓発作 もちろん、ECG で最も深刻な診断は心筋梗塞であり、その認識において心電図が主な役割を果たします。なぜなら、壊死領域を見つけて病変の位置と深さを決定するのは(最初の!)心電図だからです。 、急性梗塞と動脈瘤や過去の傷跡を区別することができます。 ECG 上の心筋梗塞の典型的な兆候は、深い Q 波 (OS) の記録です。 セグメント標高STこれにより R が変形し、滑らかになり、その後負の尖った二等辺歯 T が現れます。ST セグメントのこの隆起は視覚的に猫の背中 (「猫」) に似ています。 ただし、Q 波がある心筋梗塞とない心筋梗塞は区別されます。
ECG の結論には、「左心室肥大」という表現がよく見られます。 原則として、このような心電図は、肥満などにより心臓に長期間にわたって追加の負荷がかかった人々によって取得されます。 このような状況では、左心室に負担がかかることは明らかです。 すると電気軸が左にずれ、S>Rとなります。 ECG上の心臓の左心室(左心室)と右心室(右心室)の肥大
洞性不整脈は興味深い現象であり、恐れる必要はありません、健康な人に存在し、症状や影響を与えず、むしろ心臓を休めるのに役立つため、健康な人の心電図とみなされます。
心室内インパルス伝導の違反は、房室遮断および脚ブロックとして現れます。 右脚ブロック - 右前胸誘導の高くて広い R 波、 左足ブロック- 右胸のリードでは小さな R と広く深い S 波、左胸ではリード - R は広くなりギザギザになっています。 両脚は、心室複合体の拡張とその変形によって特徴付けられます。 房室ブロック、心室内伝導の混乱を引き起こす速度は 3 段階で表され、伝導が心室にどのように到達するかによって決まります。ゆっくりと、時々、またはまったく到達しません。 しかし、これらはすべて「花」であると言えるかもしれません。なぜなら、症状がまったくないか、それほどひどい症状が現れないからです。たとえば、房室ブロックでは息切れ、めまい、倦怠感が発生する可能性があり、それでもなお、 3 学位までしか取得できず、そのうち 1 学位は訓練を受けた若者にとって一般的です。
リズム障害と伝導障害に対しては、毎日のホルター監視が処方されています、無痛性の冠状動脈性心疾患、プリンツメタル狭心症およびその他の病理学的状態。 また、ホルター術の使用の適応症は、患者に人工ペースメーカーが存在する場合(その機能を制御する場合)、および抗不整脈薬および虚血の治療のための薬を使用する場合である。 準備をしましょうホルター心電図モニタリングも簡単ですが、髪があると記録が歪んでしまうため、男性は電極の取り付け部分を剃る必要があります。 毎日のモニタリングには特別な準備は必要ないと考えられていますが、原則として、患者には何ができるか、何ができないかを知らされます。 もちろん、お風呂に浸ることはできません;このデバイスは水処理を好みません。 シャワーすら受け付けない人もいますが、残念ながら我慢するしかありません。 デバイスは次のことに敏感です 磁石、電子レンジ、金属探知機、高圧線したがって、強度をテストしないほうがよいでしょう。それでも間違って書き込まれます。 彼はそれが気に入らない 合成繊維あらゆる種類の金属製のジュエリーがあるため、しばらくの間は、これらに切り替える必要があります。 綿の服そして宝石のことは忘れてください。
誰もがそのような自転車について聞いたことがあるでしょうが、誰もがそれに乗ったことがあるわけではありません(そして、誰もが乗れるわけではありません)。 実際のところ、隠れた冠状動脈循環不全、興奮性、伝導障害は、安静時の心電図ではほとんど検出されないため、用量を増加させながら心電図を記録する、いわゆる自転車エルゴメーター検査を使用するのが通例です(場合によっては)。定数)負荷。 負荷を伴う ECG の間、この処置に対する患者の全体的な反応、血圧、脈拍が同時に監視されます。 ストレスの種類 ECG: エアロバイクとトレッドミルを使用 自転車エルゴメトリックテスト中の最大心拍数は年齢に依存し、200拍から年数を引いた値になります。つまり、20歳なら180拍/分まで耐えられますが、60歳になると130拍/分が限界となります。 。 必要に応じて、自転車エルゴメーターテストが処方されます。 潜在的な形で発生する冠状動脈性心疾患、調律障害、伝導障害の診断を明確にする。 冠状動脈性心疾患の治療の有効性を評価する。 IHD の診断が確立されているための薬剤を選択します。 心筋梗塞を患った患者のリハビリ期間中のトレーニングと負荷レジメンを選択します( MIの発症から1か月が経過する前に、これは専門クリニックでのみ可能です!); 冠状動脈性心疾患に苦しむ患者の状態の予後評価を提供する。 しかし、負荷をかけてECGを行うことには禁忌もあり、特に心筋梗塞、狭心症、大動脈瘤、一部の期外収縮、ある段階の慢性心不全、脳血管障害、血栓性静脈炎の疑いは検査の障害となります。 これらの禁忌は、 絶対. このほかにも、いくつかあります 相対的禁忌:一部の心臓欠陥、動脈性高血圧、発作性頻脈、頻繁な期外収縮、房室ブロックなど。 FCG または心音図研究方法を使用すると、心臓の音の症状をグラフィックで描写し、それを客観化し、音やノイズ (形状と継続時間) を心周期の位相と正確に関連付けることができます。 さらに、音韻は、Q - I 音、僧帽弁が開く音 - II 音など、いくつかの時間間隔を決定するのに役立ちます。 PCG 中には、心電図も同時に記録されます (必須条件)。 心音検査法は単純であり、最新の装置を使用すると、音の高周波成分と低周波成分を分離して、研究者の知覚に最も適したものとして表示することができます(聴診と同様)。 しかし、病理学的ノイズを捕捉する場合、FCG は感度がそれほど高くないため、聴診法よりも優れているわけではありません。そのため、FCG は依然として医師を音内視鏡に置き換えることはできません。 心音検査は、心雑音の原因や心臓弁膜症の診断を明らかにする必要がある場合、心臓欠陥に対する外科的介入の適応を決定する必要がある場合、また心筋梗塞後に異常な聴診症状が現れた場合に処方されます。 活動性リウマチ性心炎の場合、心臓欠陥の形成パターンを明らかにするために、および感染性心内膜炎の場合には、PCG を使用した動的研究が必要です。 ステップ1:フォームで相談料をお支払い → ステップ2:お支払い後、下記フォームよりご質問ください↓ ステップ 3:さらに任意の金額を支払って専門家に感謝することもできます R 波の上昇が低いという一般的な ECG 症状は、医師によって誤解されることがよくあります。 この症状は通常、前部心筋梗塞に関連していますが、梗塞に関連しない他の病気によって引き起こされる場合もあります。 R 波のわずかな増加がおよそ次の時点で検出されます。 成人入院患者の10%
これは 6 番目に一般的な心電図異常です (メトロポリタン生命保険会社が 5 年半の間に 19,734 件の心電図を収集)。 その上、 前部心筋梗塞の既往歴のある患者の3分の1
心電図にはこの症状しかない場合があります。 したがって、この心電図現象の特定の解剖学的等価物を解明することは臨床的に非常に重要です。 リード V3 の通常の R 波高は通常 2 mm 以上です
。 V1~V4誘導におけるR波の高さが極端に小さい場合、「R波の増加が不十分または小さい」といわれます。 梗塞による心筋壊死では、一定量の心筋組織が電気的に不活性になり、正常な脱分極を生成できなくなります。 このとき、周囲の心室組織の脱分極が増加し(それらに対する抵抗がなくなるため)、結果として生じる脱分極ベクトルは、壊死ゾーンから離れる方向に再配向されます(妨げられない伝播の方向に)。 前部心筋梗塞では、右誘導と中央誘導(V1~V4)にQ波が現れます。 しかし、かなりの数の患者では、Q 波が保存されていません。 過去に前部心筋梗塞を起こした記録のある症例では、 R 波のわずかな増加が 20 ~ 30% の症例で検出されます。
. 病的なQ波が完全に消失するまでの平均時間は1.5年です。
注目を集める I誘導におけるR波の振幅の減少
。 前部心筋梗塞患者の最大 85% で、R 波がわずかに増加していますが、いずれかの症状がみられます。 I誘導におけるR波の振幅<= 4 мм
、 または V3誘導におけるR波の振幅<= 1,5 мм
。 これらの振幅基準がないため、前部心筋梗塞の診断は可能性が低くなります(前部心筋梗塞症例の 10% ~ 15% を除く)。 前胸誘導で R 波がわずかに増加している場合、 リード V1 ~ V3 の再分極障害 (ST-T 変化)
陳旧性前部心筋梗塞と診断される可能性が高くなります。 前胸部誘導における R 波の成長が不十分なその他の考えられる原因は: R 波がわずかに増加するもう 1 つの一般的な理由は、電極の位置が間違っていることです。胸部の電極が高すぎるか低すぎる、電極が手足から胴体まで配置されているなどです。 糖尿病患者における心電図上の R 波のわずかな増加と拡張機能障害との間に関連性が確認されているため、この症状は糖尿病患者における左室機能障害および DCM の初期兆候である可能性があります。 7.2.1. 心筋肥大 肥大の原因は、一般に、抵抗(動脈高血圧)または容積(慢性腎不全および/または心不全)による心臓への過剰な負荷です。 心臓の働きが増加すると、心筋における代謝プロセスが増加し、その後、筋線維の数が増加します。 心臓の肥大した部分の生体電気活動が増加し、それが心電図に反映されます。 7.2.1.1. 左心房肥大 左心房肥大の特徴的な兆候は、P 波の幅の増加 (0.12 秒以上) です。 2 番目の兆候は、P 波の形状の変化です (2 番目のピークが優勢な 2 つのこぶ) (図 6)。 米。 6. 左心房肥大の心電図 左心房肥大は僧帽弁狭窄症の典型的な症状であるため、この疾患の P 波は P 僧帽弁と呼ばれます。 同様の変化が誘導 I、II、aVL、V5、V6 でも観察されます。 7.2.1.2. 右心房肥大 右心房の肥大に伴い、変化はP波にも影響し、尖った形状となり振幅が増加します(図7)。 米。 7. 右心房 (P-肺)、右心室 (S 型) の肥大の ECG 右心房の肥大は、心房中隔欠損、肺循環の高血圧とともに観察されます。 ほとんどの場合、このような P 波は肺の病気で検出され、P 肺と呼ばれることがよくあります。 右心房肥大は、II、III、aVF、V1、V2 誘導における P 波の変化の兆候です。 7.2.1.3. 左心室肥大 心臓の心室はストレスに対してよりよく適応しており、初期段階では心室の肥大は心電図に現れない可能性がありますが、病状が進行するにつれて特徴的な兆候が目に見えるようになります。 心室肥大では、心房肥大よりも ECG に大幅に多くの変化が見られます。 左心室肥大の主な兆候は次のとおりです (図 8)。 心臓の電気軸の左への偏位(レボグラム)。 遷移ゾーンの右へのシフト (リード V2 または V3)。 V5、V6 誘導の R 波は高く、RV4 よりも振幅が大きくなります。 リード V1、V2 の深い S。 リード V5、V6 の拡張 QRS コンプレックス (最大 0.1 秒以上)。 上に凸の等電位線の下の S-T セグメントの変位。 I、II、aVL、V5、V6 誘導における陰性 T 波。 米。 8. 左心室肥大の心電図 左心室肥大は、動脈性高血圧症、先端巨大症、褐色細胞腫のほか、僧帽弁および大動脈弁不全、先天性心疾患などでよく観察されます。 7.2.1.4. 右心室肥大 進行した症例では、右心室肥大の兆候が心電図に現れます。 肥大の初期段階での診断は非常に困難です。 肥大の兆候 (図 9): 心臓の電気軸の右への偏位(プラボグラム)。 V1 誘導では深い S 波、III、aVF、V1、V2 誘導では高い R 波。 RV6 の歯の高さは通常よりも低くなります。 リード V1、V2 の拡張 QRS コンプレックス (最大 0.1 秒以上)。 リード V5 と V6 の深い S 波。 右の III、aVF、V1、および V2 で上に凸の等値線の下の S-T セグメントの変位。 右脚の完全または不完全な遮断。 トランジションゾーンを左にシフトします。 米。 9. 右心室肥大の心電図 右心室肥大は、肺疾患、僧帽弁狭窄症、壁血栓症、肺動脈狭窄症、および先天性心疾患における肺循環圧の上昇と最も多く関連しています。 7.2.2. リズム障害 脱力感、息切れ、心拍数の上昇、頻繁な呼吸困難、心臓機能の中断、窒息感、失神、または意識喪失のエピソードは、心血管疾患による心拍リズム障害の症状である可能性があります。 ECGは、それらの存在を確認するのに役立ち、そして最も重要なことに、それらのタイプを決定するのに役立ちます。 自動性は心臓の伝導系の細胞の固有の特性であり、リズムを制御する洞結節が最も大きな自動性を持っていることを覚えておく必要があります。 心電図に洞調律が認められない場合は、リズム障害(不整脈)と診断されます。 正常な洞調律の兆候: P 波の周波数 – 60 ~ 90 (1 分あたり) の範囲。 R-R 間隔の持続時間は同じ。 aVR を除くすべての誘導で正の P 波。 心拍リズム障害は非常に多様です。 すべての不整脈は、定所性不整脈(洞結節自体に変化が生じる)と異所性不整脈に分けられます。 後者の場合、興奮性インパルスは洞結節の外側、つまり心房、房室接合部および心室(ヒス束の枝)で発生します。 定常性不整脈には、洞性徐脈、頻脈、および不規則な洞調律が含まれます。 異所性 - 心房細動、粗動、その他の障害。 不整脈の発生が興奮性の機能不全に関連している場合、そのようなリズム障害は期外収縮と発作性頻脈に分類されます。 ECG で検出できる不整脈の種類はさまざまであることを考慮して、医学の複雑さで読者を飽きさせないよう、著者は基本的な概念を定義し、最も重大なリズム障害と伝導障害についてのみ考察することにしました。 7.2.2.1. 洞性頻脈 洞結節でのインパルスの生成が増加します(1 分あたり 100 インパルスを超える)。 ECG 上では、正常な P 波の存在と R-R 間隔の短縮によって明らかです。 7.2.2.2. 洞性徐脈 洞結節でのパルス発生頻度は 60 を超えません。 ECG 上では、正常な P 波の存在と R-R 間隔の延長によって明らかです。 収縮頻度が 30 未満の場合、徐脈は洞性ではないことに注意してください。 頻脈と徐脈のどちらの場合も、患者はリズム障害を引き起こした病気の治療を受けます。 7.2.2.3. 不規則な洞調律 インパルスは洞結節内で不規則に生成されます。 ECG は正常な波形と間隔を示しますが、R-R 間隔の継続時間は少なくとも 0.1 秒異なります。 このタイプの不整脈は健康な人でも発生する可能性があり、治療の必要はありません。 7.2.2.4. 固有心室調律 異所性不整脈。ペースメーカーが束枝またはプルキンエ線維のいずれかである。 非常に重度の病状。 ECG 上でまれなリズム (つまり、1 分あたり 30 ~ 40 拍)、P 波が存在せず、QRS 波形が変形して拡大します (持続時間 0.12 秒以上)。 重度の心臓病状でのみ発生します。 このような疾患を患う患者は緊急治療が必要であり、心臓集中治療室に即時に入院する必要があります。 7.2.2.5. 期外収縮 単一の異所性衝動によって引き起こされる心臓の異常な収縮。 実際上重要なのは、期外収縮を上室性と心室に分けることです。 心臓の異常な興奮(収縮)を引き起こす病巣が心房にある場合、上室性(心房とも呼ばれる)期外収縮が ECG に記録されます。 心室期外収縮は、心室の 1 つに異所性病巣が形成されると心電図に記録されます。 期外収縮はまれで、頻繁に発生する場合(1 分間に心臓の収縮の 10% 以上)、一対(二回以上の心臓収縮)、グループ(連続して 3 回以上)の場合があります。 心房期外収縮の ECG 兆候をリストしてみましょう。 P 波の形状と振幅が変化しました。 P-Q 間隔が短縮されます。 早期に記録された QRS 群は、正常な (洞) 群と形状が変わりません。 期外収縮に続く R-R 間隔は通常よりも長くなりますが、通常の 2 つの間隔 (不完全な代償休止) よりは短くなります。 心房性期外収縮は、心硬化症や冠状動脈性心臓病を背景に高齢者に多く見られますが、たとえば、非常に心配している場合やストレスを感じている場合など、実質的に健康な人でも観察されることがあります。 実質的に健康な人で期外収縮が認められた場合、治療はバロコルディン、コルバロールを処方し、完全な休息を確保することから構成されます。 患者に期外収縮を登録する場合は、基礎疾患の治療とイソプチン グループの抗不整脈薬の服用も必要です。 心室期外収縮の兆候: P 波は存在しません。 異常な QRS 群は大幅に拡大され (0.12 秒以上)、変形しています。 完全な代償一時停止。 心室期外収縮は常に心臓の損傷(虚血性心疾患、心筋炎、心内膜炎、心臓発作、アテローム性動脈硬化)を示します。 1分間に3~5回の収縮を繰り返す心室期外収縮の場合、抗不整脈療法が必須です。 リドカインは静脈内に投与されることがほとんどですが、他の薬剤も使用できます。 治療は注意深く心電図をモニタリングしながら行われます。 7.2.2.6. 発作性頻脈 突然の超頻繁な収縮の発作で、数秒から数日間続きます。 異所性ペースメーカーは、心室または上室のいずれかに位置します。 上室性頻拍(この場合、インパルスは心房または房室結節で形成されます)では、1 分あたり 180 ~ 220 回の収縮の頻度で正しいリズムが ECG に記録されます。 QRS 群は変更されたり拡大されたりしません。 発作性頻脈の心室型では、P 波が ECG 上の位置を変えることがあり、QRS 群が変形して広がります。 上室性頻脈はウォルフ・パーキンソン・ホワイト症候群で発生しますが、急性心筋梗塞ではあまり一般的ではありません。 心室型の発作性頻脈は、心筋梗塞、虚血性心疾患、電解質代謝障害の患者で検出されます。 7.2.2.7. 心房細動(心房細動) 上室性不整脈の一種で、心房の非同期で調整されていない電気活動とその後の収縮機能の低下によって引き起こされます。 衝動の流れは完全に心室に伝わるわけではなく、心室は不規則に収縮します。 この不整脈は、最も一般的な心拍リズム障害の 1 つです。 60歳以上の患者の6%以上、この年齢未満の患者の1%で発生します。 心房細動の兆候: R-R間隔が異なる(不整脈)。 P 波はありません。 フリッカー波が記録されます(誘導 II、III、V1、V2 で特にはっきりと見えます)。 電気的交流(1本のリード線のI波の異なる振幅)。 心房細動は、僧帽弁狭窄症、甲状腺中毒症、心硬化症によって発生し、心筋梗塞によって発生することもよくあります。 医療は洞調律を回復することです。 プロカインアミド、カリウム製剤、その他の抗不整脈薬が使用されます。 7.2.2.8. 心房粗動 心房細動よりも発生頻度ははるかに低いです。 心房粗動では、心房の通常の興奮と収縮がなくなり、個々の心房線維の興奮と収縮が観察されます。 7.2.2.9. 心室細動 最も危険で重度のリズム障害であり、急速に血液循環の停止につながります。 心筋梗塞中だけでなく、臨床的に死亡した状態にある患者のさまざまな心血管疾患の末期段階でも発生します。 心室細動の場合は、緊急の蘇生措置が必要です。 心室細動の兆候: 心室複合体の歯がすべて欠如している。 すべてのリードの細動波を 1 分あたり 450 ~ 600 波の頻度で記録します。 7.2.3. 伝導障害 興奮の伝達の減速または完全な停止の形でインパルスの伝導に障害が発生した場合に生じる心電図の変化は、遮断と呼ばれます。 封鎖は、違反が発生したレベルに応じて分類されます。 洞房遮断、心房遮断、房室遮断、および心室内遮断があります。 これらの各グループはさらに細分化されます。 例えば、I度、II度、III度の洞房遮断、右脚と左脚の遮断があります。 より詳細な分割(左脚前枝の遮断、右脚不完全遮断)もあります。 ECG を使用して記録された伝導障害の中で、次の遮断が実際的に最も重要です。 洞房III度。 房室 I、II、III 度。 左右の束の枝を封鎖します。 7.2.3.1. III度洞房ブロック 洞結節から心房への興奮の伝導が遮断される伝導障害。 一見正常な ECG では、次の収縮、つまり P-QRS-T 複合体全体 (または一度に 2 ~ 3 個の複合体) が突然消失します (ブロックされます)。 代わりにアイソラインが記録されます。 この病状は、冠状動脈疾患、心臓発作、心硬化症を患っている人、および多くの薬剤(ベータ遮断薬など)を使用している場合に観察されます。 治療は、基礎疾患の治療と、アトロピン、イサドリンおよび類似の薬剤の使用で構成されます。 7.2.3.2. 房室ブロック 房室接続を介した洞結節からの興奮の伝導障害。 房室伝導の遅延は、第 1 度房室ブロックです。 正常な心拍数での P-Q 間隔の延長 (0.2 秒以上) として ECG 上に現れます。 第 2 度房室ブロックは、洞結節から来るすべてのインパルスが心室心筋に到達するわけではない不完全なブロックです。 ECG では、次の 2 種類の遮断が区別されます。1 つ目は Mobitz-1 (Samoilov-Wenkebach)、2 つ目は Mobitz-2 です。 Mobitz-1 型封鎖の兆候: 継続的に伸びるPインターバル 最初の兆候の結果、P 波後のある段階で QRS コンプレックスは消失します。 Mobitz-2 タイプのブロックの兆候は、P-Q 間隔の延長を背景とした QRS 群の周期的な損失です。 3度房室ブロックは、洞結節から来る単一のインパルスが心室に伝えられない状態です。 ECG は、互いに関連のない 2 種類のリズムを記録します。心室 (QRS 群) と心房 (P 波) の働きは調整されていません。 第 3 度遮断は、心硬化症、心筋梗塞、強心配糖体の不適切な使用などでよく起こります。 患者にこの種の遮断が存在する場合は、心臓病病院に緊急入院する必要があることを示しています。 治療にはアトロピン、エフェドリン、場合によってはプレドニゾロンが使用されます。 7.2.Z.Z. ブランチブロックをバンドルする 健康な人では、洞結節から発生しヒ束の枝を通過する電気インパルスが両方の心室を同時に興奮させます。 右脚または左脚が遮断されると、インパルス経路が変化するため、対応する心室の興奮が遅れます。 不完全な遮断、および束枝の前枝および後枝のいわゆる遮断も可能です。 右脚の完全な遮断の兆候 (図 10): 変形して広がった (0.12 秒以上) QRS 群。 V1 誘導と V2 誘導で負の T 波。 等値線からの S-T セグメントの変位。 RsR の形式でのリード V1 と V2 の QRS の拡大と分割。 米。 10. 右脚の完全なブロックを含む心電図 左脚の完全な封鎖の兆候: QRS 群が変形して広がります (0.12 秒以上)。 等値線からの S-T セグメントのオフセット。 V5 誘導と V6 誘導では負の T 波。 RR の形式でのリード V5 と V6 の QRS 群の拡張と分割。 rS の形での V1 誘導と V2 誘導における QRS の変形と拡張。 これらのタイプの遮断は、心臓損傷、急性心筋梗塞、アテローム性動脈硬化症および心筋硬化症の場合、および多くの薬剤(強心配糖体、ノボカインアミド)の不適切な使用によって発生します。 心室内ブロックのある患者には特別な治療は必要ありません。 彼らは封鎖の原因となった病気の治療のため入院している。 7.2.4. ウォルフ・パーキンソン・ホワイト症候群 この症候群 (WPW) は、1930 年に上記の著者によって、健康な若者に観察される上室性頻拍の一種 (「機能性脚ブロック」) として初めて記載されました。 体内では、洞結節から心室までの通常のインパルス伝導経路に加えて、追加の束が存在する場合があることが現在確立されています(ケント、ジェームス、マハイム)。 これらの経路に沿って、興奮はより速く心臓の心室に到達します。 WPW 症候群にはいくつかのタイプがあります。 興奮が左心室に早く入る場合、WPW 症候群タイプ A は ECG に記録されますが、タイプ B では、興奮が右心室に早く入ります。 WPW 症候群 A 型の兆候: QRS 群のデルタ波は、右前胸部誘導では正、左では負になります (心室の一部の時期尚早興奮の結果)。 胸部リードの主歯の方向は、左脚の遮断の場合とほぼ同じです。 WPW 症候群 B 型の兆候: P-Q 間隔の短縮 (0.11 秒未満)。 QRS 群が拡大し (0.12 秒以上)、変形します。 右胸のリードでは負のデルタ波、左胸のリードでは正のデルタ波。 胸部リードの主歯の方向は、右脚枝の遮断の場合とほぼ同じです。 変形していない QRS 群とデルタ波 (ロウ・ガノン・レビン症候群) の欠如により、急激に短縮された P-Q 間隔を記録することが可能です。 追加のバンドルは継承されます。 症例の約 30 ~ 60% では、症状は現れません。 人によっては頻脈性不整脈の発作を起こす場合があります。 不整脈が発生した場合には、原則に基づいて診療を行います。 7.2.5. 初期の心室再分極 この現象は、心血管病理の患者の 20% で発生します (上室性心調律障害の患者で最もよく見られます)。 これは病気ではありませんが、この症候群を経験した心血管疾患の患者は、調律障害や伝導障害に苦しむ可能性が 2 ~ 4 倍高くなります。 初期の心室再分極の兆候 (図 11) には以下が含まれます。 ST セグメントの上昇。 後期デルタ波(R 波の下降部分のノッチ)。 高振幅の歯。 通常の持続時間と振幅の双峰型 P 波。 PR および QT 間隔の短縮。 胸部のR波の振幅が急速かつ急激に増加します。 米。 11. 早期心室再分極症候群の心電図 7.2.6. 心虚血 冠状動脈性心疾患(CHD)では、心筋への血液供給が障害されます。 初期段階では心電図に変化がない場合もありますが、後期では非常に顕著になります。 心筋ジストロフィーの発症に伴い、T 波の変化と心筋のびまん性変化の兆候が現れます。 これらには次のものが含まれます。 R 波の振幅の減少。 S-Tセグメントの低下。 ほぼすべての誘導で二相性、適度に広がった平坦な T 波。 IHD は、心筋の異栄養性変化やアテローム性心硬化症だけでなく、さまざまな原因の心筋炎の患者にも発生します。 7.2.7. 狭心症 狭心症の発作が進行すると、ECG により、血液供給が障害された領域の上に位置する誘導における S-T セグメントの変位と T 波の変化が明らかになります (図 12)。 米。 12. 狭心症の心電図(発作時) 狭心症の原因は高コレステロール血症、脂質異常症です。 さらに、動脈性高血圧、糖尿病、精神的・感情的過負荷、恐怖、肥満も発作の発症を引き起こす可能性があります。 心筋虚血が発生する層に応じて、次のような症状があります。 心内膜下虚血(虚血領域にわたって、S-T 変位は等値線より下にあり、T 波は正で、振幅が大きい)。 心外膜下虚血(等値線より上の S-T セグメントの上昇、T 陰性)。 狭心症の発生には、通常、身体活動によって引き起こされる典型的な胸痛の出現が伴います。 この痛みは本質的に差し迫ったもので、数分間続きますが、ニトログリセリンを服用すると消えます。 痛みが 30 分以上続き、ニトロ薬を服用しても軽減されない場合は、急性の局所変化が考えられます。 狭心症の救急治療には、痛みを和らげ、発作の再発を防ぐことが含まれます。 鎮痛薬(アナルギンからプロメドールまで)、ニトロ薬(ニトログリセリン、ススタック、ニトロン、モノシンクなど)、バリドール、ジフェンヒドラミン、セデュセンが処方されます。 必要に応じて酸素吸入を行います。 7.2.8. 心筋梗塞 心筋梗塞は、心筋の虚血領域における長期にわたる循環障害の結果として生じる心筋の壊死の発症です。 90% 以上の場合、診断は心電図を使用して決定されます。 さらに、心電図により、心臓発作の段階を判断し、その位置と種類を知ることができます。 心臓発作の無条件の兆候は、過剰な幅(0.03 秒以上)とより深い深さ(R 波の 3 分の 1)を特徴とする病的な Q 波が ECG 上に現れることです。 可能なオプション: QS、QrS。 S-T シフト (図 13) と T 波反転が観察されます。 米。 13. 前外側心筋梗塞(急性期)の心電図。 左心室の後下部分に瘢痕性変化がある 場合によっては、病的な Q 波が存在せずに S-T 変位が発生することがあります (小局所心筋梗塞)。 心臓発作の兆候: 梗塞領域の上に位置するリードの病理学的 Q 波。 梗塞領域の上に位置するリードの等値線に対して上向きの円弧による S-T セグメントの変位 (持ち上げ)。 梗塞領域の反対側のリードにおけるS-Tセグメント等値線の下の不一致な変位。 梗塞領域の上に位置するリードの陰性 T 波。 病気が進行すると、心電図が変化します。 この関係は、心臓発作中の変化の段階によって説明されます。 心筋梗塞の発症には 4 つの段階があります。 急性; 亜急性; 傷だらけのステージ。 最も急性の段階 (図 14) は数時間続きます。 このとき、S-T セグメントは ECG 上の対応する誘導で急激に上昇し、T 波と融合します。 米。 14. 心筋梗塞中の一連の ECG 変化: 1 – Q 梗塞。 2 – Q-梗塞ではない。 A – 最も急性期。 B – 急性期。 B – 亜急性期。 D – 瘢痕段階(梗塞後の心硬化症) 急性期では、壊死領域が形成され、病的な Q 波が現れ、R 振幅は減少し、S-T セグメントは上昇したままとなり、T 波は陰性になります。 急性期の期間は平均して1~2週間程度です。 梗塞の亜急性期は 1 ~ 3 か月間続き、壊死巣の瘢痕化組織化を特徴とします。 この時点の ECG では、S-T セグメントが徐々に等値線に戻り、Q 波が減少し、逆に R 振幅が増加します。 T波は陰性のままです。 瘢痕化段階は数年間続く場合があります。 このとき、瘢痕組織の組織化が起こります。 ECG では、Q 波は減少するか完全に消え、S-T は等電線上に位置し、負の T は徐々に等電になり、その後正になります。 この位相は、心筋梗塞中の ECG の自然なダイナミクスと呼ばれることがよくあります。 心臓発作は心臓のどの部分にも局在する可能性がありますが、最も多くの場合は左心室で発生します。 位置に応じて、左心室の前側壁と後壁の梗塞が区別されます。 変化の局在化と範囲は、対応するリードの ECG 変化を分析することによって明らかになります (表 6)。 表 6. 心筋梗塞の局在化 すでに変化した心電図に新たな変化が重なると、再発性梗塞を診断する際に大きな困難が生じます。 短い間隔で心電図を記録する動的モニタリングが役立ちます。 典型的な心臓発作は、ニトログリセリンを服用しても消えない灼熱の重度の胸痛を特徴とします。 非定型的な心臓発作もあります。 腹部(心臓と胃の痛み); 喘息(心臓の痛みおよび心臓喘息または肺水腫); 不整脈(心臓の痛みとリズム障害); 虚脱性(心臓の痛みと大量の発汗を伴う血圧の急激な低下)。 痛みはありません。 心臓発作の治療は非常に困難な作業です。 一般に、困難が増すほど、病変はより広範囲に広がります。 同時に、ロシアのゼムストヴォ医師の一人の適切な発言によれば、非常に重度の心臓発作の治療が予想外にスムーズに進むこともあれば、合併症のない単純な微小梗塞が医師にインポテンスの兆候を示すこともあるという。 救急治療は、痛みを和らげる(この目的のために麻薬やその他の鎮痛剤が使用されます)、鎮静剤の助けを借りて恐怖や精神的興奮を取り除く、心臓発作の領域を縮小する(ヘパリンを使用する)、そして順次排除することで構成されます。危険の程度に応じて他の症状も現れます。 心臓発作を起こした患者は、入院治療が終了した後、リハビリのために療養所に送られます。 最終段階は地元の診療所での長期観察です。 7.2.9. 電解質障害による症候群 特定の ECG 変化により、心筋内の電解質含有量の動態を判断することが可能になります。 公平を期すために言うと、血液中の電解質のレベルと心筋内の電解質の含有量の間には、必ずしも明確な相関関係があるわけではないと言わなければなりません。 それにもかかわらず、ECG によって検出された電解質障害は、医師が診断を探索する過程や正しい治療法を選択する際に重要な助けとなります。 ECGにおける最もよく研究されている変化は、カリウムおよびカルシウム代謝の障害である(図15)。 米。 15. 電解質障害の ECG 診断 (A.S. Vorobyov、2003): 1 – 正常。 2 – 低カリウム血症。 3 – 高カリウム血症。 4 – 低カルシウム血症。 5 – 高カルシウム血症 7.2.9.1. 高カリウム血症 高カリウム血症の兆候: 背が高く、尖ったT波。 Q-T間隔の短縮。 R の振幅が減少しました。 重度の高カリウム血症では、心室内伝導障害が観察されます。 高カリウム血症は、糖尿病(アシドーシス)、慢性腎不全、筋肉組織の粉砕を伴う重傷、副腎不全、その他の疾患で発生します。 7.2.9.2。 低カリウム血症 低カリウム血症の兆候: S-Tセグメントが下方に減少。 陰性または二相性の T; Uさんの登場。 重度の低カリウム血症では、心房および心室の期外収縮および心室内伝導障害が現れます。 低カリウム血症は、重度の嘔吐、下痢、利尿薬、ステロイドホルモンの長期使用後、および多くの内分泌疾患を患っている患者においてカリウム塩が失われると発生します。 治療は、体内のカリウム欠乏を補充することから始まります。 7.2.9.3. 高カルシウム血症 高カルシウム血症の兆候: Q-T間隔の短縮。 S-Tセグメントの短縮。 心室複合体の拡張。 カルシウムの大幅な増加を伴うリズム障害。 高カルシウム血症は、副甲状腺機能亢進症、腫瘍による骨破壊、ビタミンD過剰症、カリウム塩の過剰投与などで観察されます。 7.2.9.4。 低カルシウム血症 低カルシウム血症の兆候: QT間隔の期間を長くする。 S-T セグメントを延長します。 T 振幅の減少。 低カルシウム血症は、重度の膵炎やビタミンD欠乏症を伴う慢性腎不全の患者において、副甲状腺の機能低下に伴って発生します。 7.2.9.5。 配糖体中毒 強心配糖体は、心不全の治療に長い間使用されて成功してきました。 これらのツールはかけがえのないものです。 それらを摂取すると、心拍数(心拍数)が低下し、収縮期の血液の排出がより活発になります。 その結果、血行動態パラメータが改善され、循環不全の症状が減少します。 配糖体の過剰摂取の場合、特徴的な ECG 兆候が現れ (図 16)、中毒の重症度に応じて用量の調整または薬物の中止が必要になります。 グリコシド中毒の患者は、吐き気、嘔吐、心臓機能の中断を経験することがあります。 米。 16. 強心配糖体の過剰摂取の場合の心電図 グリコシド中毒の兆候: 心拍数の低下。 電気的収縮期の短縮。 S-Tセグメントが下方に減少。 陰性T波。 心室期外収縮。 配糖体による重度の中毒の場合は、薬物の使用を中止し、カリウムサプリメント、リドカイン、ベータ遮断薬を処方する必要があります。


左心室心筋肥大
 – 左脚ブロック:
– 左脚ブロック:
 – 右脚ブロック:
– 右脚ブロック:

 PQ 間隔を短縮します。
PQ 間隔を短縮します。

WPW症候群におけるECGの形成


 IHD (心外膜下虚血、相互変化);
IHD (心外膜下虚血、相互変化);
心拍数 相対QT–ダウアー
80%
90%
100%
110%
120%
130%
140%
QT 間隔の期間 (ミリ秒)
0,38
0,43
0,48
0,53
0,57
–
–
0,36
0,41
0,45
0,50
0,54
0,59
–
0,34
0,38
0,43
0,47
0,51
0,56
–
0,33
0,37
0,41
0,45
0,49
0,53
0,57
0,31
0,35
0,39
0,43
0,47
0,51
0,55
0,30
0,34
0,37
0,41
0,45
0,49
0,52
0,29
0,32
0,36
0,40
0,43
0,47
0,51
0,28
0,31
0,35
0,38
0,42
0,45
0,49
0,27
0,30
0,34
0,37
0,41
0,44
0,47
0,26
0,29
0,33
0,36
0,39
0,43
0,46
0,25
0,29
0,32
0,35
0,38
0,41
0,45
0,25
0,28
0,31
0,34
0,37
0,40
0,43
0,24
0,27
0,30
0,33
0,36
0,39
0,42
0,23
0,26
0,29
0,32
0,35
0,37
0,40
0,22
0,25
0,28
0,30
0,33
0,36
0,39
0,21
0,24
0,27
0,29
0,32
0,34
0,37
0,20
0,23
0,26
0,28
0,31
0,33
0,36
0,20
0,22
0,25
0,27
0,30
0,32
0,35
–
0,21
0,24
0,26
0,29
0,31
0,33
–
0,20
0,23
0,25
0,27
0,29
0,32
正常な心電図の要素
不思議なことに、海外では通常、P-Q間隔と呼ばれています。 PR.
ECG では次の波が識別されます。
ECG 上のセグメントは次のように呼ばれます。 直線セグメント隣接する 2 つの歯の間の (等値線)。 最も重要なセグメントは P-Q と S-T です。 たとえば、P-Q セグメントは、房室 (AV-) 結節における興奮伝導の遅延により形成されます。
間隔は次のとおりです。 歯(歯の複合体)とセグメント。 したがって、間隔 = 歯 + セグメントとなります。 最も重要なのは、P-Q 間隔と Q-T 間隔です。
大きなセルと小さなセルに注意してください (詳細は以下を参照)。QRS複素波

心電図分析

ベルト速度 25 mm/s の場合: HR = 300 (大きな正方形の数)。
興奮の源はここにある 洞房結節。 ECG 上の兆候:
導電率を適切に考慮するために、記録速度が考慮されます。
ECG シリーズの最初の部分では、心臓の電気軸とは何か、またそれが前頭面でどのように決定されるかについて説明しました。
通常、誘導 I、II、aVF、V2 ~ V6 では、P 波が 常にポジティブな。 III、aVL、V1 誘導では、P 波は正または二相性になります (波の一部は正で、一部は負です)。 aVR誘導では、P波は常に負になります。

この間隔の増加は、房室結節を通るインパルスの伝導が障害されると発生します( 房室ブロック、AVブロック)。
以下を含める必要があります:
ECG干渉

a) 突入電流: ネットワークピックアップコンセントの交流の周波数に対応する50 Hzの周波数の規則的な振動の形で発生します。
b)」 水泳「電極と皮膚の接触不良による等値線の(ドリフト)。
c) 干渉による干渉 筋肉の震え(不規則な頻繁な振動が見られます)。患者さんが知りたいのは…

ハートアビリティ
心臓内の生体電流を記録可能
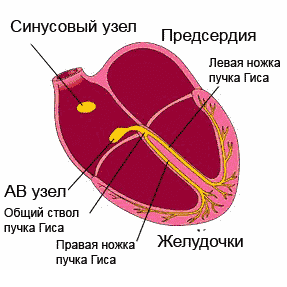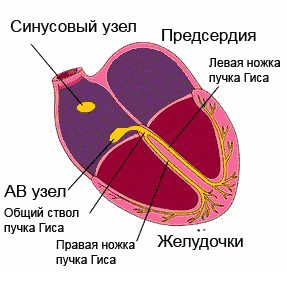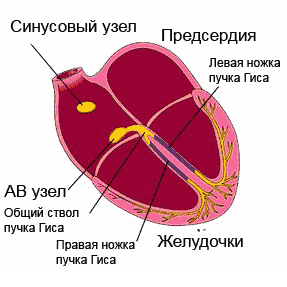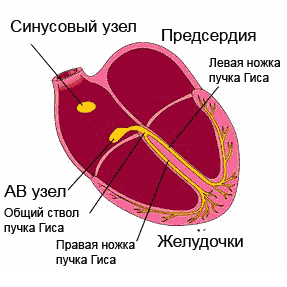 広がる興奮 伝導系、心臓の部分を順番にカバーします。 最大限の自動性を持つ洞房(洞房)結節(右心房の壁)から始まり、インパルスは心房筋、房室結節、ヒスと脚の束を通過し、心室に向けられ、各部位を刺激します。伝導システム自体の自動性が現れる前であっても。
広がる興奮 伝導系、心臓の部分を順番にカバーします。 最大限の自動性を持つ洞房(洞房)結節(右心房の壁)から始まり、インパルスは心房筋、房室結節、ヒスと脚の束を通過し、心室に向けられ、各部位を刺激します。伝導システム自体の自動性が現れる前であっても。心電図はどのように採取されますか?

歯、リード、インターバル


ビデオ: ECG 波形、セグメント、間隔に関するレッスン
心電図分析

最も残念な診断: 心臓発作


ビデオ: ECG 上の心臓発作の兆候
心に何か問題があるとき

ビデオ: ECG 上の心肥大

ビデオ: ECG 上の不整脈


ビデオ: ECG 遮断
ビデオ: ECG 上のバンドル枝ブロック
ホルター法
 HM ECG - これは何の略語ですか? 心電図を磁気テープに記録する携帯用テープレコーダーを用いて、長期間連続して心電図を記録すること(ホルター法)の名称です。 このような心電図は、定期的に発生するさまざまな障害を検出して登録するために使用されるため、通常の心電図では常にそれらを認識できるとは限りません。 さらに、特定の時間または特定の条件下で偏差が発生する可能性があるため、これらのパラメータを ECG 記録と比較するために、患者は非常に適切な検査を行う必要があります。 詳細な日記。 その中で、彼は自分の感情を説明し、休息、睡眠、覚醒、活動的な活動の時間を記録し、病気の症状や症状を書き留めます。 このようなモニタリングの期間は、研究が処方された目的によって異なりますが、最も一般的なのは日中の心電図の記録であるため、モニタリングと呼ばれます。 日当ただし、最新の機器では最大 3 日間の監視が可能です。 そして、皮下に埋め込まれるデバイスの場合はさらに時間がかかります。
HM ECG - これは何の略語ですか? 心電図を磁気テープに記録する携帯用テープレコーダーを用いて、長期間連続して心電図を記録すること(ホルター法)の名称です。 このような心電図は、定期的に発生するさまざまな障害を検出して登録するために使用されるため、通常の心電図では常にそれらを認識できるとは限りません。 さらに、特定の時間または特定の条件下で偏差が発生する可能性があるため、これらのパラメータを ECG 記録と比較するために、患者は非常に適切な検査を行う必要があります。 詳細な日記。 その中で、彼は自分の感情を説明し、休息、睡眠、覚醒、活動的な活動の時間を記録し、病気の症状や症状を書き留めます。 このようなモニタリングの期間は、研究が処方された目的によって異なりますが、最も一般的なのは日中の心電図の記録であるため、モニタリングと呼ばれます。 日当ただし、最新の機器では最大 3 日間の監視が可能です。 そして、皮下に埋め込まれるデバイスの場合はさらに時間がかかります。ビデオ: ホルターモニタリングに関する医師
自転車と心電図

心音検査とは何ですか?

R 波の変化を分析する前に、前胸部誘導における心室活性化の発生を理解するために必要ないくつかの理論的枠組みを思い出す必要があります。 心室脱分極は通常、心室中隔の左側の中央で始まり、前方および左から右に移動します。 この電気活動の初期ベクトルは、右胸部と中央胸部の誘導 (V1 ~ V3) に小さな r 波 (「」と呼ばれます) として現れます。 中隔波r").
初期の脱分極ベクトルの大きさが減少するか、逆向きになると、R 波のわずかな増加が発生する可能性があります。 中隔が活性化されると、左心室の脱分極が残りの脱分極プロセスを支配します。 右心室の脱分極は左心室と同時に起こりますが、その程度は正常な成人の心臓では無視できます。 結果として得られるベクトルは V1 ~ V3 誘導から導かれ、ECG 上に深い S 波として表示されます。
前胸部誘導における R 波の正規分布。
V1 誘導では、心室複合体は rS 型で表され、左誘導に対する R 波の相対的なサイズが着実に増加し、S 波の振幅が減少します。V5 誘導と V6 誘導は通常、qR 型を示します。複雑で、V5 の R 波の振幅は V6 よりも大きくなります。 肺組織による信号減衰.
通常の変動には、V1 の狭い QS および rSr" パターン、V5 および V6 の qRs および R パターンが含まれます。ある時点 (通常は V3 または V4) で、QRS 群は主に負の状態から主に正の状態に変化し始め、R/S比率は > 1 になります。このゾーンは「」として知られています。 移行ゾーン
一部の健康な人では、V2 の時点で移行ゾーンが見られます。これは「」と呼ばれます。 早期移行ゾーン
"。場合によっては、移行ゾーンが V4 から V5 まで遅れることがあります。これは " 後期移行ゾーン
"、 または " 移行ゾーンの遅延
".
文献では、R 波のわずかな増加についてさまざまな定義があり、次のような基準があります。V3 または V4 誘導で 2 ~ 4 mm 未満の R 波および/またはR波の逆成長の存在(RV4)< RV3 или RV3 < RV2 или RV2 < RV1 или любая их комбинация).
存在すると想定されるリード I の R 波<= 4,0 мм или зубцов R в отведении V3 <= 1,5 мм, указывает на старый передний инфаркт миокарда.

急性前心筋梗塞
ほとんどの場合、R 波の不十分な成長は、右胸部の電極の位置が高いことが原因で発生します。 電極を通常の位置に移動すると、R 波の通常の成長が回復しますが、 陳旧性前部心筋梗塞ではQS複合体は保存される
.
残念ながら、これらの基準は診断にはほとんど役に立たず、多くの偽陰性および偽陽性の結果が得られることが判明しました。
参考文献。